Ограниченно растворимыми называют жидкости, которые в пределах определенных концентраций и температур образуют одну гомогенную фазу; в другой области концентраций и температур система становится гетерогенной.
По характеру зависимости взаимной растворимости от температуры жидкости делятся на четыре типа: 1) с верхней критической температурой растворения; 2) с нижней критической температурой растворения; З) с верхней и нижней критическими температурами растворения; 4) без критических температур растворения.
Прибавляя анилин (компонент В) к воде (компонент А) небольшими порциями при температуре t и тщательно встряхивая, можно наблюдать, что до определенного состава х1 (рис. 8,а) система остается прозрачной — образуется однородный не насыщенный раствор анилина в воде. При достижении насыщения воды анилином (состав х1) дальнейшее добавление анилина вызывает помутнение системы, а при отстаивании — появление нового слоя — насыщенного раствора воды в анилине (состава х2). Система становится гетерогенной, жидкости более не растворяются друг в друге. В начале количество вновь образовавшегося слоя незначительно, но по мере добавления новых порций анилина оно растет, одновременно уменьшается количество водного слоя. Концентрация слоев при этом остается постоянным.
Наконец, слой, представляющий собой насыщенный раствор анилина в воде, исчезает. Остается раствор воды в анилине. С этого момента снова наблюдается не ограниченная взаимная растворимость жидкостей (область составов от х2 до 1,0).
Таким образом, в интервале составов от х1 до х2 при температуре t в системе сосуществует два насыщенных раствора постоянного состава. С увеличением температуры взаимная растворимость компонентов растет и область гетерогенном состояния уменьшается (при температуре она определяется составами от х3 до х4). Температуру, чуть выше которой наступает неограниченная взаимная растворимость компонентов, называют верхней критической температурой растворения tвкр (точка К). Температуру соответствующую появлению (или исчезновению) второй фазы, называют температурой гетерогеннизации (или гомогенизации) раствора данного состава. Таким образом, кривая LКС показывает зависимость температуры гомогенизации (или гетерогеннизации) растворов от их состава. Ветвь LК характеризует зависимость растворимости анилина в воде, а КС — воды в анилине от температуры. Любая точка на кривой LКС отражает составы насыщенных растворов выше кривой — поле 1 гомогенного состояния системы; слева — ненасыщенный раствор анилина в воде, справа — воды в анилине. Система в этом состоянии имеет две степени свободы (С=2-1+1=2), т.е. произвольно можно задавать температуру и состав. Область под кривой LKC отвечает двух фазному моновариантному состоянию системы (С=2-2+1=1), т.е. равновесные состояния из двух насыщенных растворов определенных составов возможно при строго заданной температуре. Например, фигуративная точка М отражает валовый (общий) состав системы. В этом случае система в равновесном состоянии двухфазна; составы фаз находят на пересечении изотермы, проведенной через точку М до пересечения с кривыми растворимости. Точка 1 характеризует состав насыщенного раствора анилина в воде или водный слой (хв=0.1) и точка 2 — воды в анилине или анилиновый слой (хв=0,95).
При изотермическом изменений валового состава системы, что соответствует перемещению фигуративной точки М в N, в системе увеличивается масса анилинового слоя и уменьшается масса водного слоя. Составы насыщенных растворов не меняются.
Рассмотрим пример охлаждения не насыщенного раствора анилина в воде состава х3 заданного точкой D. При охлаждении раствора до температуры t’ образуется анилиновый раствор состава х4 (точка 2’), которой обогащен анилином по сравнению с водным слоем. Следовательно, водный слой при дальнейшем охлаждении обогащается водой и его состав изменяется по кривой LК, а состав анилинового слоя —по кривой КС вниз (по направлению стрелок).
Ограниченно растворимые жидкости с критической температурой растворения (триэтиламин — вода, диэтиламин — вода). У жидкости данного типа взаимная растворимость компонентов А и В растет с уменьшением температуры и чуть ниже критической температуры растворения tнкр наступает неограниченная растворимость (рис. 8,б). Смысл полей, линий, точек и примеры чтения диаграммы аналогичный первому типу диаграмм.
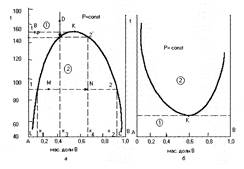
рис. 8
 2015-07-04
2015-07-04 3811
3811
