 (5.4)
(5.4)
Уравнение (5.4) можно преобразовать, заменив количество молей компонента 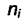 на его мольную долю
на его мольную долю 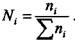 . Для этого нужно
. Для этого нужно
разделить 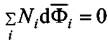 левую и правую части (5.4) на постоянную величину
левую и правую части (5.4) на постоянную величину 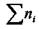 ∑ni:
∑ni:
Дифференцируя последнее выражение по мольной доле какого-либо компонента 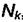 , получается ещё одна форма соотношения (5.4)
, получается ещё одна форма соотношения (5.4)
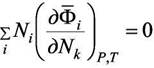
Если в качестве экстенсивного параметра взять изобарно-изотермический потенциал G, то приведённые выше уравнения называются уравнениями Гиббса-Дюгема. Их исключительное значение для теории растворов связано с тем, что молярная
парциальная величина G является химическим потенциалом i-го компонента по определению:
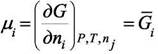
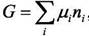
|
Для раствора можно записать
или при бесконечно малом
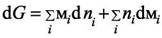
|
| изменении состава |
Совместная запись первого и второго закона термодинамики для открытых систем или фундаментальное уравнение Гиббса для величины dG 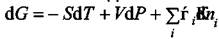 имеет вид
имеет вид
Разность последних двух уравнений приводит к одному из важнейших уравнений в теории растворов
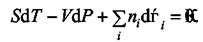 (5.5)
(5.5)
Уравнение (5.5) связывает между собой изменения давления, температуры и химических потенциалов компонентов раствора. При постоянных P и Т формула (5.5) преобразуется в уравнения Гиббса-Дюгема
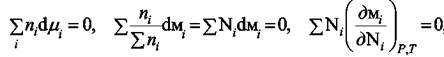 5
5
с помощью которых изучают взаимную зависимость химических потенциалов различных компонент раствора.
 2015-07-04
2015-07-04 355
355








