Скорость химической реакции зависит от энергии ее активации. Эта энергия необходима для эффективного соударения молекул (частиц), приводящего к их взаимодействию.
· Энергия активации (Еа) - энергия, необходимая для достижения системой переходного состояния, называемого активированным (или переходным) комплексом, который превращается в продукты реакции уже самопроизвольно.
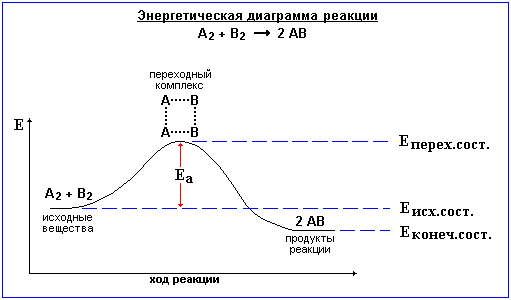
Изменение энергии в ходе реакции
Энергия активации Еа равна разности энергий переходного и исходного состояний:
Еа = Еперех.сост. - Еисх.сост.
Чем меньше энергия активации реакции, тем выше ее скорость. Эта зависимость выражается уравнением Аррениуса, которое связывает константу скорости реакции k с Еа:

 2015-07-03
2015-07-03 402
402








