Исходя из молекулярно-кинетических представлений, американский физико-химик И. Ленгмюр предложил модель адсорбции в системе твердое тело – газ, исходя из следующих положений. Во-первых, физическая адсорбция на границе твердое тело – газ происходит не на всей поверхности, а на так называемых активных центрах – участках поверхности, активно взаимодействующих с адсорбтивом. Во-вторых, энергия адсорбции – одна и та же для молекул адсорбтива. В соответствии с этими положениями при достижении состояния динамического равновесия (рис. 15) скорость адсорбции становится равна скорости десорбции – процессу, обратному адсорбции.
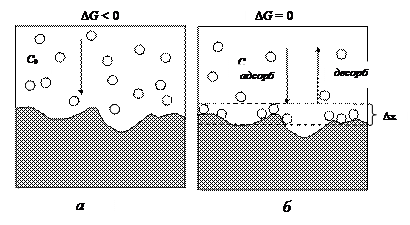
Рис. 15. Схема процесса адсорбции газа на твердой поверхности: а) состояние системы до начала процесса адсорбции, концентрация газа с 0; б) состояние динамического равновесия между адсорбцией и десорбцией, концентрация газа в газовой фазе с; Dх – толщина адсорбционного слоя
Для твердого адсорбента обычно остается неизвестным поверхностное натяжение sт-г и толщина поверхностного слоя (Dх), в котором концентрируется адсорбат. Чтобы преодолеть возникшее затруднение в определении параметров адсорбционного слоя, поступают следующим образом. Измеряют концентрацию адсорбтивав u [л] газовой фазы до (с 0) и после (с) контакта газа с адсорбентом, когда наступит динамическое равновесие. Разность концентраций позволяет определить избыток адсорбата n [моль] на поверхности s [м2] адсорбента и величину адсорбции Гиббса:
сs = (с – с0),
n =(с – с0)×u [моль],
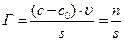 [моль/м2].
[моль/м2].
Обычно поверхность s твердого пористого адсорбента неизвестна. В этом случае экспериментальную величину адсорбции Гиббса рассчитывают в моль на грамм адсорбента: Г [моль/г].
Физико-химический процесс адсорбции можно представить уравнением:
Ац + Ад ⇄ Ац×Ад,
где Ац – активные центры на поверхности, Ад – адсорбтив в объеме газовой фазы, Ац×Ад – адсорбционные центры, занятые адсорбатом.
Константа равновесия адсорбции выражается уравнением:
К = [Ац×Ад]/[Ац]×[Ад],
где К – константа равновесия, [Ад] = с моль/м3 – концентрация адсорбтива в объеме газовой фазы, [Ац×Ад] = a моль/м2 – концентрация активных центров, занятая адсорбатом, [Ац] =(a0 – a) моль/м2 – концентрация свободных активных центров на поверхности адсорбента, a0 моль/м2 – максимальная концентрация активных центров адсорбента, которые могут быть заполнены адсорбатом.
Воспользовавшись введенными обозначениями, получим выражение константы равновесия для адсорбционного процесса на поверхности:
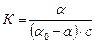 ,
,
или
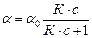 (адсорбционное уравнение Ленгмюра) (2.16)
(адсорбционное уравнение Ленгмюра) (2.16)
Уравнение Ленгмюра может быть представлено в ином виде. В нем концентрация активных центров, занятая адсорбатом, выражена через давление газа:
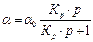 , (2.17)
, (2.17)
где Кр = К / RT.
Анализ уравнения Ленгмюра показывает, что при низких давлениях (концентрациях) газа произведением Кр×р по сравнению с единицей можно пренебречь (Кр×р << 1), тогда уравнение (2.17) примет вид:
a = a0 ×Крр.
В соответствии с этим уравнением наблюдается линейное нарастание количества адсорбированного вещества при увеличении давления газа.
При высоких давлениях (Кр×р >> 1) достигается практически полное заполнение активных центров адсорбента. Количество адсорбированного вещества перестает зависеть от давления. Уравнение (2.17) принимает вид:
a = a0
Взаимодействие адсорбтива с активными центрами адсорбента является обратимым процессом при соблюдении следующих условий:
1) на каждом адсорбционном центре может располагаться только одна молекула адсорбата, поэтому поверхность адсорбента покрывается мономолекулярным слоем адсорбата.
2) адсорбированные молекулы не взаимодействуют друг с другом.
Типичная изотерма адсорбции Ленгмюра представлена на рис. 16.

Рис. 16. Изотерма адсорбции Ленгмюра
 2015-07-03
2015-07-03 3510
3510
