Основы термодинамики адсорбции созданы американским физиком-теоретиком Дж. Гиббсом.
Рассмотрим равновесную двухфазную систему водный раствор поверхностно-активного вещества – воздух. Поверхностно-активное вещество (ПАВ) – химическое соединение, структура которого включает неполярную углеводородную цепь, например СН3(СН2)nСН2-, соединенную с полярной группой, например такой, как -[О(СН2)2]xOH (рис. 10).
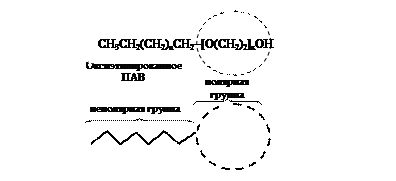
Рис. 10. Структура молекулы поверхностно-активного вещества
Молекулы воды вытесняют некоторую часть поверхностно-активного вещества на границу раздела фаз вода – воздух (газ). Полярные группы остаются в водной (полярной) среде, неполярные – в газовой фазе (неполярной среде). Так, молекулярный слой ПАВ концентрируется на границе раздела фаз.
Каждая из фаз однородна, но однородность нарушается в поверхностном слое за счет избытка количества поверхностно-активного вещества (адсорбтива), который концентрируется на границе раздела фаз, внедряясь между молекулами воды. В поверхностном слое изменяется концентрация молекул воды (она уменьшается) и молекул поверхностно-активного вещества (она увеличивается) по сравнению с водным раствором ПАВ (рис. 11).
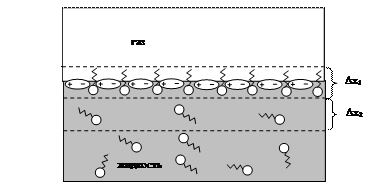
Рис. 11. Адсорбция (концентрирование) ПАВ на границе раздела фаз жидкость – газ
Внедрение неполярных углеводородных групп между молекулами воды приводит к уменьшению энергии межмолекулярного притяжения в поверхностном слое, что уменьшает поверхностное натяжение s.
Отступление. Гиббсом введена величина Г [моль/м2] (гиббсовская адсорбция), представляющая собою избыток адсорбата в объеме поверхностного слоя толщины Dх по сравнению с количеством адсорбтива в таком же объеме жидкой фазы, отнесенный к единице площади поверхности адсорбента.
Связь между гиббсовской адсорбцией Г, поверхностным натяжением s и концентрацией адсорбтива с в растворе устанавливается на основании термодинамических расчетов.
Функция Гиббса G, отражающая состояние двухфазной системы жидкий раствор – газ, зависит от температуры Т, давления р, площади поверхности раздела фаз s, а также количества адсорбата n 1 (ПАВ) и растворителя n 2:
G = f (p, T, s, n 1, n 2),
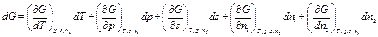 .(2.7)
.(2.7)
При постоянной температуре и давлении (р,Т = const) уравнение (2.7) примет вид:
dG = 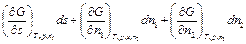 , (2.8)
, (2.8)
где  - поверхностное натяжение,
- поверхностное натяжение,
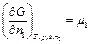 и
и 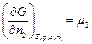 - химические потенциалы адсорбтива и воды соответственно.
- химические потенциалы адсорбтива и воды соответственно.
dG = 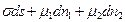 , (2.9)
, (2.9)
dG = d (s s + m 1 n 1 + m 2 n 2),
где G = s s + m 1 n 1 + m 2 n 2.
Полный дифференциал функции G:
dG = s ds + sd s + m 1 dn 1 + n 1 dm 1 + m 1 dn 1 + n 1 dm 1. (2.10)
Принимая во внимание уравнение (2.9), получим:
sd s + n 1 dm 1 + n 2 dm 2 = 0. (2.11)
Уравнение (2.11) отражает энергетическое состояние поверхностного слоя (sd s), а также количества адсорбата n 1 и растворителя n 2 в поверхностном слое.
Объемная фаза раствора не зависит от энергетического состояния поверхностного слоя и уравнение (2.11) для объемной фазы имеет вид:
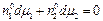 , (2.12)
, (2.12)
где 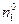 и
и 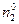 количество адсорбтива и растворителя в жидкой фазе.
количество адсорбтива и растворителя в жидкой фазе.
Из уравнения (2.12) следует
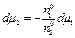 .
.
Подставим значение dm 2 в уравнение (2.11), получим:
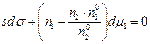
или
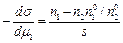 , (2.13)
, (2.13)
где 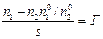 - избыток адсорбата в объеме поверхностного слоя толщиной Dх по сравнению с количеством адсорбтива в таком же объеме жидкой фазы, отнесенный к единице площади поверхности адсорбента.
- избыток адсорбата в объеме поверхностного слоя толщиной Dх по сравнению с количеством адсорбтива в таком же объеме жидкой фазы, отнесенный к единице площади поверхности адсорбента.
Из уравнения (2.13) следует:
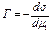 . (2.14)
. (2.14)
Для разбавленных растворов:
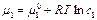 и
и 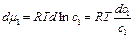 .
.
Подставляя 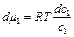 в уравнение (2.14), получим фундаментальное адсорбционное уравнение Гиббса:
в уравнение (2.14), получим фундаментальное адсорбционное уравнение Гиббса:
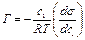 . (2.15)
. (2.15)
Графическая зависимость адсорбции Гиббса (Г – избыток адсорбата в поверхностном слое) и поверхностного натяжения s от концентрации адсорбтива представлена на рис. 12.
Прямые измерения избытка адсорбата Г [моль/м2] в поверхностном слое – трудная задача. Обычно поступают следующим образом. Экспериментально определяют зависимость поверхностного натяжения s от концентрации адсорбтива с в водном растворе и строят изотерму в координатах s от с (рис. 12). Графически определяют величины 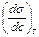 для различных значений с – концентрации ПАВ в растворе и по уравнению
для различных значений с – концентрации ПАВ в растворе и по уравнению 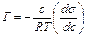 вычисляют значения избытка адсорбата Г на поверхности адсорбента.
вычисляют значения избытка адсорбата Г на поверхности адсорбента.
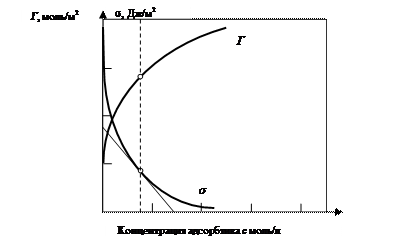
Рис. 12. Изотерма адсорбции Г и поверхностного натяжения s от концентрации адсорбтива при Т = 298 К
Среди способов экспериментального определения поверхностного натяжения s на границе жидкость – газ рассмотрим метод наибольшего давления образования пузырьков на приборе Ребиндера (рис. 13).
Поверхностное натяжение рассчитывают по формуле: 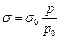 , где s - поверхностное натяжение водного раствора адсорбтива, концентрация которого с; р – давление внутри сосуда, при котором пузырек воздуха отрывается от капилляра; s0 = 71.95×10-3 Дж/м2 - табличное значение поверхностного натяжения воды; р 0 – давление внутри сосуда, при котором пузырек воздуха отрывается от капилляра в чистой воде.
, где s - поверхностное натяжение водного раствора адсорбтива, концентрация которого с; р – давление внутри сосуда, при котором пузырек воздуха отрывается от капилляра; s0 = 71.95×10-3 Дж/м2 - табличное значение поверхностного натяжения воды; р 0 – давление внутри сосуда, при котором пузырек воздуха отрывается от капилляра в чистой воде.
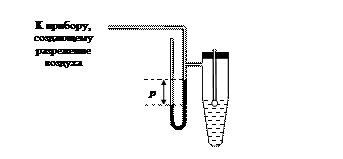
Рис. 13. Прибор Ребиндера - вакуумная пробирка с капилляром для определения поверхностного натяжения sж-г
Наряду с поверхностно-активными веществами, уменьшающими поверхностное натяжение на границе раздела фаз, существуют поверхностно-инактивные вещества, увеличивающие поверхностное натяжение. Как правило, это электролиты, соли неорганических кислот. Ионы окружены гидратными оболочками и удерживаются в объеме. Лишь незначительные количества ионов электролита проникают в поверхностный слой. Но и этого количества достаточно для увеличения поверхностного натяжения (рис. 14) на границе раздела газ – жидкость.
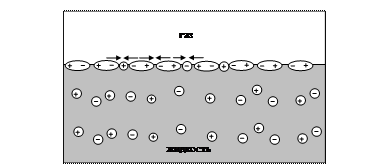
Рис. 14. Адсорбция поверхностно-инактивного вещества на границе раздела фаз жидкость – газ
 2015-07-03
2015-07-03 2009
2009
