- Все поглощают ИК-свет, спектры поглощения (плаквенил)
- Поглощают свет в УФ-области спектра –для хингамина и плаквенила – 3 максимума при 257, 329 и 343 нм.
- ВЭЖХ для плаквенила (по времени удерживания основного пика на хроматограмме СО и анализируемой субстанции).
- Реакции с общеалкалоидными осадительными реактивами на третичный атом азота (на хингамин с пикриновой кислотой, Тпл образующегося пикрата)
- Осаждение оснований из растворов солей под действием NaOH и определение Тпл основания
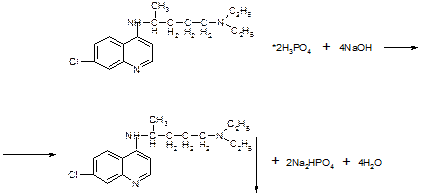
- На алкалоиды хинин и хинидин – Талейохинная проба – специфическая реакция, основанная на окислении метокси-группы хинолинового ядра у 6 атома углерода бромной или хлорной водой с образованием продуктов окисления: 5,6-ортохинолинхинона и 5,6,7-тригидроксипроизводного. При последующем добавлении аммиака эти соединения конденсируются в талейохин, который имеет изумрудно-зеленое окрашивание.
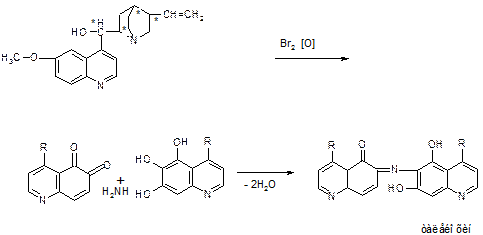
Известными неофицинальными реакциями являются эритрохинная проба и образование герепатита.
- Эритрохинная проба протекает под действием бромной воды и
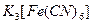 в щелочной среде на раствор хинина – появляется красное окрашивание. Реакция в 10 раз чувствительней талейохинной, но окрашивание сохраняется короткое время. Механизм реакции: окисление хинина до производного 5,8-хинолинхинона, который далее взаимодействует с непрореагировавшим хинином через 5 и 7 атомы углерода с образованием эритрохина
в щелочной среде на раствор хинина – появляется красное окрашивание. Реакция в 10 раз чувствительней талейохинной, но окрашивание сохраняется короткое время. Механизм реакции: окисление хинина до производного 5,8-хинолинхинона, который далее взаимодействует с непрореагировавшим хинином через 5 и 7 атомы углерода с образованием эритрохина

- Водные растворы хинина и хинидина в присутствии серной кислоты имеют голубую флюоресценцию в УФ-свете
- Образование герепатита – для хинина и хинидина. К горячему спиртовому раствору хинина, подкисленному
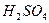 , добавляют спиртовой раствор йода, при охлаждении образуются кристаллы герепатита в виде зеленых листочков.
, добавляют спиртовой раствор йода, при охлаждении образуются кристаллы герепатита в виде зеленых листочков.
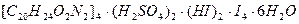
- По величине
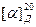 - 3% растворы в 0,1 н HCl. Хинин l-изомер, хинидин d-изомер
- 3% растворы в 0,1 н HCl. Хинин l-изомер, хинидин d-изомер - Для хингамина и плаквенила – реакции на ковалентно связанный хлор:
а) проба Бельштейна
б) минерализация: путем сжигания в колбе с кислородом или сплавления со смесью
для спекания, затем открываем ионы хлора
- Реакции на анионы кислот.
а) Хинина гидрохлорид, хинина дигидрохлорид – на ионы хлора с 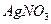 в растворе
в растворе 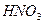
б) Хинина и хинидина сульфат и плаквенил на 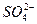
в) Хингамин на 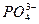 - ион с молибдатом аммония
- ион с молибдатом аммония
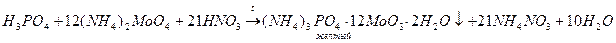
Отличить хинин от хинидина можно следующей реакцией:
Одну каплю спиртового раствора соли хинина и хинидина, подкисленного 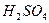 , нанести на фильтровальную бумагу и 30 сек. обрабатывать парами
, нанести на фильтровальную бумагу и 30 сек. обрабатывать парами 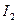 , хинин дает серовато-синее пятно с темно желтым ободком, а хинидин – темно-желтое пятно.
, хинин дает серовато-синее пятно с темно желтым ободком, а хинидин – темно-желтое пятно.
Примеси:
Плаквенил – метод ТСХ в сочетании с УФ-спектрофотометрией при 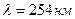 определяются – посторонние примеси (сумма примесей не более 1%)
определяются – посторонние примеси (сумма примесей не более 1%)
- Для солей хинина по ФС – гравиметрия. Из водного раствора соли осаждают основание раствором NaOH, осадок извлекается
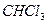 , хлороформ отгоняют, осадок взвешивают и вес осадка умножают на
, хлороформ отгоняют, осадок взвешивают и вес осадка умножают на 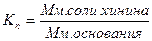 , и определяют соответственно содержание определенных веществ во взятой навеске.
, и определяют соответственно содержание определенных веществ во взятой навеске. - Кислотно-основное титрование в неводных средах по МФ в среде ледяной
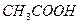 с добавлением
с добавлением 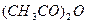
1) для гидрохлоридов в присутствии 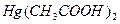 Э=М/2
Э=М/2
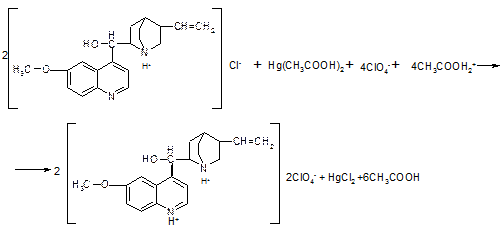
2) Э=М/2
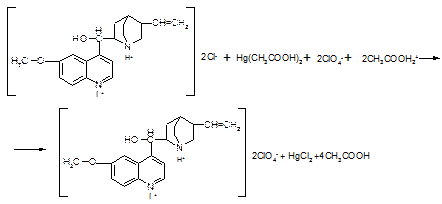
3) для сульфатов хинина и хинидина. Э=М/3
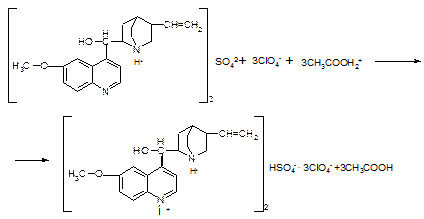
для плаквенила. Э=М.м.
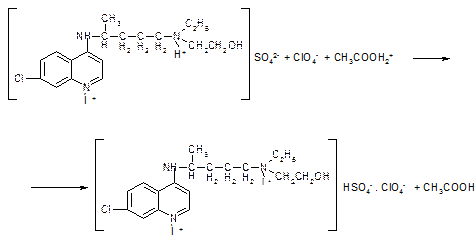
4) для хингамина в среде 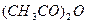 и
и 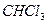 .Э=М/2
.Э=М/2
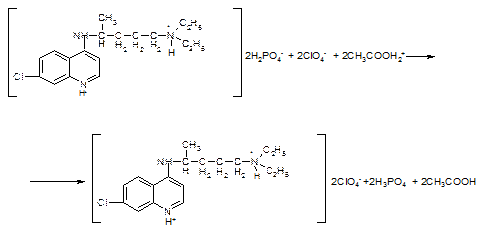
- Алкалиметрия. Титрант 0,1 н. NaOH, индикатор ф/ф в присутствии спирто-хлорофомной смеси. Для гидрохлоридов Э=М.м., дигидрохлоридов Э=М/2, для сульфатов Э=М/2, для хингамина:
1. 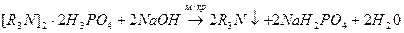 Э=М/2
Э=М/2
2. 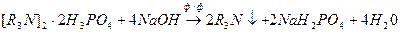 Э=М/4
Э=М/4
- Для хинина гидрохлорида и дигидрохлорида – аргентометрия: метод Фаянса, Фольгарда, меркуриметрия.
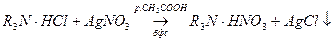
Э=М.м – гидрохлоридов Э=М/2-дигидрохлоридов
1) ВЭЖХ (плаквенил), ТСХ (для лекарственных форм).
1) УФ-спектрофотометрия, флюориметрия (для солей хинина)
1) Для хингамина и плаквенила – меркуриметрия, после сжигание в колбе с кислородом. Э=М.м
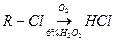
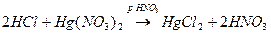
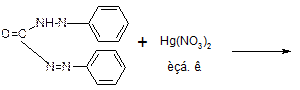
 2015-07-14
2015-07-14 15894
15894
