Продуктом окислительной, нейтральной или даже восстановительной плавки сульфидных, медных, полиметаллических, медно-никелевых руд и концентратов, а также и восстановительно-сульфидирующей плавки окисленных никелевых руд являются штейны, которые в основе своей состоят из сульфидов железа и цветных металлов. В зависимости от типа плавки, в штейне может содержаться определенное количество магнетита (Fe3O4) или свободных металлов (главным образом Fe, Ni, в меньшем количестве Cu).
Обычная классификация штейнов такова:
1. Медные: состоят из FeS, Cu2S, и содержат тем больше магнетита, чем штейн «беднее» (по меди), т.е. содержат больше FeS.
2. Медно-никелевые: состоят из FeS, Cu2S, Ni3S2, CoS и в качестве обязательного компонента содержат либо Fe3O4, либо свободные Fe и Ni – в зависимости от типа плавки (окислительная или восстановительная).
3. Никелевые: состоят из FeS, Ni3S2, CoS и в значительной мере металлического Fe и Ni (до 30-35%).
4. Полиметаллические: FeS, Cu2S, ZnS, PbS и Fe3O4.
Мировая металлургическая практика для переработки штейнов использует главным образом конвертерный процесс, заключающийся в продувке расплавленного штейна воздухом. При продувке штейна в конвертере сжатым воздухом в зоне непосредственно контакта струи и расплава (дутьевая зона) происходит интенсивное окисление сульфидов и металлов кислородом:
FeS + 1,5O2 = FeO + SO2, а также 3FeS + 5O2 = Fe3O4 + 3SO2
МeS + 1,5O2 = МeO + SO2
2Fe + O2 = 2FeO, а также 3Fe + 2O2 = Fe3O4
2Мe + O2 = 2МeO
Поскольку количество FeS в расплавленной ванне в штейнах обычного состава существенно преобладает над количеством сульфидов металлов, в той части ванны, которая находиться за пределами «дутьевой зоны», имеется избыток FeS. В этой части ванны происходят термодинамически обусловленные реакции обменного взаимодействия типа МeO + FeS = МeS + FeO, т.е. оксиды цветных металлов «отнимают» серу у железа и возвращают в сульфидную форму. В такой последовательности протекают реакции конвертирования, пока железо и его сульфид практически полностью не будут переведены в форму оксидов. Цветные же металлы остаются в основном в форме сульфидов. Следовательно, с некоторым упрощением, совокупность реакций окисления и обменного взаимодействия может быть сведена в итоге к реакциям окисления железа и его сульфида:
FeS + aи× 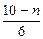
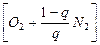 = nFeO +
= nFeO + 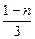 Fe3O4 + SO2 +
Fe3O4 + SO2 + 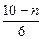
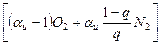 (1)
(1)
Fe+aи× 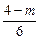
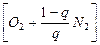 =
=
mFeO+ 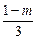 Fe3O4 +
Fe3O4 + 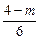
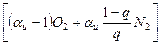 (2)
(2)
где aи и q – коэффициенты избытка дутья и степень обогащения дутья кислородом соответственно; n и m – коэффициенты, отвечающие факту наличия в конвертерных шлаках вюстита FeO и магнетита Fe3O4.
 2015-08-21
2015-08-21 344
344








