Ионы металлов имеют ряд преимуществ перед протоном. Больший заряд ионов металлов позволяет им связываться не с одним, а с двумя и более донорными атомами молекул реагента и тем самым обеспечивать более высокую степень их поляризации. Кроме того, каталитические функции ионов металлов сохраняются в средах с очень низкой концентрацией протонов. Еще одно их преимущество состоит в специфичности действия, обусловленной особенностями электронной конфигурации, лигандным составом и структурой координационной сферы. Особенности поведения ионов металлов явились основой для разработки нового класса гомогенных катализаторов – растворимых в реакционных средах соединений переходных металлов.
Основная группа таких металлов имеет частично заполненные d -орбитали. Эти орбитали выходят за периферию атомов или ионов, что способствует образованию связей различной симметрии между металлом и его окружением. Среди них наиболее интересны соединения металлов, растворимые в органических средах (комплексные соединения и соли).
Группу очень активных металлокомплексных катализаторов составляют так называемые кластеры. Понятие «кластер» связывают с молекулярными системами разных уровней организации: ассоциатами или комплексами молекул, ассоциатами атомов металлов или благородных газов, фрагментами больших молекул или кристаллов. Особый интерес представляют соединения, в которых присутствуют одна или несколько связей типа металл-металл. Чаще всего такие кластеры металлов находятся в конфигурациях М 3 (треугольный) (рисунок 7.2) или М 6 (октаэдрический) (рисунок 7.3).
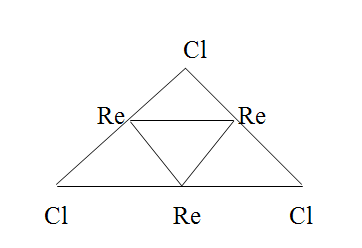 Рис. 7.2. Структура кластера Re3Cl3 Рис. 7.2. Структура кластера Re3Cl3 | 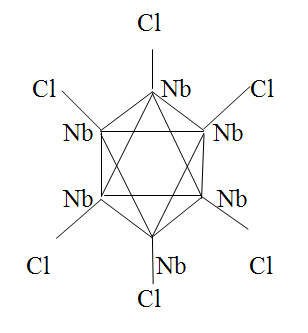 Рис. 7.3. Структура кластера Nb6Cl6 Рис. 7.3. Структура кластера Nb6Cl6 |
Высокая каталитическая активность кластеров обусловлена прежде всего многоточечным контактом атомов металла с молекулой субстрата и закреплением последнего в наиболее благоприятной для реакции конформации, а также возможностью координации нескольких молекул двумя соседними металлическими центрами и осуществления многоэлектронных реакций, благодаря высокой проводимости металлической связи. По этим причинам кластеры проявляют во многих химических реакциях уникальные каталитические свойства, несвойственные одноядерным частицам. Например, в присутствии кластера Ni4[CNC(CH3)3]7 циклизация ацетилена в бензол и бутадиена в циклооктадиен протекает при комнатной температуре.
Особый интерес в катализе представляют гетероядерные кластеры. Так хорошо известную реакцию гидроформилирования этилена (7.17):
С2Н4 + СО + Н2 ® СН3СН2СНО (7.17)
проводят при 100 – 1800С и давлении 100 – 300 МПа в присутствии многоядерных комплексов кобальта НСо(СО)4. Проведение этого процесса на закрепленном гетероядерном кластере Со2(СО)6[Pd(PPh)3]2 позволяет получать этот продукт при 400С.
Наибольшие успехи при использовании металлокомплексных катализаторов были достигнуты в различных превращениях олефиновых углеводородов. Реакции гидрирования, олигомеризации, димеризации, гидроформилирования, карбонилирования, гидрокарбоксилирования и другие в присутствии гомогенных соединений переходных металлов протекают, как правило, при комнатной температуре с высокой скоростью и селективностью.
При разработке технологии гомогенно-каталитической реакции часто предпочтение отдают не отдельному катализатору, а каталитической системе, включающей собственно катализатор и один или несколько активаторов. Активатором называют вещество с собственной каталитической активностью или без нее, добавка которого в небольшом количестве к основному катализатору существенно повышает его активность.
Применение активаторов в гомогенном катализе позволяет снизить себестоимость продукции за счет увеличения скорости и селективности процесса, уменьшения давления и температуры синтеза.
 2015-08-21
2015-08-21 2826
2826
