Лабораторная работа № 4.
Цель работы: Изучить электродные процессы при электролизе растворов.
Общие сведения.
Окислительно-восстановительная реакция, протекающая в растворе или расплаве электролита у электродов при пропускании постоянного электрического тока, называется электролизом.


Ход работы:
Электролизный стакан.
2. Анод
3. Катод
Уравнение электролизного раствора CuSO4 с медным анодом.
A(+): Cu 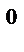 - 2e→Cu
- 2e→Cu 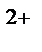
K(-): Cu 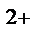 + 2e→Cu
+ 2e→Cu 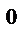 ↓ (масса катода увеличивается)
↓ (масса катода увеличивается)
m(г)- масса катода до элетролиза
mτ(г)- масса катода после электролиза
Закон Фарадея
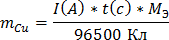
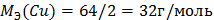
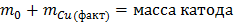
Выход по току 100% (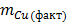 )
)
| I(A) | t(c) | Масса катода (Cu) | Масса катода (Cu) | mт (теор.) | mτ- mo (факт.) | η(Сu)% |
| mo | mт | |||||
| 2,5 | 35,99 | 0,99 | 0,99 | 100% |

Выход по току 100% - 1
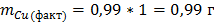
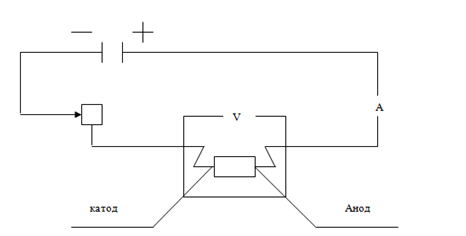
Схема процесса электролиза.
Вывод: Я изучил электродные процессы при электролизе растворов
КОНТРОЛЬНЫЕ ВОПРОСЫ.
1. В каких случаях образуются вторичные продукты при электролизе?
Ответ: Вторичные продукты при электролизе образуются в случае, если анод активный.
2. В какой последовательности и выделяются на катоде металлы при электролизе раствора, содержащего ионы Ni2+, Cr2+,Fe3+?
Ответ: Cr2+, Fe3+, Ni2+
3. Какой силы должен быть ток, чтобы при пропускании его через расплав MgSO4 выделить на катоде 6 г. магния за 10 часов?
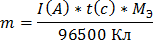
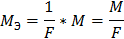
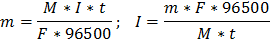
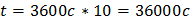
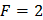
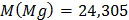
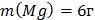
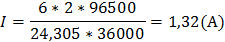
4. Через последовательно соединенные электролитические ванны с платиновыми электродами пропустили ток. В первой ванне раствор сульфата натрия, во второй - раствор нитрата серебра, а в третьей - раствор соляной кислоты. Какие продукты выделились на электродах во всех трех ваннах и сколько их получилось по массе, если в первой ванне выделится на катоде 1 мг. водорода?
K1: 2H2O + 2e = H2 + 2OH-
A1: 2H2O - 4e = O2 + 4H+
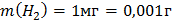
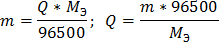
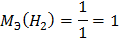
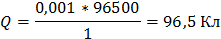
K2: Ag+ + e = Ag0
A2: 2H2O - 4e = O2 + 4H+
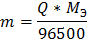
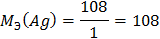
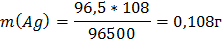
K3: 2H+ + 2e = H20
A3: 2Cl- - 2e = Cl20
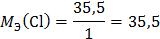
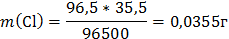
5. Через водный раствор NaCl (электроды угольные) пропускали ток сначала при перемешивании раствора, а затем без перемешивания, отделив в последнем вторичные продукты. Написать уравнения электродных процессов для двух случаев.
Решение для 1 случая.
К: 2H2O + 2e = H2 + 2OH
А: 2Cl - 2e = Cl2
Суммарное ионное ур-ие:
2H2O + 2Cl = H2 + Cl2 + 2OH
Суммарное молекулярное ур-ие:
2H2O + 2NaCl = H2 + Cl2 + 2NaOH
Решение для 2 случая.
K1: 2H2O + 2e = H2 + 2OH-
A1: 2H2O - 4e = O2 + 4H+
K2: Ag+ + 1e = Ag0
A2: 2H2O - 4e = O2 + 4H+
K3: 2H+ + 2e = H20
A3: 2Cl- - 2e = Cl20
 2015-08-13
2015-08-13 9924
9924