4. Выражение для произведения растворимости Sr3(AsO4)2 – это...
Решение.
[Sr2+]3[AsO 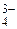 ]2.
]2.
| 5. | Формула соли | ... | ... | ... |
| ПР, (моль/л) z | ... | ... | ... |
Формулы солей, расположенные в порядке увеличения/уменьшения их растворимости (в моль/л) – это...
Решение.
Надо расположить соли в порядке увеличения/уменьшения их ПР.
Пример.
| 5. | Формула соли | AgCN | AgNCS | AgNO2 |
| ПР, (моль/л)2 | 7·10–15 | 2·10–12 | 3·10–10 |
Формулы солей, расположенные в порядке уменьшения их растворимости (в моль/л) – это...
Решение.
ПР(AgCN) < ПР(AgNCS) < ПР(AgNO2), значит, порядку уменьшения растворимости соответствует AgNO2, AgNCS, AgCN.
ОВР
ПРАВИЛА ОПРЕДЕЛЕНИЯ СТЕПЕНЕЙ ОКИСЛЕНИЯ.
1. В простых веществах степени окисления равны нулю, например Сu0, S 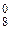 .
.
2. Некоторые элементы в сложных веществах и в ионах имеют, как правило, постоянные степени окисления, в частности:
а) у элементов IA-группы, II группы (кроме Hg) и III группы (кроме B и Tl) периодической системы степень окисления равна номеру группы со знаком «+», например K+1NO3, Be+2SO4, Al+3F3;
б) у водорода степень окисления равна +1, кроме соединений с элементами, перечисленными в п. а), а также с B и с Si, в которых степень окисления водорода составляет –1, например H+1Br, но B2H 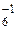 ;
;
в) у кислорода степень окисления равна –2, кроме пероксидов, надпероксидов, озонидов и соединений со фтором, например CCl2O-2, H2O 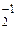 (пероксид водорода), KO
(пероксид водорода), KO 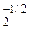 (надпероксид калия), RbO
(надпероксид калия), RbO 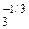 (озонид рубидия), O
(озонид рубидия), O 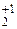 F2 (дифторид дикислорода);
F2 (дифторид дикислорода);
г) у элементов VIIA-группы периодической системы степень окисления равна –1, причем у фтора всегда, а у остальных галогенов, кроме соединений со фтором, кислородом, азотом и между собой, например, H[РF 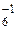 ], BCl
], BCl 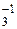 , Br
, Br 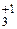 N;
N;
3. У элементов кислотных остатков в солях степени окисления такие же, как в кислотах, например, в хлоридах MCl x – степень окисления хлора –1, Cl–1; в сульфатах M a (SO4) b – степень окисления серы +6, S+6; в нитратах M(NO3) x – степень окисления азота +5, N+5.
4. Сумма степеней окисления всех атомных частиц в молекуле (или в формульной единице вещества немолекулярного строения) равна нулю, а в ионе – заряду этого иона.
 2015-08-13
2015-08-13 625
625








