1. Записати сталу приладу А, яка є в паспорті установки. Виміряти за показами термометра і барометра кімнатну температуру Т = (... ±...) К й атмосферний тиск P = (...±...) Н/м2. Увімкнути живлення секун-доміра 7.
2. Мірну склянку 9 поставити під кран 8. Обережно відкрутити кран, щоб вода з посудини 1 повільно виливалась у мірну склянку.
3. Стежити за показами манометра 6. Коли різниця рівнів води h в колінах манометра перестане змінюватись, виміряти її та ввімкнути відлік часу t за секундоміром 7, одночасно зафіксувавши на лінійці 2 висоту H 1 рівня води в посудині 1.
4. Після того, як рівень води в посудині 1 опуститься на 3–5 см, припинити відлік часу й одночасно зафіксувати на лінійці 2 висоту Н 2 рівня води в посудині 1.
5. Результати вимірювань h, t, Н 1 і Н 2 записати в таблицю:
| Номер за пор. | h, м | D h, м | t, с | D t, с | H 1, м | D H 1, м | H 2, м | D H 2, м |
| …. | ||||||||
| С.з. |
6. Повторити експеримент згідно з пунктами 1–5 ще двічі. Результати вимірювань усереднити.
7. За середніми значеннями виміряних експериментально величин обчислити згідно з формулами (8) і (11) ` l і de.
8. Абсолютні похибки D l і D de обчислити за формулами
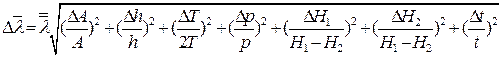 ;
;
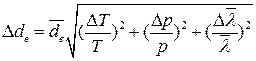 .
.
9. Записати кінцевий результат експерименту у вигляді
l = (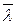 ±D
±D 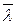 ) м, El = … %;
) м, El = … %;
de = (de ±D de) м, Ede = … %.
Контрольні запитання
1. Сформулюйте головні положення молекулярно-кінетичної теорії газів.
2. Що називають довжиною вільного пробігу молекул? Від чого вона залежить?
3. Дайте означення ефективного діаметра молекули газу. Запишіть і поясніть формулу залежності між ` l і de.
4. Запишіть одне з рівнянь МКТ, яке пов’язує макро- і мікропараметри газу.
5. Порівняйте між собою середню, середню квадратичну та найімовірнішу швидкості молекул газу. Як їх визначають?
6. Запишіть і поясніть формулу Пуазейля.
7. Як змінюється в’язкість газу зі зміною температури?
Лабораторна робота № 212 ВИЗНАЧЕННЯ СПІВВІДНОШЕННЯ ТЕПЛОЄМНОСТЕЙ ПОВІТРЯ СP/СV МЕТОДОМ КЛЕМАНА–ДЕЗОРМА
Завдання: експериментально визначити співвідношення теплоєм-ностей повітря за сталого тиску і сталого об’єму СP /СV.
Приладдя: установка для визначення співвідношення теплоємностей повітря.
Теоретичний матеріал, який необхідно засвоїти під час підготовки до виконання роботи: ізопроцеси в ідеальному газі; адіабатичний процес; рівняння Пуассона; внутрішня енергія ідеального газу; теплоємність, питома та молярна теплоємності; теплоємність за сталого тиску і сталого об’єму; рівняння Майєра; ступені вільності молекул; визначення СP /СV через ступені вільності молекул.
Література:
1) § 16.2–16.5, с. 285–304;
2) § 18.6–18.8, c. 68–74;
3) § 45–46, с. 104–146; § 71–72, с. 223–232;
4) § 41, с. 73–75; § 50–51, с.88–90; § 53,55, с. 94–96.
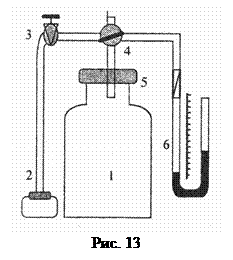
Опис установки. Експериментальна установка (рис. 13) складається зі скляної посудини 1, герметично закритої корком 5. Через корок проходить скляна трубка з двоходовим краном 4. Кран 4 може з’єднувати посудину 1 з атмосферою або ж із помпою 2, якщо кран 3 відкритий. У першому випадку тиск повітря в балоні дорівнює атмосферному, а різниця рівнів рідини у манометрі 6 – нулю. Якщо кран 4 повернути в інше положення і помпою 2 нагнітати повітря в балон, то тиск у ньому збільшиться на D р = rgh, де r – густина, а h – різниця рівнів рідини в манометрі 6.
Ідея роботи та виведення робочої формули. В цій роботі досліджують процес адіабатичного розширення газу, який описує рівняння Пуассона
PVg = const або P 1- g Tg = const, (1)
де g = СP / СV – показник адіабати.
Очевидне таке: якщо зв’язок між параметрами двох станів газу Р і Т відомий, то з (1) можна отримати вираз для розрахунку СP / СV. У цій роботі досліджуваним газом є повітря, яке міститься в балоні. Після нагнітання в балон повітря його рівноважний стан визначатимуть такі параметри: V, Т 1 і P 1, де V – об’єм балона; Т 1– кімнатна температура, а
Р 1= Р 0+ rgh 1. (2)
Тут P 0 – атмосферний тиск; h 1 – різниця рівнів рідини в манометрі.
Переведемо повітря в балоні в інший стан, з’єднавши за допомогою крана 4 об’єм балона на короткий проміжок часу з атмосферою. Внаслідок адіабатичного розширення частина повітря вийде з балона. Тиск у балоні буде дорівнювати P 0, а температура знизиться до Т 2. Цей процес описує рівняння (1), а саме:
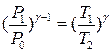 . (3)
. (3)
Після закриття крана 4 повітря в балоні з часом знову нагріється до кімнатної температури Т 1, а тиск у балоні
Р 2= Р 0+ rgh 2. (4)
Зазначимо, що цей процес є ізохорним, оскільки об’єм повітря в балоні не змінюється, а тому
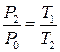 . (5)
. (5)
Параметри T 1 і P 2 визначають третій стан газу.
Підставимо (5) у (3), отримаємо
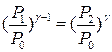 . (6)
. (6)
Прологарифмуємо рівняння (6) і розв’яжемо його щодо g:
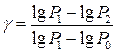 , (7)
, (7)
або, використавши (2) і (4),
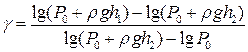 . (8)
. (8)
Розкладемо логарифми в ряд Тейлора і, обмежившись двома першими членами, матимемо
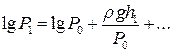 i
i 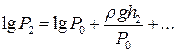
Підставимо отримані вирази в рівняння (8) і отримаємо
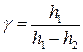 . (9)
. (9)
Формула (9) є робочою формулою цієї лабораторної роботи.
 2015-08-21
2015-08-21 344
344








