1. Нарисуйте орбитальные картины для молекул пиридина, фурана, пиррола, и тиофена.
2. Свободная электронная пара атома азота в пирроле находится на орбитали
A) sp2 орбитали
B) sp3 орбитали
C) p орбитали
D) sp орбитали
3. Предложите объяснение наблюдающейся основности пиррола (рКа -4.4), пиридина (рКа 5.29) и пирролидин (рКа 11.31).
4. Получите 2,5-диметилфуран (А) из этилацетата и других необходимых реагентов.
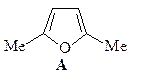
5. Из ацетоуксусного эфира, пинаколина и других необходимых реагентов получите 2-метил-5- трет -бутилфуран (А).
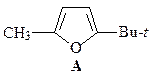
6. Из циклогексанона, пирролидина, бромацетона и других необходимых реагентов получите замещенный фуран А.
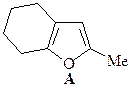
7. Получите 1-метил-2,5-дифенилпиррол (А) из метиламина, этилбензоата, этилацетата и других необходимых реагентов.
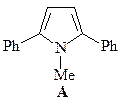
8. Синтезируйте соединение А, исходя из адипиновой кислоты, бромацетона и метиламина.
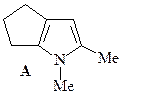
9. Получите гетероцикл А из пиридина, ацетилена, ацетальдегида и других необходимых неароматических реагентов.
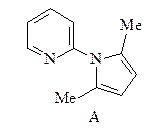
10. Исходя из ацетофенона и диэтилового эфира адипиновой кислоты осуществите синтез соединения А.
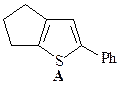
11. Реакции электрофильного замещения для фурана, пиррола и тиофена проходят преимущественно в положение С-2, а если это положение занято, то в положение С-5. Объясните этот факт. Нарисуйте резонансные структуры для промежуточного s-комплекса, который образуется при атаке в положения С-2 (С-5) и С-3 (С-4). Приведите основной продукт и объясните причину его образования.
12. Приведите условия приведенных ниже реакций.
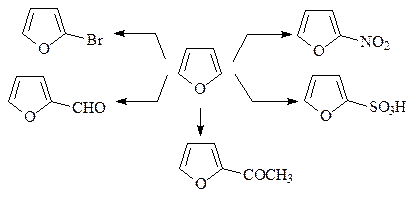
13. Из фурана и других необходимых реагентов синтезируйте фурфуриловый спирт.
14. Приведите структуру соединения А, получающегося в результате следующей реакции.
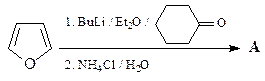
15. В нижеприведенной схеме укажите структуры соединений А - В.
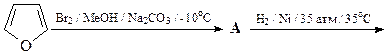
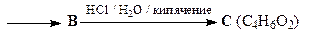
16. Приведите строение соединения А, которое образуется при обработке 2,5-диметилфурана одним эквивалентом диметилового эфира ацетилендикарбоновой кислоты.
17. Напишите структуру продукта А нижеприведенной реакции.
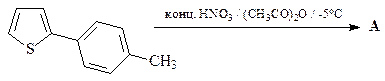
18. Предложите два метода синтеза 5-этилтиофен-2-карбоновой кислот, исходя из тиофена и других необходимых реагентов.
19. Исходя из метилфурана и других необходимых реагентов, получите, используя реакцию Юрьева, 1,2-диметилпиррол. Напишите структуру продукта реакции монобромирования 1,2-диметилпиррола под действием диоксандибромида.
20. Предложите схему синтеза a-фурил-a-тиенилкетона, исходя из тиофена, фурфурола и других необходимых реагентов.
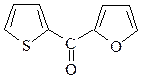
21. Расшифруйте цепочку превращений,
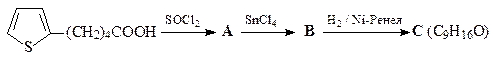
22. Исходя из формальдегида и ацетоуксусного эфира, получите 2,6-диметилпиридин А, используя синтез пиридинов по Ганчу.
23. Синтезируйте 3-бензоилпиридин, исходя из пиридина.
24. Укажите условия превращения пиридина: а) в 3-нитропиридин; б) в 3-бромпиридин.
25. Нарисуйте структуры интермедиатов, образующихся в электрофильных атаках по положениям С-2, С-3 и С-4 кольца пиридина и объясните, почему замещение по положению С-3 является преобладающим.
26. Напишите схемы превращения а) пиридина в 2-аминопиридин под действием амида натрия в жидком аммиаке и б) 4-хлорпиридина в 4-метоксипиридин при обработке метилатом натрия в метиловом спирте; сравните эту реакцию с взаимодействием 4-нитрохлорбензола с нуклеофильными реагентами.
27. Приведите механизм превращения 2-хлорпиридина в 2-метоксипиридин.
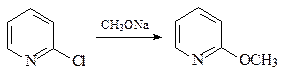
28. Укажите структуры соединений A - Е в приведенной ниже схеме.
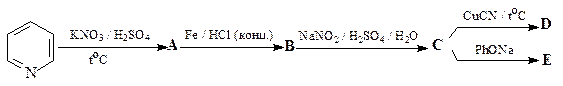
29. Расшифруйте приведенную ниже цепочку превращений.
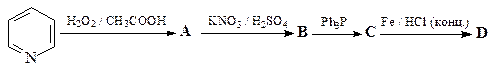
30. Приведите структуры соединений А и В в приведенной последовательности превращений.
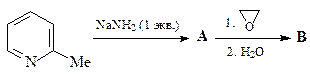
31. Расшифруйте приведенную ниже схему.
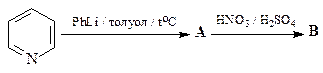
32. Исходя из пиридина осуществите синтез 2,5-дибромпиридина. Какой продукт получится при обработке этого соединения раствором одного эквивалента метилата натрия в метаноле?
33 Обработка 4-бромпиридина NaNH2 / жидк. NH3 дает два изомерных соединения А и В с брутто-формулой C5Н6N2, а реакция с MeONa / MeOH приводит только к одному продукту – С ( C6Н7NO) Приведите структуры соединений А, В и С и схемы их образования.
34. Получите 2- и 4-бромпиридины, исходя из пиридина.
35.Исходя из пиридина и других необходимых реагентов, получите соединения пиридинового ряда A и В.
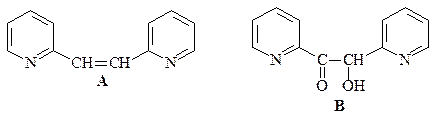
36. Получите 3-пиридинкарбоновую (никотиновую) кислоту А двумя способами: исходя из пиридина и исходя из хинолина.
37. Какой a,b-непредельный кетон нужно ввести в реакцию с анилином (синтез Дебнера-Миллера), для того, чтобы получить 4-фенилхинолин?
38. Расшифруйте схему приведенной ниже реакции.
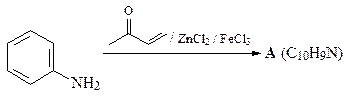
39. Приведите структуру соединения А в приведенной ниже схеме.
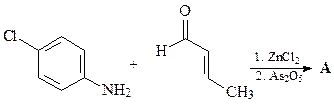
40. Синтезируйте 6-бромхинолин (А) из анилина и глицерина.
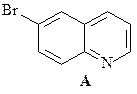
41.Из о -броманилина, гептандиаля и других необходимых реагентов получите замещенный хинолин А.
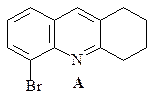
42. Приведите реагенты и условия реакций, необходимые для осуществления приведенного ниже превращения.
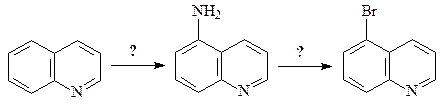
43. Сопоставьте свойства бензольного и пиридинового колец в хинолине. Напишите соответствующие уравнения реакций.
44. Получите 4-гидрокси-2-метилиндол (Е), исходя из 3-гидразинофенола и ацетона.
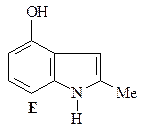
45. Имея в своем распоряжении 3-ацетилпиридин и пара -анизидин (пара -метоксианилин) получите соединение А.
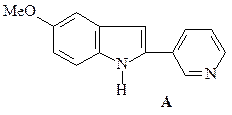
46. Приведите структуру продукта сульфирования индола (А) и механизм его образования.
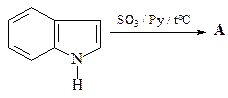
47. Исходя из фенилгидразина и любых других необходимых реагентов, получите 2- и 3-индолкарбоновые кислоты.
48. Синтезируйте, исходя из ацетофенона, п -анизидина (п -метоксианилина) и других необходимых реагентов, 5-метокси-2-фенилиндол (А).
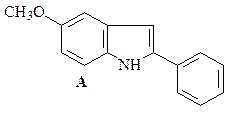
Какой продукт получится в результате обработки индола А Me2NCHO/POCl3 и последующего гидролиза реакционной смеси водным ацетатом натрия?
49. Какие продукты образуются в результате каждой из приведенных ниже реакций?
1. 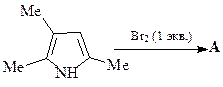 | 2. 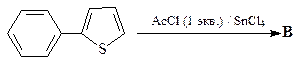 |
3. 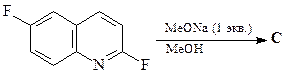 | 4. 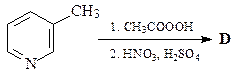 |
5. 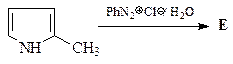 | 6. 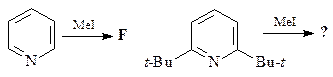 |
 2015-08-21
2015-08-21 969
969






