Ароматические амины, обладая основными свойствами, реагируют с сильными кислотами, образуя соли аминов:
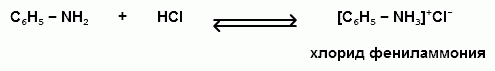
Соли аминов называют заменяя слово –амин на –аммоний, и перед названием указывают название аниона (хлорид, сульфат, нитрат).
Под действием более сильных оснований ароматические амины вытесняются из их солей:
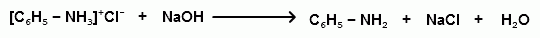
Ароматические амины имеют менее выраженный основный характер, чем алифатические. Уменьшение основности анилина по сравнению с алифатическими аминами объясняется взаимодействием неподеленной пары электронов азота с электронами ароматического ядра - их сопряжением. Сопряжение уменьшает способность неподеленной электронной пары присоединять протон.
Расположив амины по мере снижения основности, получим следующий ряд:
Alk-NH2 > NH3 > C6H5N(Alk)2 > C6H5NHAlk > C6H5NH2 > (C6H5)2NH > (C6H5)3N
Таким образом, алкилирование аминогруппы в ароматических аминах увеличивает основность, а введение в молекулу второго или третьего ароматического кольца приводит к ослаблению основных свойств (трифениламин почти совсем не обладает основными свойствами).
Введение в ароматическое кольцо различных заместителей оказывает значительное влияние на основные свойства ароматических аминов.
Электроноакцепторные заместители (-NO2, –CN, –COOH) усиливают сопряжение атома азота с бензольным кольцом и уменьшают основные свойства аминов.
Электронодонорные заместители (Alk, -OCH3) приводят к увеличению электронной плотности на атоме азота и, следовательно, к усилению основных свойств.
2) Кислотные свойства
Кислотные свойства у ароматических аминов выражены сильнее, чем у алифатических. Это связано со снижением электронной плотности на атоме азота за счет р,π-сопряжения, приводящего к увеличению поляризации связи N-H.
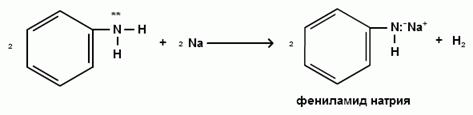
Однако, кислотные свойства ароматических аминов очень слабы, и водород может замещаться лишь при действии щелочных металлов и амидов:
 2015-08-21
2015-08-21 8194
8194
