В молекуле анилина за счет большей ЭО атома азота электронная плотность по системе σ-связей смещена в сторону гетероатома, т.е. имеет место –I –эффект. Однако ЭО азота (3,0) ненамного превышает ЭО атома углерода в sp2-гибриди-зации (2,8). Поэтому –I –эффект атома азота небольшой.
Свободная электронная пара атома азота в молекуле анилина находится в сопряжении с π-электронами бензольного кольца, т.е. имеет место +М-эффект (р-π-сопряжение). При этом +М-эффект довольно большой, что связано с близкими значениями атомных радиусов атомов азота и углерода и эффективным перекрыванием электронных облаков этих атомов.
Таким образом, положительный мезомерный эффект будет в значительной степени преобладать над отрицательным индуктивным эффектом: +М > -I
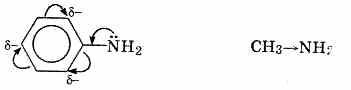
Электронное строение анилина можно представить в виде следующих граничных (или резонансных) структур:

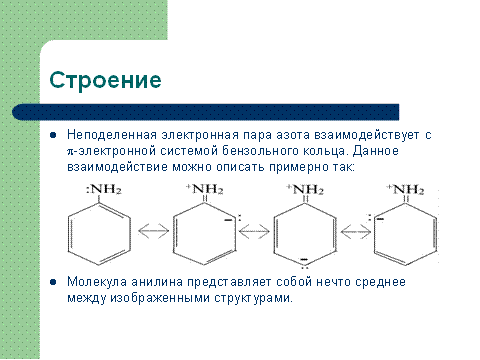
Эти структурные формулы показывают, что:
1) электронная пара азота втягивается в бензолное кольцо, при этом на атоме азота появляется частичный положительный заряд (δ+) и основные свойства аминогруппы уменьшаются.
2) в бензольном кольце, напротив, электронная плотность увеличивается, причем наиболее сильно в орто- и пара-положениях по отношению к аминогруппе. Поэтому атака электрофильных реагентов происходит в орто- и пара-положения. Аминогруппа является ориентантом 1 рода.
 2015-08-21
2015-08-21 1582
1582
