1. Определение порога коагуляции золя.
1.1. В 10 пробирок налить золь, воду и электролит в следующих объемах:
Таблица 1
| № пробирки | ||||||||||
| Объем золя, мл | ||||||||||
| Объем воды, мл | 10,0 | 9,0 | 8,5 | 8,0 | 7,5 | 7,0 | 6,5 | 6,0 | 5,5 | 5,0 |
| Объем электролита Vэл, мл | 1,0 | 1,5 | 2,0 | 2,5 | 3,0 | 3,5 | 4,0 | 4,5 | 5,0 | |
| Оптическая плотность, D |
Электролит вводят в каждую пробу золя за 2-4 мин непосредственно перед измерением ее оптической плотности.
 1.2. Измерить оптическую плотность золя в каждой колбе с помощью фотоэлектроколориметра, полученные данные записать в таблицу.
1.2. Измерить оптическую плотность золя в каждой колбе с помощью фотоэлектроколориметра, полученные данные записать в таблицу.
1.3. Построить график зависимости D = f(Vэл), по нему найти пороговый объем электролита V к, вызывающие быструю коагуляцию золя.
1.4. Рассчитать значение с к по формуле
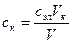
где с эл – концентрация электролита, моль/л;
Vк - пороговый объем электролита, мл;
V - объем золя, мл.
2. Определение защитного числа казеина.
2.1. В 10 пробирок налить золь и растворы в следующем объеме и последовательности:
Таблица 2
| № пробирки | ||||||||||
| Объем золя, мл | ||||||||||
| Объем воды, мл | 6,5 | 7,0 | 7,5 | 8,0 | 8,5 | 9,0 | 9,5 | |||
| Объем раствора казеина Vст, мл | 5,0 | 4,0 | 3,5 | 3,0 | 2,5 | 2,0 | 1,5 | 1,0 | 0,5 | |
| Объем раствора электролита, мл | В объеме, соответствующем V к | |||||||||
| Оптическая плотность, D |
 Общий объем проб должен быть одинаковым и составлять 20 мл. Электролит-коагулятор добавить через 10-15 минут после введения казеина (для адсорбции казеина на частицах золя). Оптическую плотность золя измерить через 3-5 минут после введения электролита. Измерения производить при l = 480 нм (толщина кюветы 10 мм). Значения D записать в таблицу 1.
Общий объем проб должен быть одинаковым и составлять 20 мл. Электролит-коагулятор добавить через 10-15 минут после введения казеина (для адсорбции казеина на частицах золя). Оптическую плотность золя измерить через 3-5 минут после введения электролита. Измерения производить при l = 480 нм (толщина кюветы 10 мм). Значения D записать в таблицу 1.
2.3. Построить график зависимости D = f (V ст). Найти объем раствора казеина Vзащ, необходимый для предотвращения коагуляции золя.
2.4. Рассчитать защитное число 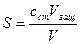 ,
,
где с ст – концентрация раствора стабилизатора, г/л;
V защ –объем раствора стабилизатора, необходимый для предотвращения коагуляции золя, мл;
V – объем золя, мл.
Контрольные вопросы
1. Что такое защитное действие ВМС?
2. Механизм образования защитного действия.
3. Флокуляция.
4. Сенсибилизация.
5. Действие стабилизаторов.
6. Особенности белков как стабилизаторов. Смешанные пленки.
7. Влияние заряда на прочность макромолекул.
8. Осмотическое расклинивающее давление.
1. Зимон А.Д. Коллоидная химия. – М.: Агар. 2001. 320 с.
2. Фридрихсберг Д.А. Курс коллоидной химии. – Л.: Химия. 1984. – 300 с.
3. Хмельницкий Р.А. Физическая и коллоидная химия. – М.: Высш. шк. 1988. – 400 с.
4. Фролов Ю.Г., Гродский А.С. Лабораторные работы и задачи по коллоидной химии. – М.: Химия, 1986. – 216 с.
5. Практикум по коллоидной химии /Под ред. И.С. Лаврова. – М.: Высш. шк., 1983. – 216 с.
 2015-09-06
2015-09-06 834
834






