Газификацией называют высокотемпературные процессы взаимодействия органической массы твердых или жидких горючих ископаемых или продуктов их термической переработки с воздухом, кислородом, водяным паром, диоксидом углерода или их смесями, в результате которых органическая часть топлива обращается в горючие газы.
Единственным твердым остатком при газификации должна явиться негорючая часть угля — зола. В действительности не удается полностью перевести органическую массу угля в газ, и в шлаке остается часть горючей массы топлива.
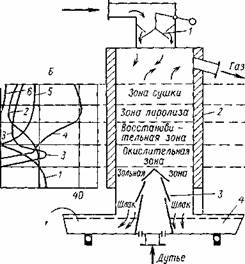
Общие принципы работы аппаратов для газификации — газогенераторов—можно рассмотреть на примере простейшего газогенератора, изображенного на рис 2.
Рис. 2. Схема работы слоевого газогенератора:
А — устройство газогенератора 1 — затвор, 2 — корпус газогенератора, 3 — колосниковая решетка; 4 — чаша для отвода золы;
Б — изменение состава газа по высоте газогенератора (паровоздушное дутье, обогащенное кислородом)- 1 — кислород, 2 — водяной пар, 3 — диоксид углерода, 4 — монооксид углерода, 5 — водород, 6 — метан и пары смолы; В — распределение температур по высоте газогенератора
Газогенератор такого типа представляет собой вертикальную шахту из листовой стали, футерованной огнеупорным кирпичом. В верхней части его имеется загрузочный люк, снабженный затвором 1. В нижней части газогенератора установлена колосниковая решетка 3, через которую в шахту непрерывно подается газифицирующий агент. Сверху непрерывно поступает уголь. При подаче в газогенератор воздуха в зоне, расположенной непосредственно у колосниковой решетки (окислительная зона, или зона горения), происходит горение твердого горючего ископаемого с образованием СО и СО2 по реакциям-
2С + О2 = 2СО + 218,8 МДж/кмоль углерода (2.1)
С + О2 = СО2 + 394,4 МДж/кмоль углерода (2.2)
Образующийся диоксид углерода в восстановительной зоне восстанавливается новыми порциями углерода в оксид углерода:
СО2 + С = 2СО— 175,6 МДж/кмоль углерода (2.3)
Если вместе с воздухом в генератор подают также водяной пар, то в восстановительной зоне дополнительно протекают реакции:
С + Н2О = СО + Н2 — 132,57 МДж/кмоль углерода (2.4)
С + 2Н2О = СО2 + 2Н2 — 89,5 МДж/кмоль углерода (2.5)
В этом случае образующийся газ содержит два горючих компонента: оксид углерода и водород.
В газовой фазе могут протекать и другие реакции. Так, возможна реакция между оксидом углерода и водяным паром:
СО + Н2О=СО2 + Н2 + 43,1 МДж/кмоль (2.6)
При взаимодействии СО и Н2 может образоваться метан:
СО + ЗН2 =СН4 + Н2О + 203,7 МДж/кмоль (2.7)
который в условиях процесса подвергается термическому распаду
СН4 —> С + 2Н2 —71,1 МДж/кмоль (2.8)
Сочетание всех этих реакций и определяет состав образующегося газа, который изменяется по высоте газогенератора. После окислительной и восстановительной зон, называемых вместе зоной газификации, выходят горячие газы при температуре 800—900 °С. Они нагревают уголь, который подвергается пиролизу в вышележащей зоне. Эту зону принято называть зоной пиролиза, или зоной полукоксования. Выходящие из этой зоны газы подогревают уголь в зоне сушки. Вместе эти две зоны образуют зону подготовки топлива. Таким образом, при слоевой газификации сочетается термическая переработка топлива и собственно газификация полукокса или кокса, полученного в зоне подготовки топлива. Поэтому газ, отводимый из аппарата, содержит не только компоненты, образовавшиеся в процессе газификации, но и продукты пиролиза исходного твердого горючего ископаемого (газ пиролиза, пары смолы, водяной пар). При охлаждении отводимого из газогенератора газа происходит конденсация смолы и воды, которые далее необходимо очистить и подвергнуть переработке.
В этом процессе изменяется и состав твердой фазы. В зону газификации, как отмечалось выше, поступает уже не уголь, а кокс, а из окислительной зоны выводится раскаленный шлак, который охлаждается в чаше 4 с водой, выполняющей одновременно функции гидравлического затвора, а затем выводится из аппарата.
Из изложенного выше следует, что газификация представляет собой сложное сочетание гетерогенных и гомогенных процессов. Возможно и последовательное, и параллельное протекание этих реакций. Механизм этих процессов до сих пор еще до конца не выяснен. Так, если первой стадией взаимодействия кислорода и углерода в зоне горения считают образование поверхностного углерод-кислородного адсорбционного комплекса, то вопрос о том, что является первичным продуктом взаимодействия водяного пара с раскаленным коксом, является предметом дискуссий.
В газогенераторе протекает ряд экзотермических и эндотермических реакций. Равновесия реакций (2.1) и (2.2) смещены в сторону образования СО и СО2. Равновесие эндотермических реакций (2.3) — (2.5) при повышении температуры смещены в сторону образования соответственно СО и Н2, но выход указанных продуктов (равновесный) уменьшается при повышении давления.
Равновесие экзотермической реакции (2.6) сдвинуто в сторону образования исходных продуктов при температурах выше 1000 °С и не зависит от давления.
Образование метана по реакции (2.7) более вероятно при повышении давления газификации.
Термодинамические расчеты позволяют определить равновесные составы газов в зависимости от температуры и давления газификации. Однако использовать результаты этих расчетов для предсказания реального состава газов трудно из-за значительных различий в скоростях реакций и влияния на процесс ряда технологических факторов.
Скорость реакций газификации лимитируется скоростью химических превращений в газовой фазе и на поверхности твердой фазы, а также скоростью диффузии. При температурах 700—800 °С процесс газификации тормозится преимущественно химической реакцией, а при температурах выше 900 °С — преимущественно диффузией. В реальных условиях суммарный процесс газификации протекает в промежуточной области, и скорость его зависит от кинетических и диффузионных факторов.
Процессы газификации интенсифицируют путем повышения температуры, увеличения давления газификации (что позволяет значительно увеличить парциальные давления реагирующих веществ), а также увеличения скорости дутья, концентрации кислорода в дутье или развития реакционной поверхности.
Для приближения процесса газификации к кинетической области используют тонкоизмельченный уголь и ведут процесс при высоких скоростях газовых потоков.
Выход газа, его состав и теплота сгорания изменяются в зависимости от того, что используется в качестве дутья. Названия газов, получаемых при использовании различных видов дутья, приведены ниже:
Дутье Название
Сухой воздух Воздушный газ
Смесь воздуха и водяного пара Полуводяной газ
Водяной пар (при внешнем подводе тепла) Водяной газ
Смесь кислорода и водяного пара Оксиводяной газ (газ парокислородного дутья)
Для сопоставления составов и свойств этих газов следует сделать следующие допущения: газовая смесь состоит только из горючих компонентов (единственный возможный балласт — азот воздуха); газифицируется чистый углерод; не учитываются потери тепла. Газы, отвечающие этим допущениям, называют идеальными генераторными газами.
Получаемые на практике генераторные газы отличаются по выходу и составу от идеальных. Во-первых, уголь нельзя считать чистым углеродом, поэтому выход горючих компонентов в расчете на 1 кг органической массы угля всегда значительно меньше. В первую очередь это относится к молодым углям, отличающимся высоким содержанием кислорода, а тем более к торфу.
Во-вторых, в генераторных газах всегда содержится заметное количество СО2. Химическое равновесие в газогенераторах не достигается, поэтому содержание СО2 всегда превышает равновесную концентрацию.
В-третьих, в зоне подготовки угля образуются пары воды и летучие продукты термического разложения, которые попадают в состав газа.
В любом газе содержится большее или меньшее количество азота, что снижает реальную теплоту сгорания газа, так как при сжигании газа часть тепла расходуется на нагревание балластного азота.
В реальных условиях газификации вследствие неравномерного распределения зон и смешения потоков часть горючих газов сгорает с образованием водяного пара и СО2. Кроме того, в реальных условиях газификации неизбежны различные тепловые потери (в окружающую среду, с горячими газами, со шлаком и уносимым топливом). Поэтому фактические значения термических коэффициентов полезного действия значительно меньше величин, рассчитанных для идеальных условий.
Процессы газификации можно классифицировать по следующим признакам:
1) по теплоте сгорания получаемых газов (в МДж/м3): получение газов с низкой (4,18—6,70), средней (6,70—18,80) и высокой (31—40) теплотой сгорания;
2) по назначению газов: для энергетических (непосредственного сжигания) и технологических (синтезы, производство водорода, технического углерода) целей;
3) по размеру частиц используемого топлива: газификация крупнозернистых, мелкозернистых и пылевидных топлив;
4) по типу дутья: воздушное, паровоздушное, кислородное, парокислородное, паровое;
5) по способу удаления минеральных примесей: мокрое и сухое золоудаление, жидкое шлакоудаление;
6) по давлению газификации: при атмосферном (0,1 — 0,13 МПа), среднем (до 2—3 МПа) и высоком давлении (выше 2—3 МПа);
7) по характеру движения газифицируемого топлива: в псевдостационарном опускающемся слое, в псевдоожиженном (кипящем) слое, в движущемся потоке пылевидных частиц;
8) по температуре газификации: низкотемпературная (до 800 °С), среднетемпературная (800—1300 °С) и высокотемпературная (выше 1300 °С);
9) по балансу тепла в процессе газификации: автотермический (стабильная температура поддерживается за счет внутренних источников тепла в системе) и аллотермические, т. е. нуждающиеся в подводе тепла со стороны для поддержания процесса газификации. Внешний подвод тепла можно осуществлять с помощью твердых, жидких и газообразных теплоносителей [10].
 2015-09-06
2015-09-06 1131
1131
