Вопросы для самоподготовки
1. Корпускулярно-волновой дуализм. Уравнение Де Бройля.
2. Принцип неопределённости. Вероятностная модель атома.
3. Электронная орбиталь. Граничная поверхность и кривая радиального распределения электронной вероятности.
4. Уравнение Шрёдингера. Волновая функция, её физический смысл.
5. Главное квантовое число. Орбитальное квантовое число. Энергетические уровни и подуровни.
6. Магнитное квантовое число. Ориентация орбиталей в пространстве. Спин и спиновое квантовое число.
7. Эффекты экранирования и проникновения электрона к ядру.
8. Правила Клечковского. Распределение орбиталей по энергии.
9. Принцип запрета Паули. Правило Хунда.
10. Периодический закон Д.И. Менделеева.
11. Структура периодической системы химических элементов.
12. Внутренняя и вторичная периодичность в изменении свойств химических элементов.
13. Периодические свойства химических элементов: эффективный заряд, атомный радиус, электроотрицательность.
14. Энергия ионизации и характер ее изменения в периодах и группах.
15. Сродство к электрону и характер его изменения в периодах и группах.
16. Виды аналогий в периодической системе элементов.
Задания
1. Каков атомный номер и атомная масса элемента, ядро которого состоит из 81 протона и 122 нейтронов?
2. Элемент таллий (атомный номер - 81) представляет собой смесь изотопов 203Tl (30,8%) и 205Tl (69,2%). Рассчитайте относительную атомную массу таллия. Определите состав ядра каждого из изотопов.
3. Составить электронно-графические схемы ионов V2+ и V3+.
4. Структура валентного электронного слоя атома элемента выражается формулой 4s24p4. Определите порядковый номер элемента. В каком периоде, какой группе и подгруппе периодической системы он расположен? Ответ мотивируйте.
5. Какое максимальное число электронов может содержать атом в электронном слое со значением главного квантового числа n = 6. Сколько значений орбитального и магнитного орбитального квантовых чисел соответствует этому числу?
7. Составить электронно-графические схемы ионов Сr2+ и Cr3+.
8. Составить электронно-графические схемы ионов Fe2+ и Fe3+. Чем можно объяснить особую устойчивость электронной конфигурации иона Fe3+?
9. Могут ли электроны атома Са (IV период, IIА подгруппа) находиться на следующих орбиталях: 3s, 2d, 4p. Ответ мотивируйте.
Примеры решений
Пример № 1. Символ изотопа элемента 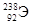 . Определить а) число нуклонов в ядре, б) число электронов, содержащихся в электронной оболочке атома.
. Определить а) число нуклонов в ядре, б) число электронов, содержащихся в электронной оболочке атома.
Решение. Заряд ядра элемента Z = 92, число протонов в ядре также равно 92. Число нейтронов составит:
N = А – Z = 238 – 92 = 146
Число электронов в атоме равно заряду ядра, в данном случае - 92.
Пример № 2. Составьте электронные и электроно-графические формулы элементов второго периода.
Решение. При составлении электронной формулы атома или другой атомной частицы числом указывается главное квантовое число, буквой - орбитальное квантовое число и верхним индексом - число электронов на подуровне.
У элементов второго периода происходит последовательное заполнение второго энергетического уровня, начиная с конфигурации 1s22s1 (Li) и заканчивая конфигурацией 1s22s22p6 (Ne).
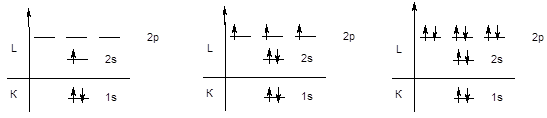
Li 1s22s1 N 1s22s22p3 Ne 1s22s22p6
Пример № 3. Составить электронно-графическую схему иона Mn2+.
Решение. Элемент расположен в IV периоде, в подгруппе VII B, следовательно это – d-элемент, у которого на внешнем, четвертом, электронном слое размещается только 2 электрона на 4s-подуровне, оставшиеся 5 электронов - на внутреннем 3d-подуровне: Mn - KL3s23p63d54s2.
При образовании иона Mn2+ с внешнего электронного уровня уходят 2 электрона и электронная формула приобретает следующий вид KL3s23p63d54s0. Распределение электронов по орбиталям передатся следующей схемой:
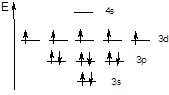
Пример № 4. Составьте электронную формулу мышьяка, а также электронно-графическую формулу внешнего и предвнешнего энергетических уровней.
Решение. Элемент расположен в IV периоде, в подгруппе V А, следовательно это – р-элемент, у которого на внешнем, четвертом, электронном слое размещается 5 электронов на 4s- и 4р-подуровнях, а внутренний слой М (3s-, 3р-, 3d-подуровни) уже завершен: As (Z = 33): 1s22s22p63s23p63d104s24p3 или KLM4s24p3
Графическая формула выглядит следующим образом:
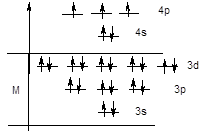
Пример № 5. Распределите подуровни 5s, 4p, 4d в порядке заполнения их электронами.
Решение. Найдем главное и орбитальное квантовые числа, отвечающие указанным подуровням, и суммы этих чисел:
| Подуровень | n | l | n + l |
| 5s | |||
| 4p | |||
| 4d |
Согласно правилам Клечковского, наибольшая сумма (n + l) отвечает подуровню 4d; у подуровней 5s и 4р суммы (n+l) одинаковы, но число n меньше у подуровня 4р. Отсюда подуровни застраиваются в следующем порядке: 4p, 5s, 4d.
Пример № 6. Какие элементы открывают и завершают подуровни: а) 6р; б) 4d?
Решение. Открывать и завершать указанные подуровни будут: а) элементы с конфигурациями 6р1 и 6р6 на внешнем уровне, т. е. Tl (Z = 81) и Rn (Z = 86); б) элементы с конфигурациями d1 и d10 на предвнешнем уровне, т.е. Y (Z = 39) и Cd (Z = 48).
 2015-10-16
2015-10-16 1316
1316