d 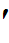 Q=dU+pdV,
Q=dU+pdV,
pdV=0; d 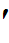 U=dU,
U=dU,
Первое начало термодинамики приобретает такой вид.
Теплоемкость при V-const:
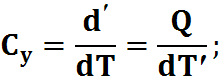
Теплоемкость определяется отношение приращения полученного системой тепла к приращению температуры.
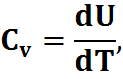
2) Изобарический процесс:
P=const;
d  Q=dU+d
Q=dU+d  A;
A;
Разделим на dT (для 1 моля газа):
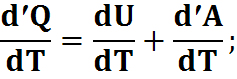
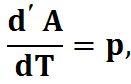
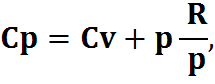
pV=RT,
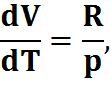
Cp=Cv+R,
3) Изотермический процесс:
T=const,
PV=A;
Поскольку внутренняя энергия зависит от T, то при изотермическом расширении dU=0:
d 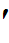 Q=d
Q=d 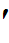 A,
A,
Подводимые к газу при изотермическом расширении тепло целиком превращается в работу расширения.
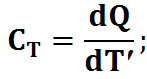
dQ стремится к ∞, dT стремится к 0.
4) Адиабатический процесс:
Без теплообмена с окружающей средой. Первое начало термодинамики приобретает вид:
d 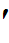 Q=0; dU+d
Q=0; dU+d 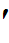 A=0,
A=0,
dU+d 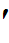 A=0; d
A=0; d 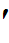 A=-dU,
A=-dU,
 2015-10-13
2015-10-13 683
683








