∆Н 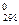 и ∆S
и ∆S 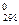 находим из соотношений
находим из соотношений
∆H298 = ∑ni∆Hпрод – ∑nj∆Hисх,
ΔS 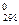 =ΣniS
=ΣniS 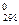 прод – ΣnjS
прод – ΣnjS 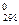 исход .
исход .
∆Н 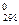 = (3 (-110,52) + 2·0) – (-822,10 + 3·0) = -331,56 + 822,10 =
= (3 (-110,52) + 2·0) – (-822,10 + 3·0) = -331,56 + 822,10 =
= 490,54 кДж;
∆S 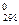 = (2·27,2 + 3·197,91) – (89,96 + 3·5,69) = 541,1 Дж/К
= (2·27,2 + 3·197,91) – (89,96 + 3·5,69) = 541,1 Дж/К
Энергию Гиббса при соответствующих температурах находим из соотношения: ∆G 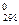 =∆Н
=∆Н 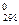 - Т · ∆S
- Т · ∆S 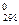
∆G500= 490,54 – 500 · 541,1/1000 = +219,99 кДж;
∆G1000= 490,54 – 1000 · 541,1/1000 = -50,56 кДж.
Так как ∆G500> 0, а ∆G1000< 0, то восстановление Fe2O3 углеродом возможно при 1000 К и невозможно при 500 К.
 2015-10-14
2015-10-14 245
245








