Взаимодействие этих веществ возможно либо в результате происходит связывание ионов с образованием слабых электролитов (Н2О, HСlO), осадка (PbS↓), газа (СО2↑). Запишем уравнения взаимодействия указанных веществ в молекулярном виде:
а) НСl + NaOH = NaCl + H2O,
в ионном виде:
H+ + Cl- + Na+ + OH- = Na+ + Cl- + Н2O,
исключив одинаковые ионы Na+ и Cl- из обеих частей равенства, получим краткое инно-молекулярное уравнение:
Н+ + ОН- =Н2О.
б) Pb(NO3)2 + Na2S = PbS↓ + 2NaNO3;
Pb2+ + 2NO 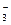 + 2Na+ + S2- = PbS↓+ 2Na+ + 2NO
+ 2Na+ + S2- = PbS↓+ 2Na+ + 2NO 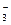 ;
;
Pb2+ + S2- = PbS↓.
в) NaClO + HNO3 = NaNO3 + HClO;
Na+ + ClO- + H+ + NO 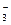 = Na+ + NO
= Na+ + NO 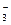 + HClO;
+ HClO;
H+ + ClO- = HClO.
г) K2CO3 + H2SO4 = K2SO4 + CO2↑ + H2O;
2K+ + CO 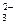 + 2H+ + SO
+ 2H+ + SO 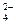 = 2K+ + SO
= 2K+ + SO 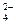 + CO2↑ + H2O;
+ CO2↑ + H2O;
CO 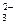 + 2H+ = CO2↑ + H2O
+ 2H+ = CO2↑ + H2O
д) В реакции два слабых электролита (СН3СООН и H2O), но так как реакции идут в сторону большего связывания ионов и вода – более слабый электролит (константа диссоциации воды 1,8 · 10-16 (табл. 6)), чем уксусная кислота (константа диссоциации уксусной кислоты 1,8 · 10-5 (табл.6)), равновесие реакции смещено в сторону образования воды:
СН3СООН + NaOH = CH3COONa + H2O;
CH3COOH + Na+ + OH- = CH3COO- + Na+ + H2O;
CH3COOH + OH- = CH3COO- + H2O.
Пример 2. Составьте молекулярные уравнения реакций, которым соответствуют следующие ионно-молекулярные уравнения:
a) SO 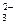 + 2H+ = SO2 + H2O;
+ 2H+ = SO2 + H2O;
b) Pb2+ CrO 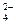 = PbCrO4;
= PbCrO4;
c) HCO 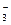 + OH- = CO
+ OH- = CO 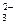 + H2O;
+ H2O;
d) ZnOH+ + H+ = Zn2+ + H2O.
 2015-10-14
2015-10-14 297
297







