Газовые законы
Состояние газа определяется тремя параметрами: давлением (Р), температурой (Т) и объемом (V). Взаимосвязь этих параметров для определенного количества газа выражается газовыми законами.
1. Закон Бойля – Мариотта: при постоянной температуре для заданного количества газа его давление пропорционально объему:
PV = Const или P1V1 = P2V2 для состояния 1 и 2
2. Закон Гей – Люссака: при постоянном давлении объем заданного количества газа пропорционален его абсолютной температуре:
V = c(t + 273), где с – постоянная величина, или  для состояний 1 и 2.
для состояний 1 и 2.
3. Закон Шарля: при постоянном объеме давление заданного количества газа пропорционально его абсолютной температуре:
Р = c(t + 273), где с – постоянная величина, или  для состояний 1 и 2.
для состояний 1 и 2.
Соотношение всех трех параметров для двух состояний 1 и 2 определенного количества газа показывает объединенный газовый закон:

 , причем, какой это газ или смесь газов не имеет значения.
, причем, какой это газ или смесь газов не имеет значения.
Так по закону Авогадро в равных объемах различных газов при одинаковых условиях содержится одинаковое число молекул.
Если состояние 2 отвечает нормальным условиям (Т = 273,15 К, Р = 101,3·103 Па), состояние «0» (ноль), то объединенный газовый закон принимает вид: 
 .
.
Из закона Авогадро можно вывести следствия:
1. Один моль газообразного вещества содержит одинаковое число структурных единиц, которое называется числом Авогадро (Na = 6,02 · 1023). Это следствие справедливо для веществ в любом агрегатном состоянии.
2. Один моль любого газообразного вещества при одинаковых условиях занимает одинаковый объем. Эксперимент показал, что этот объем при нормальных условиях равен 22,4 л (в СИ 22,4 · 10-3 м3). Его называют молярным объемом газообразного вещества при нормальных условиях (VМ,О = 22,4 л/моль = 22,4 · 10-3 м3/моль).
Для одного моль газа правая часть объединенного газового закона принимает конкретную величину:
 , где величина R – универсальная газовая постоянная.
, где величина R – универсальная газовая постоянная.
Объединенный газовый закон для n моль газа можно записать так:
 или
или 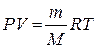
Это выражение называется уравнение Клапейрона – Менделеева.
Закон дальтона: общеедавление смеси газов равно сумме парциальных давлений составных частей (компонентов):
Р = P1+ Р2 + … + Рk
где Р – общее давление смеси газов, P1, P2 – парциальные давления компонентов смеси. Парциальным давлением называется давление каждого компонента, если бы он один занимал объем, равный объему смеси при той же температуре.
Зависимость между парциальными давлениями и общим выражается уравнениями:
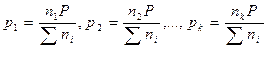
Таким образом, парциальное давление каждого компонента равно произведению его мольной доли на общее давление смеси.
Для идеальных газов мольная доля cравна объемной доле φ.
Кинетическая теория газов. Основным уравнением кинетической теории газов для одного моль является уравнение:
PV=1/3NAmu2
где т – масса молекулы; и – средняя квадратичная скорость молекул; NA – число молекул в одном моль. Для любого количества вещества в уравнение вместо NА входит N. Из основного уравнения кинетической теории газов можно вывести изложенные выше газовые законы и некоторые новые положения.
Для одного моль газа: 1/3NAmu2 = RT
Отсюда средняя квадратичная скорость молекул:
 , где М = Nат – масса одного моль газа.
, где М = Nат – масса одного моль газа.
Из этого уравнения следует, что для одного и того же газа средняя квадратичная скорость молекул прямо пропорциональна корню квадратному из абсолютной температуры:
 , где u1 – средняя квадратичная скорость при температуре T1, а и2 – при Т2. Для различных газов при одинаковой температуре средняя квадратичная скорость молекул обратно пропорциональна корню квадратному из молекулярных масс:
, где u1 – средняя квадратичная скорость при температуре T1, а и2 – при Т2. Для различных газов при одинаковой температуре средняя квадратичная скорость молекул обратно пропорциональна корню квадратному из молекулярных масс:
 , где и1 и М1 относятся к первому газу, а u2 и М2 – ко второму.
, где и1 и М1 относятся к первому газу, а u2 и М2 – ко второму.
NАmu2/2=3/2RT.
Выражение, стоящее в левой части этого равенства, есть средняя кинетическая энергия поступательного движения молекул одного моль идеального газа. Обозначив ее через Е -
E=3/2RT.
Средняя кинетическая энергия поступательного движения одной молекулы газа равна:
e = 3/2kT, где k = R/N постоянная Больцмана.
Следовательно, кинетическая энергия идеального газа пропорциональна абсолютной температуре.
 2015-10-22
2015-10-22 1236
1236
