Пример 1.Определите тип химической связи в молекулах NaBr, HBr, Br2.
Решение. Тип химической связи в молекуле можно определить, сравнивая значения электроотрицательностей (ЭО) атомов, входящих в ее состав (см. табл. 1.1).
Молекулы, образованные атомами, имеющими одинаковую ЭО, являются электросимметричными, химическая связь в них– ковалентная неполярная (Br2).
Если электроотрицательности атомов отличаются друг от друга (как в данном случае, в молекуле NaBr − ЭОNa =0,9, ЭОBr =2,8; в молекуле HBr − ЭОH=2,1, ЭОBr=2,8), то связь в молекуле – ковалентная полярная.
С увеличением разности между ЭО атомов растет степень ионности связи в молекуле. Разность ЭО, равная 1,7, соответствует 50%-ному ионному характеру связей, поэтому связи с разностью больше 1,7 могут считаться ионными.
В молекуле NaBr – разность ЭО равна 1,9; следовательно, химическая связь в ней – ионная.
В молекуле HBr разность ЭО равна 0,7 и соответственно, связь – ковалентная полярная.
Пример 2. Приведите орбитальную схему перекрывания электронных облаков в молекуле BH3.
Решение. Перекрывание sp 2 -гибридных орбиталей атома бора с 1 s -АО трех атомов водорода приводит к образованию треугольной (тригональной) молекулы гидрида бора BH3.
Ввалентный угол H–B–H в молекуле BH3 равен 120° (рис. 2.15).
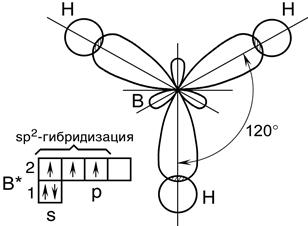
Рис. 2.15. Пространственная конфигурация молекулы BH3
Пример 3. Укажите тип гибридизации и валентные углы в молекуле BeCl2.
Решение. В молекуле ВеСl2 обе химические связи равноценны несмотря на то, что в их образовании участвуют различные орбитали (s и p) центрального атома (электронная формула атома Be в возбужденном состоянии 1s22s12p1). Это объясняется гибридизацией s- и p-орбиталей, приводящей к образованию двух гибридных sp-орбиталей.
Перекрывание 2−х sp -гибридных орбиталей атома бериллия с 3 p- атомными орбиталями 2−х атомов хлора приводит к образованию линейной молекулы хлорида бериллия ВеСl2.
Валентный угол Cl–Be–Cl в молекуле ВеСl2 равен 180°.
 2015-10-22
2015-10-22 3809
3809








