Уравнение состояния идеальных газов имеет вид
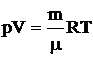 , (2.1)
, (2.1)
где p – давление газа, Па;
V – объем газа, м3;
m – масса газа, кг;
μ – молярная масса газа, кг/моль;
R – универсальная газовая постоянная, R = 8,31 Дж/моль·К;
T – температура, К.
Уравнение Менделеева-Клапейрона хорошо описывает поведение одного моля любого газа при малых давлениях и высоких температурах. Этому замечательному уравнению подчиняются и воздух, которым мы дышим, и раскаленные газы в топках, и плазма внутри звезды.
 2017-11-30
2017-11-30 624
624








