Предисловие.
Будучи огорчен качеством преподавания химии в РНИИМУ, и тем более, способом последующего контроля качества образования – тестами, я решил оказать посильную помощь студентам в сдаче оных. Пособие представляет собой краткую, насколько возможно, инструкцию, как минимально загрузив голову таки сдать этот окаянный тест. Я исследовал большое их количество, обобщил результаты.
На каждый вид вопросов я постарался дать ответ, в меру научный, чтобы все-таки не слишком уйти от своих химических корней, но и достаточно ясный, чтобы он мог быть воспринят среднестатистическим студентом. Теперь я представляю свой труд для использования широкой общественностью, надеюсь, моё творение сможет послужить к чьей-нибудь пользе.
Тема несложная, и, что важно, она опирается на простую и красивую теорию. Очень рекомендуем вникнуть в теоретическое описание, приведённое перед разборами вопросов. На этот раз оно получилось кратким, содержательным и, хотелось бы надеяться, понятным. Тема имеет связи с настоящей медициной, еще и поэтому рекомендуется к подробнейшему изучению.
Конечно, многим хотелось бы иметь готовые ответы и не париться. Думаю, что за годы работы eois общественность накопила некоторый объем ответов, он постепенно совершенствуется, доля верных ответов растет, уже в 2016 она была больше 70%. Правда, обновление вопросов в 2017 добавило веселья. Однако, в отношении химии мне это кажется неудачным путем. Объясню, почему я так считаю. Во-первых, вопросов большое количество, и они, как назло, очень похожи. Это делает трудным списывание с правильных ответов, и, одновременно, делает тесты уязвимыми к методичкам вот такого плана, с разбором вопросов на группы и злой иронией по этому поводу. Во-вторых, некоторые персонажи, как Карина, например, почему-то борются со списыванием, что делает этот процесс не самым простым трюком. А глядя на всё это глобально, по-моему, все же лучше что-то понимать и мыслить, чем списывать.
Заранее благодарен за адекватные комментарии, дополнения и исправления к тексту. Текст создан исключительно из гуманных соображений и распространяется безвозмездно.
Удачи, ни пуха, ни пера, дорогие любители химии.
Алексей «Леша-химик» Федоров
14.10.2017.
Тема 7. Буферные растворы.
Введение:
Тема, как мы уже заметили, устроена очень красиво. Будет много проще, если Вы поймете эту красоту, тогда не будет нужды (она всё равно будет) в делении на вопросы, каких-то хитростях, и тому подобной хуите. Если теория — это не ваше, можете спокойно дропнуть этот раздел (только таблица обязательно нужна), в вопросах тоже есть всё нужное, чтобы еле-еле пройти порог. Так что мы настоятельно рекомендуем остаться с нами.
Итак, буферные растворы. Скорее всего, вы знаете, что в человеческом желудке сильнокислая среда, и нужно это затем, чтобы расщеплять белки до аминокислот. Но, что если человек выпьет три литра воды? Кислота разбавится, да еще и всё это стечет в кишечник, а там среда щелочная, в итоге все нейтрализуется, человек не сможет усваивать ни белки, ни углеводы, и всё пойдёт по пизде, и подопытный сдохнет? Однако, точно известно, что три литра воды к смерти не приводит, хотя и весёлого мало. Желающие идут проверять, остальные продолжают курить теорию вместе с нами.
Буферный раствор — раствор, поддерживающий рН (кислотность, короче) постоянным при добавлении кислот и щелочей в небольших количествах и разбавлении. Организм человека — почти сплошные Буферные растворы. Оговоримся: у буферного раствора есть ёмкость, при которой он может поддерживать рН относительно постоянным. Бесконечное количество кислоты или щелочи, конечено, ни один буферный раствор не нейтрализует.
Но постойте, это же охренеть! В него льют кислоту — он нейтрализует её. В него льют щелочь — он нейтрализует и её тоже. В него льют воду — он держит рН постоянным и просит ещё. Кто он?!?! Что он такое?!?! Буферный раствор, встречайте (далее БР). Он офигенен. Он просто бесконечно крут. Как он, мать его, это делает? Да он же состоит из сопряженной кислотно-основной пары. Строго надо говорить, что состоит из кислоты и сопряженного основания или основания и сопряженной кислоты. Но мы далее для избежания путаницы будем говорить просто, сопряжённое основание и сопряжённая кислота. Сопряженное основание — это какая-то фигня (слабый электролит) без Н+, сопряженная кислота — та же самая с Н+. Например, NH3 / NH4+. НРО42- / Н2РО4-. СН3СОО- / СН3СООН. И так далее. Полный список см. таблицу (сразу договоримся, что в растворе молеклы легко распадаются на ионы, например поэтому СН3СООNa и СН3СОО- одно и то же. Может встречаться вариант как молекула и как ион, не удивляйтесь. Натрий легко удаляется диссоциацией):
| Название: | Состав | Формула для рН | |
| Сопряженна кислота | Сопряженное основание | ||
| Ацетатная | СН3СООН | СН3СОО- (или СН3СООNа) |  |
| Гидрокарбонатная | Н2СО3 (или СО2+Н2О) | НСО3- (или NаНСО3) |  да, вот тут внезапно да, вот тут внезапно |
| Карбонатная | НСО3- (или NаНСО3) | СО32- (или Nа2СО3) | 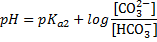 |
| Аммиачная | NH4+ (или NH4Cl) | NH3 |  |
| ДигидроФосфатная | Н3РО4 | Н2РО4- |  |
| Гидрофосфатная | Н2РО4- | НРО42- | 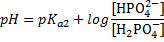 |
| Фосфатная | НРО42- | РО43- |  |
| Аминокислотная-1 | NH3+-CH(R)-COOH Катионная форма | NH3+-CH(R)-COO- Диполярная форма |  |
| Аминокислотная-2 | NH3+-CH(R)-COO- Диполярная форма | NH2-CH(R)-COO- Анионная форма |  |
| И многие другие | НХ | Х |  |
К таблице мы ещё вернемся чуть позже. А сейчас фишка БР-ов.
Как же этот хитрый пидор работает? А вот так. Для примера возьмём аммиачный буферный раствор. Он состоит из сопряженного основания NH3 и сопряженной кислоты NH4+ (то же, что NH4Cl) Имея в виду это, рассмотрим случаи.
1) Если к нему добавили сильную кислоту, например HCl. Так как в БР есть основание (сопряженное), оно будет её нейтрализовывать.
NH3 + HCl = NH4Cl
Или в ионном виде
NH3 + H+ + Cl- = NH4+ + Cl-
А если сократить хлорид
NH3 + H+ = NH4+
Пресвятой Менделеев, получилась сопряженная кислота. Из сопряженного основания получилась сопряженная кислота, при этом важно, что сильная кислота нейтрализовалась нахер. Значит, рН останется примерно постоянным (сопряженная кислота — слабая, она влияет на рН, конечно, но много слабее, чем HCl. Ион Н+ связывается)
2) Если к тому же буферному раствору добавили щелочь. Теперь-то этот пидор не отвертится? Хер там плавал! Ведь в нём есть и сопряженная кислота, которая может нейтрализовать щелочи.
NH4Сl + NaOH = NH3 + H2O + NaCl
Или в ионном виде
NH4+ + Сl- + Na+ + OH- = NH3 + H2O + Na+ + Cl-
Или, сократив одинаковое
NH4+ + OH- = NH3 + H2O
В рот мне ноги, это же сопряжённое основание. Охренеть, из сопряженной кислоты получилось сопряженное основание! А щелочь нейтрализовалась. Сами Гендерсон и Гассельбах охренели бы от такого поворота. А рН остается примерно постоянным. Этот мелкий засранец снова выкрутился. Вот же ж!
Подобные реакции могут быть написаны для любого другого БР и называются механизмами буферного действия. Хотя напрямую это не касается тестов, это может быть в колке, если он будет устным, и, кроме того, половина вопросов тестов как бы подразумевает, что механизм работы БР понятен.
Теперь вернемся к таблице и прокомментируем некоторые подводные грабли. Таблица состоит из названия буферной системы, её компонентов и формулы для расчета рН. Например, если где-то попадается "аммиачная буферная система", то нужно самостоятельно догадаться, что это NH3/NH4+. Это важно, второй раз останавливаться на этом не будем. В составах все просто, основание на Н меньше, кислота на Н больше. Последний столбик — формулы для расчета рН. Они устроены одинаково, по принципу:

Квадратные скобки в записях означают концентрации, однако в принципе на это можно класть хер и подставлять моли, результат всё равно будет верным.
Самая подстава — обратите внимание, что есть формулы с рКа1, есть с рКа2, есть с рКа3. Номер константы соответствует стадии диссоциации той кислоты, что есть в этом БР. Например, в гидрокарбонатной системе кислота Н2СО3, диссоциирующая по первой ступени, в формуле константа рКа1. Для карбонатной буферной системы кислота НСО3-, диссоциирующая уже по второй ступени, поэтому константа в формуле рКа2. Еще более наглядно это видно на группе фосфатных БР. Уделите время пониманию этого, это реально упростит понимание тестовых вопросов.
В конце списка лежат аминокислотные буферные системы. Аминокислоты это — глицин, аланин, валин, лейцин, изолейцин, серин, треонин, цистеин, метионин, аспарагиновая и глутаминовая кислоты, лизин и аргигнин, глутамин и аспарагин, фенилаланин и тирозин, гистидин и триптофан, пролин. Формулы не приводим за ненадобностью. Вам их всё равно скоро учить. Внимательно рассмотрите их, поймите, чем отличаются анионная/диполярная/катионная формы. Там выделено красным. Запомните, что у анионной рКа2, у катионной рКа1, объяснить это сложно, стоит запомнить.
Типичные вопросы:
1. Типы буферных систем.
Пример:
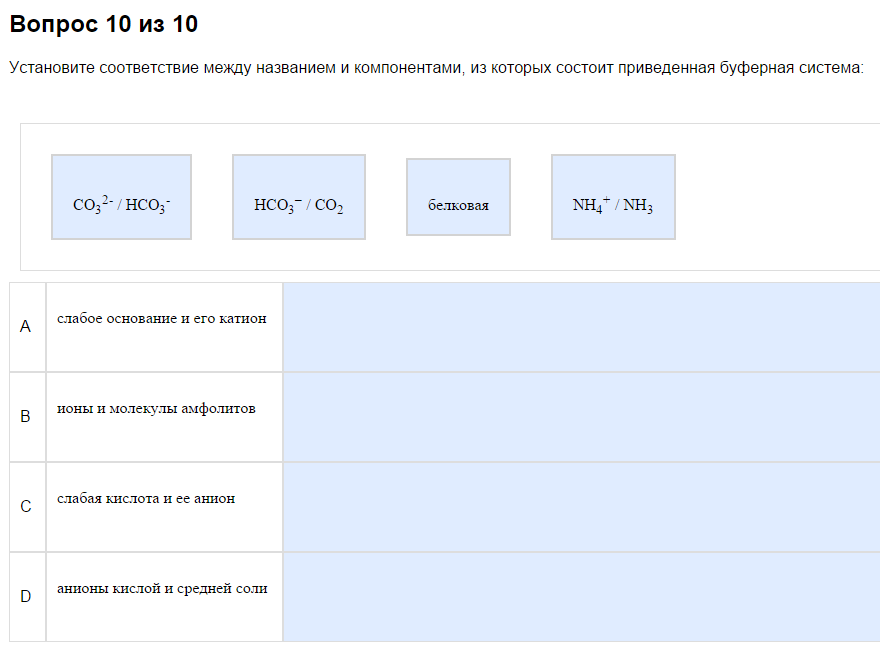
На первый взгляд путано, фактически несложно…
Как с этим бороться:
Всегда в наборе есть
1) Слабая кислота и её анион. Вспомните прошлую тему, найдите, какие кислоты слабые. Здесь то же самое. Чаще всего это что-то-СООН, но не обязательно. В примере это внезапно СО2, потому что обратимо превращается в Н2СО3 в растворе. Ориентир — один минус.
2) Слабое основание и его катион. См. прошлую тему про слабые основания. Чаще всего это амины и аммиак, что-то типа что-то там такое R-NHy. Катион — это один полюс.
3) Анионы кислой и средней соли. О кислых солях также можно почитать в прошлой теме. Обычно что-то вида НА+А, например НСО3-+СО32-, как в примере, кстате. Ориентир — два минуса.
4) Амфолит. Это аминокислоты. Самые большие формулы из предложенных. В них обязательно должны быть СОО(Н) и NH2(3). Они ж аминокислоты, в них и должен быть амин и кислота. Могут быть названиями, глицин, аланин, серин, лизин - это все о них. Могут быть белки, это тоже амфолиты, производные аминокислот. Это в примере.
2. Аминокислотные буфера.
Пример:

Суперлайт…
Как с этим бороться:
Очень легкая задача. Сравниваем рН с рI. Если рН<pI, аминокислоты в катионной и диполярной форме. Если рН>pI, то в анионной и диполярной. Да, всё так просто. Нет, это не наёбка. Нет, ошибки в том, что диполярная использована два раза, нет, так и должно быть, см. таблицу. Осторожно! Во избежания повреждения мозга о том, что такое рI, задумываться не надо!
3. Подбор формулы.
Пример:

Ну так себе…
Как с этим бороться:
Несложно, в целом. Во-первых, если в теории вы ничего не поняли, можно тупо брать формулы из таблицы. Там есть почти все нужное. Обращайте внимание, где первая константа, где вторая, и что на что делить. Большинство формул можно подобрать по таблице или по аналогии, например, БР СН3NH2 / CH3NH3+ является близким аналогом NH3 / NH4+, и формула аналогичная. Если в теории вы разобрались, то еще лучше. БР состоит из пары основание-кислота. Даже если попадется непонятный БР, то в любом случае,
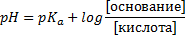
Например, может быть какая-то хрень нетабличная, NaHS+Na2S. Если подумать, то можно догадаться, что первое — кислота, второе — основание. Если сравнить с карбонтаной и гидрокарбонатной системой, можно догадаться, что тут нужна рКа2. Итого:

Самое жопошное — аминокислоты. Выучите или запишите, где рКа1, где рКа2, там это нельзя вывести. В примере ответ В.
4. Интервал буферного действия.
Пример:

…
Как с этим бороться:
Тоже очень просто. Интервал буферного действия это область рН от рКа-1 до рКа+1. Например, если рКа=4,75, то интервал равен от 3,75 до 5,75. Подвох в том, что констант может быть дано несколько. Использовать надо ту же самую, по которой считали рН. Ту же самую, которая рКа кислоты в БР. Найти её можно в таблице. Например, если дана карбонатная буферная система (состоит из NaHCO3+Na2CO3), то её рН считается по рКа2 (см. таблицу БР) и следовательно, интервал тоже по ней же. В примере если в БР есть анионная форма, то рН считают по рКа2, следовательно интервал А.
5. Соотношение компонентов, рН и рКа.
Пример:

…
Как с этим бороться:
Всего возможно три случая.
1) рН > pKa, тогда сопряженного основания больше, чем кислоты. Может быть, 10:1, а может просто c(CH3COOK) > c(CH3COOH).
2) рН < pKa, тогда сопряженной кислоты больше, чем основания. Может быть, 1:10, а может просто c(CH3COOK) < c(CH3COOH).
3) рН = pKa, тогда их поровну. Может быть, 1:1, а может просто c(CH3COOK) = c(CH3COOH).
Обратные утверждения также верны.
6. Нейтрализовать больше кислоты / больше щелочи / поровну.
Пример:

…
Как с этим бороться:
Вопрос в целом похож на предыдущий.
На всякий случай расскажем, как это должно быть вообще. Для того, чтобы БР мог нейтрализовать максимальное количество щелочи, в нем должно быть больше кислоты (это может быть выражено как c(CH3COOK):c(CH3COOH)=1:10). Если больше щелочи, то наоборот. Если поровну — то поровну. Заметим, тут мы по дефолту считаем, что вам понятно, что такое сопряженная кислота и сопряженное основание.
У аминокислот всё немного не так.
1) Максимальное количество кислоты — больше анионной формы
2) Максимальное количество щелочи — больше катионной формы
3) Поровну при рН=pI
Нет, множественный выбор в данном случае наёбка, правильный ответ один, А.
7. Задача, в которой смешали.
Пример:

Вот и начинается треш…
Как с этим бороться:
Как со всеми другими задачами, путём расчётов по формулам. Смотрим, из чего состоит БР, подбираем к такому составу формулу. Большая часть описана в таблице, но выпады возможны, и тут мы еще раз рекомендуем курнуть теорию, она несложная и нам очень нравится. В любом случае, даже если теория не далась, из таблицы выводим, что если БР состоит из НРО4 и Н2РО4, то формула такая, с именно рКа2!:
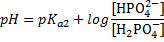
Заметим, в задаче дано для двух веществ объем и концентрация. Как мы уже заметили, ионы и молекулы в растворах можно считать эквивалентными. В формулу подставлять вот так:
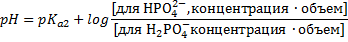
Получается
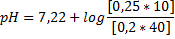
Сначала считаем всё, что под логарифмом:

Потом сам логарифм

И наконец, результат

Округлили до десятых.
Огромная просьба, считать на листочке, записывая ручкой промежуточные результаты. Все вычисления на калькуляторе. Делать всё внимательно и аккуратно, по возможности два-три раза перепроверить!
8. Задача, в которой добавляют сильную кислоту или щёлочь.
Пример:

Градус адеквата растёт.
Как с этим бороться:
Похоже на прошлую задачу в более усложнённом варианте. Есть два случая.
1) Добавили щелочь (NaOH, KOH,...). Если вы втыкали теорию, тогда можете помнить, что сопряженная кислота из БР нейтрализует щелочь, при этом расходуется, при этом образуется сопряженное основание. Формулой это выражается так:

В примере как раз про это, разберем подробнее. В роли сопряженной кислоты Н2РО4-, в роли сопряженного основания НРО42-, в роли щелочи NaOH. Для такой буферной системы, согласно таблице,
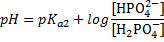
С учетом добавления щелочи

Всё подставляем прямо, как есть переводить ничего никуда не нужно, прям хуярим моли:

Дальнейшие расчеты как в прошлой задаче, сначала под логарифмом, потом сам логарифм, потом всё остальное. Не приводим ввиду очевидности. Ответ рН=7,0, с точностью до десятых.
2) Добавили кислоту, например HCl. Всё то же самое, но формула:

Пример не приводим, он аналогичен прошлой задаче.
9. Задача про буферную ёмкость, Вк или Вщ.
Пример:
Раз

И два:

…
Как с этим бороться:
Тоже по формулам, как ни странно. Буферная ёмкость определение можно посмотреть в методичке с САРСами, а формула:

Тут надо немного прокомментировать. Вк — буферная ёмкость по кислоте. Бывает еще и по щелочи, Вщ, считается почти так же. Ск и Vк — концентрация и объем добавленной кислоты (если считаем ёмкость по щелочи, то исправляем на щелочь). VБР — объем буферного раствора, ΔрН — изменение рН при добавлении кислоты или щелочи. Тонкость в том, что при добавлении щелочи рН увеличивется, а кислоты уменьшается. Чтобы не получить отрицательную ёмкость, правильнее писать
ёмкость по кислоте:

ёмкость по щелочи:

Вертикальные черты читаются как «модуль», это математический оператор, который убирает минус, если он есть.
Первая задача из скрина: всё подставить, посчитать, получить ответ. Заметьте, что концентрация в «М», то есть «моль/л», а ёмкость просят в «ммоль/л», то есть милимоль. Коварные, коварные. Перевод делается умножением на 1000. Получается

Прикиньте, какая фигня может привести к потере бала? EOIS же похер, что вы считаете правильно, но не видите перевод.
Вторая задача уже сложнее, там выводить надо. Вывод, не вдаваясь в тонкости, делается простой перестановкой.

Обратите внимание, тут тоже есть этот ебучий перевод ммоль/л в моль/л. Вк=4,5 ммоль/л мы перевели в 0,0045 моль/л, то есть делили на 1000. Чтобы концентрация с=0,015 моль/л была в одной размерности с Вк. Вопрос, нужно ли вбивать в ответы минус остаётся открытым. Формулировка вопроса «на сколько изменится рН» не определяет однозначно, нужно ли писать этот минус. При добавлении кислоты рН уменьшается на 1,0, то есть изменяется на -1,0. Экспериментально выяснять это нам лень.
10. Норма, ацидоз, алкалоз.
Пример:

…
Как с этим бороться:
Норма — рН от 7,36 до 7,43.
Ацидоз — рН меньше 7,36
Алкалоз — рН больше 7,43
Больше нечего сказать.
11. Буферные системы крови.
Пример:

Наконец-то что-то медицинское…
Как с этим бороться:
Буферные системы крови:
· H2CO3 / HCO3-
· HPO42- / H2PO4-
· Белки, в том числе гемоглобин (Hb- / HbH)
Аж три ответа, B, C, D.
12. Верно-неверно.
Пример:

Жопа химии…
Как с этим бороться:
Смиритесь, несчастные, химическая теория это не ваше. Никак, с этим невозможно ничего сделать. Нет, это не шутка. Поэтому мы просто приводим правильные ответы.
· рН буферного раствора зависит не только от соотношения концентраций сильного и слабого электролита в буферной системе, но и от константы диссоциации кислоты.
· Роль сопряженной кислоты в гидрокарбонатной буферной системе в условиях организма выполняет растворенный СО2
· Гидрокарбонатная буферная система состоит из слабой кислоты и ее аниона
· Анионная форма аминокислоты — частица, в виде которой аминокислота существует в растворах при рН >> p I
· Буферная емкость зависит от суммарной концентрации компонентов буферной системы в растворе
· Диполярный ион — частица, несущая две разноименно заряженных группы атомов
· Ацидоз — нарушение кислотно-основного состояния организма, обусловленное повышенным пониженным значением рН плазмы крови,
· Роль сопряженного основания в карбонатной буферной системе выполняет карбонат-ион
· Ацидоз — патологическое состояние, связанное с пониженной повышенной концентрацией ионов водорода
· Буферная емкость буферных систем организма по кислоте больше, чем по щелочи
· Изоэлектрическая точка α -аминокислоты не зависит от концентрации кислоты в растворе
· Ионы HCO3– и HPO42–НЕ являются диполярными ионами
· Роль сопряженного основания в гидрокарбонатной буферной системе выполняет гидрокарбонат-ион
· Уравнение Гендерсона-Гассельбаха – уравнение, характеризующее зависимость рН буферного раствора только от концентрации от соотношения концентраций слабого электролита и его сопряженной кислоты (основания)
· Буферная емкость — количество кислоты или щелочи, которые нужно добавить к 1 л буферного раствора, чтобы значение его рН изменилось на единицу
· Изоэлектрическая точка – это значение рН раствора, при котором амфолит электронейтрален
· Буферный раствор способен поддерживать практически постоянное значение рН при разбавлении или при добавлении НЕ(!)больших количеств кислоты или щелочи
· Диполярная форма аминокислоты может выступать как в роли кислоты, так и в роли основания
· Изоэлектрическая точка α -аминокислоты НЕ(!)зависит от концентрации кислоты в растворе
· При добавлении к буферной системе щелочи ее буферная емкость по кислоте может увеличиться (в смысле «может»? увеличится)
· Интервал буферного действия определяется как р K а ± 1
· Ацидоз Алкалоз – нарушение кислотно-основного состояния организма, обусловленное повышением рН,
· Катионная форма аминокислоты — частица, в виде которой аминокислота существовует в растворах с рН < p I
· Катионная форма аминокислоты — положительно заряженная частица, в виде которой α -аминокислота существует в растворах при рН < p I
· Интервал буферного действия не зависит от соотношения концентраций компонентов буферной системы в растворе
Прежде, чем предложить Вам, мы всегда проверяем наши теоретически выкладки практикой. Ничего сложного, но задачи грузят, поэтому приличное время.
Спасибо за внимание!
Если вам понравились наши разборы, Вы можете поддержать наш проект тут
https://vk.com/mars_him_prom
через функцию «поддержать…»

За хорошие Буфера Буферные растворы!
 2017-10-31
2017-10-31 23199
23199