В поддержании постоянства рН плазмы принимает участие и фосфатная буферная система, состоящая из слабой кислоты Н2РО4- и сопряженного основания НРО42-. Фосфатная буферная система способна поддерживать постоянство рН в интервале 6,2-8,2 и обеспечивает значительную долю буферной емкости крови.
Для фосфатной буферной системы уравнение Гендерсона-Гассельбаха выглядит так:
 .
.
Подставив физиологическое значение  и значение рН крови в норме, равное 7,4, получим:
и значение рН крови в норме, равное 7,4, получим:
 .
.
Отсюда:
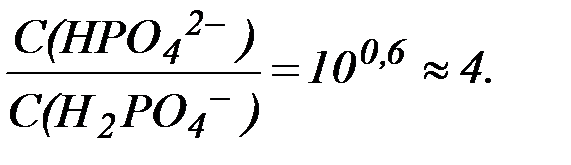
Таким образом, соотношение концентраций Na2HPO4 и NaH2PO4 в фосфатной буферной системе крови приблизительно равно 4, поэтому фосфатная буферная система имеет более высокую емкость по кислоте, чем по щелочи и более эффективно нейтрализует кислые метаболиты плазмы крови, например молочную кислоту и продукты переработки мясной пищи:
НРО42- + HLac⇄Н2РО4- + Lac-
Образующееся в результате нейтрализации избыточное количест-водигидрофосфат-иона H2PO4- выводится почками.
Однако, в отличие от гидрокарбонатной буферной системы, различия буферной емкости фосфатной системы по кислоте и по щелочи не столь существенны. Эти величины составляют:  = 1-2 ммоль/л,
= 1-2 ммоль/л,  = 0,5 ммоль/л.
= 0,5 ммоль/л.
Фосфатная буферная система менее мощная, чем гидрокарбонатная, что объясняется малым содержанием фосфатов в плазме крови. Фосфатная буферная система содержится также в тканях, особенно в почках, и внутри клеток, например, в эритроцитах.
 2017-12-14
2017-12-14 2520
2520
