Типовые задачи с решениями и для самостоятельного решения по теме «Электрический ток в жидкостях и газах»
Типовые задачи по теме лекции
Задача 1.
За какое время t при электролизе медного купороса масса медной пластинки (катода) увеличится на Dm = 99г? Площадь пластинки S = 25см2, плотность тока j =200А/м2. Найти толщину слоя меди, образовавшегося на пластинке.
Решение.
1. Согласно первому закону Фарадея Dm = KIt, откуда
t=Dm/(KI). (1)
Определим значения электрохимического эквивалента К и тока I. 2.Молярная масса меди А = 64×10-3 кг/моль, валентность меди в CuSO4 равна Z=2.Следовательно электрохимический эквивалент
K=A/(F×Z)=332,8×10-9кг/Кл.
2. Сила тока равна:
I=jS. (2)
4.Подставив значение К и выражение для тока (2)в формулу(1), получим:
t =Dm/(K jS. )=99×10-3/( 332,8×10-9×200×25×10-4) = 595 с = 10мин.
5. Определим толщину слоя меди исходя из следующих соображений. Объем образовавшейся меди можно рассчитать по двум формулам:
V = S×d = Dm/r, (3)
где r- плотность вещества (r(Сu)=8,93×103 кг/м3). Следовательно,
d =Dm/(r× S )=4,6×10-6 м.
Ответ: t= 10мин., d = 4,6×10-6 м.
Задача 2.
При получении алюминия электролизом раствора Al2O3 в расплавленном криолите проходил ток I =20кА при разности потенциалов на электродах U =5В. За какое время t выделится масса m=1т алюминия? Какая электрическая энергия W при этом будет затрачена?
Решение.
1.Согласно первому закону Фарадея Dm=K×I×t, откуда
t=Dm/(K×I), (1)
где электрохимический эквивалент K=A/(F×Z).
Молярная масса алюминия А=27×10-3 кг/моль, валентность алюминия равна Z=3.Следовательно электрохимический эквивалент К равен:
K = 27 × 10-3 / (96,48 × 10-3 × 3) = 9,3×10-8 кг/Кл.
Подставим числовые значения в (1):
t = 1×103/(9,3×10-8 × 20×103) = 537634 с = 149,3 час.
3. Затраченная энергия W будет равна работе электрических сил
A = P×t = U×I×t, то есть:
W= U×I×t= 5× 20×103 ×537634= 53,8 ГДж.
Ответ: t = 537634 с = 149,3 час., W= 53,8 ГДж.
Задача 3
Потенциал ионизации атома гелия U = 24,5 B. Найти работу ионизации А.
Решение.
Потенциальная энергия атомов гелия  .
.
По закону сохранения энергии, работа ионизации идет на разрыв связи молекул, т.е. равна потенциальной энергии:

Ответ: А = 39,2·10-19 Дж.
Задача 4
При какой температуре Т атомы ртути имеют кинетическую энергию поступательного движения, достаточную для ионизации? Потенциал ионизации атома ртути U = 10,4 B.
Решение
Средняя кинетическая энергия поступательного движения атомов ртути равна:
 , (1)
, (1)
где k- постоянная Больцмана, k =1,38·10-23 Дж/К.
Потенциальная энергия атомов в металле составляет:
 . (2)
. (2)
По закону сохранения энергии:
Wk =Wп, или 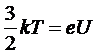 . (3)
. (3)
Из (3) получим:
 .
.
Ответ: Т=8036 К.
Задача 5
При освещении сосуда с газом рентгеновскими лучами в единице объема в единицу времени ионизируется число молекул N=10 16 м-3 ·с -1  . В результате рекомбинации в сосуде установилось равновесие, причем в единице объема газа находится число ионов каждого знака n =1014м-3. Найти коэффициент рекомбинации γ.
. В результате рекомбинации в сосуде установилось равновесие, причем в единице объема газа находится число ионов каждого знака n =1014м-3. Найти коэффициент рекомбинации γ.
Решение:
Количество рекомбинирующих за единицу времени в единице объема пар ионов пропорционально квадрату числа имеющихся в единице объема пар ионов  . Отсюда коэффициент рекомбинации
. Отсюда коэффициент рекомбинации 
Ответ: 
Задача 6.
К электродам разрядной трубки приложена разность потенциалов U =5В, расстояние между ними d = 10см. Газ,находящийся в трубке, однократно ионизирован. Число ионов каждого знака в единице объема газа n = 108м-3; подвижности ионов и+ =3·10-2 м2/(В·с) и и- =3·102м2/(В·с). Найти плотность тока j в трубке.
Решение:
При небольшой плотности тока, текущего в газе, имеет место закон Ома  , (1)
, (1)
где Е -напряженность поля между электродами, которая равна:
 . (2).
. (2).
Так как по условию газ однократно ионизирован, то заряд ионов равен
1,6·10-19Кл. Подставляя (2) в (1), окончательно получим:

Ответ: 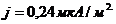
 2017-12-14
2017-12-14 2799
2799