Переважна більшість білків при нагріванні з концентровано нітратною кислотою дає жовте забарвлення. Реакція обумовлена наявністю в білках циклічних амінокислот – тирозину і триптофану, які при взаємодії з нітратною кислотою утворюють нітропохідні жовтого кольору. Амінокислота фенілаланін нітрується важко і її участь в ксантопротеїновій реакції сумнівна. Ксантопротеїнова реакція не є строго специфічною. Оскільки вона обумовлена нітруванням ароматичного кільця, то її дають сполуки, що не є амінокислотами, наприклад, фенол, і не дають білки, в яких відсутні циклічні амінокислоти (желатин).
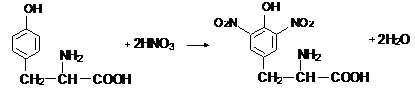
Нітропохідні амінокислот в лужному середовищі утворюють солі хіноїдної природи, забарвлені в оранжевий колір:
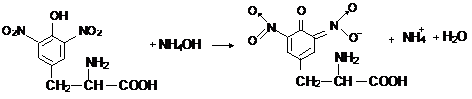
Хід роботи
В пробірку наливають 1 мл розчину білку і додають 5 крапель концентрованої нітратної кислоти. Осад білка, що утворився, обережно підігрівають і спостерігають появу жовтого забарвлення. Пробірку охолоджують і обережно додають 0,5 мл 30%-ного розчину NaOH або аміаку. Забарвлення переходить в оранжеве.
Реакція на триптофан
При додаванні до білків гліоксалевої кислоти на межі з концентрованою сульфатною кислотою утворюється червоно-фіолетове кільце. Реакція зумовлена присутністю в молекулі білку триптофану, який, реагуючи з гліоксалевою кислотою (присутня у вигляді домішку в концентрованій оцтовій кислоті), дає забарвлені продукти конденсації. Концентрована сульфатна кислота приймає участь у реакції як водовіднімаючий агент.
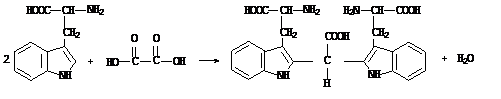
Хід роботи
У пробірку наливають 0,5 мл розчину білку. Потім додають 1 мл концентрованої оцтової кислоти і, нахиливши пробірку, уважно підшаровують 1 мл концентрованої сульфатної кислоти. Спостерігають утворення забарвленого кільця.
 2018-01-08
2018-01-08 1948
1948








