Результаты химического анализа веществ принято выражать процентным содержанием элементов, образующих исследуемое химическое соединение. Вычислить процентный состав сложного вещества - это определить процентное содержание каждого элемента, входящего а его состав.
Пример. Вычислить процентный состав едкого натра NaOH.
Решение:
Молекулярная масса NaOH равна 23+16+1=40.
1 моль=40 г.
Вычисляем процентное содержание натрия:

 ×100=57,5 (%).
×100=57,5 (%).
Вычисляем процентное содержание кислорода:
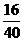 ×100=40 (%).
×100=40 (%).
Вычисляем процентное содержание водорода:
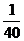 ×100=2,5 (%).
×100=2,5 (%).
Ответ: в едком натре содержится натрия - 57,5%, кислорода - 40% и водорода - 2,5%.
Задания:
1)Сколько азота содержится в: а) натриевой селитре NaNO3; б) сульфате аммония (NH4)2SO4; в) цианамиде кальция CaCN2? (Ответ: а)16,47%; б)21,21%; в)35%)
2)Сколько фосфора находится в: а) 1 кг костяной муки, содержащей 88% Ca3(PO4)2; б) 2 т фосфоритной муки, содержащей 82% Ca3(PO4)2; в) 0,5 т двойного суперфосфата, содержащего 92% Ca(H2PO4)2? (Ответ: а) 0,176 кг; б) 164кг; в) 50,34 кг.)
3)Вычислить процентный состав следующих веществ: а) едкого кали KOH; б) угольной кислоты H2CO3; в) сернистой кислоты H2SO3; г) хлористого хрома CrCl2; д) сернокислого кальция CaSO4; е) азотнокислого магния Mg(NO3)2; ж) сернокислого железа Fe2(SO4)3; з) Фосфорнокислого кальция Ca3(PO4)2; и) соды Na2CO3; к) известняка CaCO3. (Ответ: а)70,2%, 28,1%, 1,75%, б)3,22%, 19,35, 77,4%; в) 5,2%; 39%; 55,8%; г) 42,6%, 57,3%; д) 29,4%, к) 40%; 12%; 48%);
 2018-01-08
2018-01-08 2568
2568








