Квантово-механическая теория атома, построенная на уравнении Шредингера, гораздо совершеннее полу‑классичекой теории атома Бора, построенной на ряде постулатов. Она сохраняет некоторые аспекты старой теории – например, электроны могут находиться в атоме только в состояниях с определенной дискретной энергией; при переходе электрона из одного состояния в другое испускается (или поглощается) фотон. Но квантовая механика не просто дополняет теорию Бора, она рисует совершенно иную картину строения атома. Согласно квантовой механике, не существует определенных круговых орбит у электронов, как в теории Бора. В силу волновой природы электрон «размазан» в пространстве, т.е. может с определенной вероятностью находится в любой точке пространства.
При рассмотрении атома водорода, движение его единственного электрона можно рассматривать как движение в электрическом поле ядра. По аналогии с задачей о движении частицы в потенциальной яме простой формы, здесь необходимо найти решения стационарного уравнения Шредингера в трехмерном пространстве с конкретным видом потенциальной энергии, описывающем его электростатическое взаимодействие с ядром
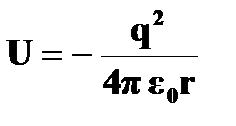 . (2.1)
. (2.1)
При решении уравнения Шредингера в данном случае используют специальные функции математической физики - сферические функции и сферическую систему координат, центр которой совпадает с центром ядра атома. Если записать уравнение Шредингера в сферических координатах (r, a, q), то его можно строго аналитически решить, это решение представляют в виде произведения трех функций
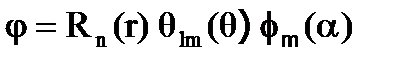 (2.2)
(2.2)
Важной особенностью решения является его зависимость от трех чисел n, l, m, называемых квантовыми числами. В квантовой механике каждому решению соответствует определенное состояние атома со своим распределением электрона вокруг ядра, которое задается соответствующей волновой функцией, зависящей от трех квантовых чисел: n, l, m.
Квантовое число n называется главным квантовым числом, от него зависит значение полной энергии атома водорода, при этом атом может иметь не любые значения энергии Е, а лишь некоторые Еn. Квантовое число n может принимать следующий ряд значений n = 1, 2, 3, … ¥. Значения энергии Еn, которые может иметь атом, называют разрешенными значениями энергии атома, а их совокупность Е1, Е2, … Е¥ представляет собой энергетический спектр атома. Разрешенные значения энергии обычно изображаются в виде горизонтальных линий, называемых энергетическими уровнями. Для атома водорода квантовая механика предсказывает точно такие же энергетические уровни, что и теория Бора, т.е.
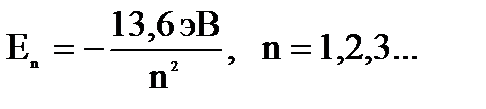 . (2.3)
. (2.3)
Состояние атома с наименьшей энергией называется основным (n = 1), все остальные состояния – возбужденными (см. рис.8).
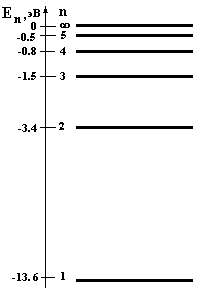
Рис.8. Схема энергетических уровней атома водорода.
Орбитальное квантовое число l связано с моментом импульса орбитального движения электрона вокруг ядра. Так как электрон имеет электрический заряд, то его движение вокруг ядра приводит к появлению магнитного момента, аналогичного магнитному моменту кругового витка с током. Орбитальное квантовое число l может принимать целочисленные значения от 0 до n -1, оно квантует величину момента импульса L и магнитного момента m согласно соотношениям
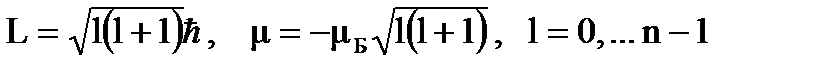 , (2.4)
, (2.4)
где mБ - постоянная, служащая единицей измерения магнитных моментов атомов и называемая магнетоном Бора. Сравнивая формулу квантования момента импульса с формулой квантования в теории Бора, можно заметить, что они не совпадают. Более того, при l=0, в квантовой механике возможны состояния атома с нулевым моментом импульса электрона. Опыт подтверждает существование квантовых состояний атома с нулевыми орбитальными моментами, хотя при классическом описании движения электрона в атоме по определенной орбите атом должен всегда обладать ненулевым моментом импульса.
Магнитное квантовое число m характеризует ориентацию момента импульса L и магнитного момента m во внешнем силовом поле (например, магнитном или электрическом) и может принимать целочисленные значения от –l до + l. Согласно классической теории магнитный момент всегда стремится повернуться вдоль направления магнитного поля. В квантовой механике движение электрона таково, что магнитный момент может быть направлен в нескольких, строго определенных направлениях в зависимости от состояния атома, то есть он квантуется не только по величине, но и по направлению. Такое пространственное квантование приводит к тому, что проекции момента импульса и магнитного момента электрона на выделенное в пространстве направление могут иметь только строго определенные значения. Ориентацию магнитного момента и момента импульса задают как и в классической физике, указывая его компоненту вдоль оси z, совпадающей с направлением магнитного поля. В квантовой механике возможные проекции Lz и mz определяются магнитным квантовым числом m с помощью соотношений
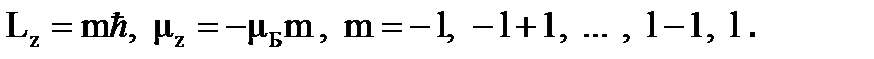 (2.5)
(2.5)
Так как формула квантования проекции механического момента соответствует вполне определенным направлениям ориентации в пространстве векторов L и m, то эту формулу называют обычно формулой пространственного квантования. С точки зрения классического представления об электронной орбите, эта формула определяет возможные дискретные расположения электронных орбит в пространстве по отношению к направлению внешнего поля. По отношению к другим координатам x и y положение векторов момента импульса L и магнитного момента m меняется так, как если бы они вращались вокруг оси z. Такое вращение называется прецессией (см. Рис. 9).
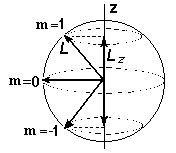
Рис. 9. Пространственное квантование момента импульса для состояния l=1 и траектории прецессии.
 2018-01-08
2018-01-08 811
811








