Основные понятия органической химии. Углерод выделяется среди всех элементов тем, что его атомы могут связываться друг с другом в длинные цепи или циклы. Именно это свойство позволяет углероду образовывать миллионы соединений, изучению которых посвящена целая область — органическая химия.
Современная теория строения молекул объясняет и огромное число органических соединений, и зависимость свойств этих соединений от их химического строения. Она же полностью подтверждает основные принципы теории химического строения,, разработанные выдающимся русским ученым А. М. Бутлеровым. (НЕ ФАКТ ЧТО ТО ЧТО НУЖНО).
Гибридизация (химия) — специфическое взаимодействие атомных орбиталей в молекулах.
Атомы (наименьшая возможная частица любого из простейших химических веществ, называемых элементами) состоят из ядер и электронов, которые вокруг них крутятся. Электроны - это не совсем корпускулы, но и волны тоже, поэтому они образуют своеобразные облака вокруг ядер атомов (некие пространства, в которых "обитают" электроны). Если облако одного электрона парекрывается с облаком другого, то может произойти гибридизация - электронные облака объединяются и два электрона начинают "обитать" в одном общем облаке. Поскольку эти электроны принадлежат разным атомам, атомы становятся связаными.
Гибридизация орбиталей — концепция смешения разных, но близких по энергии орбиталей данногоатома, с возникновением того же числа новых гибридных орбиталей, одинаковых по энергии и форме. Гибридизация атомных орбиталей происходит при возникновении ковалентной связи между атомами. Гибридизация орбиталей очень полезна при объяснении формы молекулярных орбиталей и является интегральной частью теории валентных связей.
Химические превращения высокомолекулярных соединений. Реакции деструкции полимеров. Виды деструкции.
Различают три вида реакций полимеров:
– реакции без изменения степени полимеризации (полимераналогичные превращения);
– реакции, приводящие к ее увеличению (структурирование, блок- и привитая сополимеризация);
– реакции, приводящие к уменьшению степени полимеризации (разрыв цепи при деструкции полимера).
Виды:
Химическая деструкция;
Окислительн6ая деструкция;
Окислительная деструкция наблюдается как у гетероцепных, так и у карбоцепных полимеров;
Деструкция под влиянием физических воздействий
Термическая деструкция
Фотохимическая деструкция
Деструкция под влиянием радиоактивного излучения. Под влиянием ионизирующих излучений полимеры претерпевают глубокие химические и структурные изменения, приводящие к изменению физико-химических и физико-механических свойств
Механохимическая деструкция
Билет № 5
1.Типы гибридизации атомных орбиталей в органических соединениях. sp3−, sp2−, sp− гибридизация.
Атомная орбиталь – это функция, которая описывает плотность электронного облака в каждой точке пространства вокруг ядра атома.
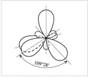 | 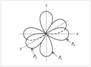 | |
| Четыре sp3-гибридные орбитали атома углерода | Форма и ориентация р-электронных орбиталей | |
 | ||
Образование  -связи -связи
|
Виды гибридизации
Sp-гибридизация
Происходит при смешивании одной s- и одной p-орбиталей. Образуется две равноценные sp-атомные орбитали, расположенные линейно под углом 180 градусов и направленные в разные стороны от ядра атома углерода. Две оставшиеся негибридные p-орбитали располагаются во взаимно перпендикулярных плоскостях и участвуют в образовании π-связей, либо занимаются неподелёнными парами электронов.
sp2-гибридизация
Происходит при смешивании одной s- и двух p-орбиталей. Образуется три гибридные орбитали с осями, расположенными в однойплоскости и направленными к вершинам треугольника под углом 120 градусов. Негибридная p-атомная орбиталь перпендикулярна плоскости и, как правило, участвует в образовании π-связей
sp3-гибридизация
Происходит при смешивании одной s- и трех p-орбиталей, образуя четыре равноценные по форме и энергии sp3-гибридные орбитали. Могут образовывать четыре σ-связи с другими атомами или заполняться неподеленными парами электронов.
Оси sp3-гибридных орбиталей направлены к вершинам правильного тетраэдра. Тетраэдрический угол между ними равен 109°28', что соответствует наименьшей энергии отталкивания электронов. Так же sp3-орбитали могут образовывать четыре σ-связи с другими атомами или заполняться неподеленными парами электронов.
 2018-01-21
2018-01-21 5400
5400

