Экспериментально была установлена формула скорости растворения твёрдого тела в жидкости:
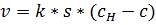
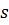 – площадь поверхности соприкосновения твёрдого тела с жидкостью;
– площадь поверхности соприкосновения твёрдого тела с жидкостью;
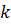 – константа при данных условиях;
– константа при данных условиях;
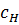 - концентрация насыщенного раствора вблизи границы раздела фаз;
- концентрация насыщенного раствора вблизи границы раздела фаз;
 - концентрация растворяющегося раствора в глубине объёма жидкой фазы;
- концентрация растворяющегося раствора в глубине объёма жидкой фазы;
Скорость растворения тем больше, чем больше площадь поверхности твёрдого тела и разность концентраций. Нернстом было предложено, что жидкость возле поверхности твёрдого тела образует диффузионный слой, за пределами которого при условии постоянного перемешивания концентрация растворённого вещества постоянна. При чём скорость растворения твёрдого тела будет больше скорости диффузии, следовательно, вблизи поверхности тела раствор близок к насыщенному.
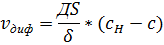

Процесс растворения газа в жидкости по сравнению с твёрдым телом имеет ряд особенностей:
Около поверхности раздела фаз возникает два диффузионных слоя:
- Первый: расположен в газовой фазе обеспечивает подвод к поверхности жидкости молекул газа;
- Второй: слой обеспечивает переход молекул газа в глубину объёма жидкой фазы;
В зависимости от соотношения скоростей диффузии в этих слоях суммарный процесс может лимитироваться процессом, протекающим в одном из слоёв или в двух слоях одновременно.
Растворение:
ü Газ хорошо растворим: градиент концентрации в газовой фазе обеспечивает предельную скорость диффузии, которая может быть увеличена за счёт перемешивания газовой фазы.
ü Газ плохо растворим: предельное значение достигает градиент концентрации в жидкой фазе, и суммарный процесс будет минимизироваться диффузией в жидкой фазе.
Диффузия у поверхности раздела фаз будет зависеть от системы поверхности, т.к. кроме внешней диффузии, протекает и внутренняя диффузия в порах поверхности тела. Характер внутренней диффузии зависит от размера пор, формы и количества.
 2018-01-21
2018-01-21 537
537








