Данный вид осложняется тем, что присутствует растворитель, который может так же, как и растворённое вещество адсорбироваться твёрдым телом. Если растворитель плохо смачивает поверхность, то адсорбция будет достаточно большой величиной.
Существует два вида веществ:
1. Гидрофильные – хорошо смачиваются водой, лучше адсорбируют из неполярных растворителей (силикагель, алюмогель, глина и т.д.);
2. Гидрофобные – лучше адсорбируют из полярных растворителей (активированный уголь).
При адсорбции из жидкости возможны два случая: адсорбция молекул неэлектролитов и электролитов.
Адсорбция неэлектролитов идёт медленнее адсорбции газов, т.к. изменение концентрации происходит из-за диффузионных процессов.
Вещество В может адсорбироваться на границе фаз А/С, если будет уравнением полярности этих двух фаз. Полярность можно характеризовать величиной 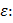
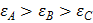
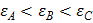
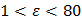
Все предельные одноосновные кислоты имеют одинаковое значение поверхностного натяжения, но с увеличением длины радикала их адсорбируемость на твёрдом адсорбенте различна. Из водных растворов на гидрофобных адсорбатах, оно растёт.
Из неполярных растворителей на гидрофильных адсорбатах адсорбируемость убывает. выравнивание полярности фаз адсорбента и среды будет происходить при определенной ориентации ПАВ на границе раздела фаз.
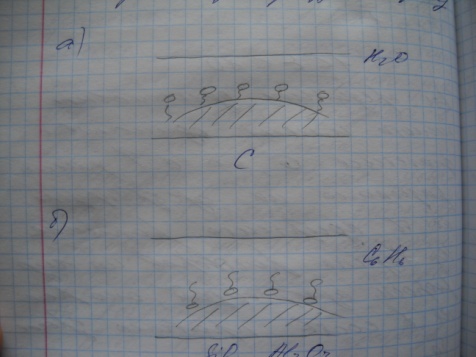
Молекулярная адсорбция из растворов может быть описана уравнением Лангмюра:
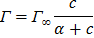
За счёт адсорбции ПАВ из растворов можно изменить природу твёрдой поверхности. Если гидрофильную поверхность обработать водным раствором одноосновной кислоты, то её молекулы ориентируются полярными группами к поверхности – поверхность становится гидрофобной.

 2018-01-21
2018-01-21 263
263








