Аккумуляторы – устройства, в которых электрическая энергия превращается в химическую, а химическая – в электрическую.
Электрическая энергия  химическая энергия
химическая энергия
Аккумуляторы:
· Кислотные (свинцовый),
· Щелочные ( )
)
Аккумуляторы состоят из электродов: катода (восстановление) и анода (окисление) и ионного проводника.
При зарядке аккумулятор работает как электролизёр, а при разрядке – как гальванический элемент.
Свинцовый аккумулятор. Состоит из двух перфорированных электродов, покрытых слоем PbO и погружённых в раствор  .
.
 .
.
Процессы при разрядке:
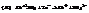 ,
,
 .
.
Процессы при зарядке:
 ,
,
 .
.
Суммарная реакция:
 .
.
Щелочной аккумулятор (кадмиеникилевый). Состоит из кадмиевого электрода (катода) и электрода из  . Электролит – КОН.
. Электролит – КОН.
Суммарная реакция:
 .
.
№9.
Коррозия металлов. Виды коррозии. Химическая коррозия.
Коррозия металлов – это процесс самопроизвольного разрушения металлов под воздействием окружающей среды. Причиной является термодинамическая неустойчивость металлов в атмосферных условиях и других средах.
 ,
,  ;
;
 ,
,  ;
;
Коррозия: химическая, электрохимическая.
Химическая коррозия.
Окислительно-восстановительный процесс, в котором процессы окисления и восстановления протекают в одной точке без электролита и без возникновения электрического тока.
По характеру взаимодействия химическая коррозия подразделяется на:
1) в атмосфере сухих газов  :
:
 ,
,
2) в растворах сухих неэлектролитов:

 .
.
Коррозия осуществляется либо по всей поверхности (сплошная), либо в определённых точках (питтинговая), либо между отдельными кристаллами (язвенная).
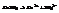 №10.
№10.
 2018-01-21
2018-01-21 608
608








