При определении потенциалов металлов используют металлический проводник с электронной проводимостью и проводник с ионной проводимостью. Раствор KCl служит для устранения диффузионного потенциала, возникающего на границе двух растворов. Гальванометр показывает величину стандартного потенциала.
Электроны от цинковой пластины идут к водородному электроду, и потенциал равняется 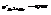 при
при  ,
, 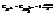 . Если электроны идут к металлической пластинке, то потенциал положительный:
. Если электроны идут к металлической пластинке, то потенциал положительный:
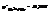
№5.
Ряд стандартных потенциалов металлов.
Металлы, расположенные в порядке возрастания стандартных электродных потенциалов, образуют ряд напряжений.
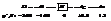
1) В начале ряда расположены активные восстановители (щелочные и щелочноземельные металлы).
2) Металлы, стоящие в ряду напряжений левее, восстанавливают из солей ионы металлов, стоящие за ними.
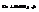 ,
,
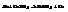 , т.к. Fe левее.
, т.к. Fe левее.
3) Металлы, стоящие в ряду напряжений до Н, вытесняют водород из разбавленных кислот.
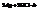
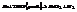
4) Металлы, стоящие в ряду напряжений до и после Н, взаимодействуют с серной и азотной концентрированными кислотами.
5) Чем дальше друг от друга расположены металлы, тем большее значение будет иметь напряжение гальванического элемента, составленного из этих металлов.
№6.
 2018-01-21
2018-01-21 569
569








