С)5 и 6
$$$ 35
Укажите ряд элементов, расположенных в порядке возрастания электроотрицательности.
А)Ca, Cl, Se, Al;
В)Na, H, N, F;
С)K, N, F, Mg;
D)P, Se, O, Ca;
Е)O, Br, I, H.
$$$ 36
Количественная характеристика способности атома в молекуле притягивать к себе электроны называется:
D)сродством к электрону
$$$ 37
Реакция ионного обмена идет до конца при взаимодействии
А) AI(NO3)3 и KCI;
B) CuSO4 и Zn(NO3)2;
C) NaCI и LiNO3;
D) HCI и Na2CO3;
E) KOH и NaOH.
$$$ 38
Какая из приведенных электронных формул соответствует иону фосфора Р3-.
S2 3p6
$$$ 39
При сжигании 2 моль водорода образуется вода в количестве (моль)
$$$ 40
Квантовое число, определяющее ориентацию электронного облака в пространстве называется:
Орбитальное
$$$ 41
В 100 мл раствора содержится 4,9 г Н2SO4 (M(Н2SO4)=98 г/моль). Какова нормальность раствора (моль/л)?
1)0.5
$$$ 42
Определите эквивалентную концентрацию (моль/л) раствора HNO3, содержащего 6,3 г HNO3 в 100 мл раствора.
1)0.003
$$$ 43
Определите объём (при н.у.), занимаемый 6,8 г сероводорода.
$$$ 44
Вычислите рОН 0,01М раствора HNO3.
1) 10
$$$ 45
Вычислите рН 0,01М раствора КОН.
1)2
$$$ 46
Укажите соль, раствор которой имеет щелочную среду.
А)K2SO4;
В)K2CO3;
С)MgSO4;
D)CuCl2;
Е)NaNO3.
$$$ 47
Укажите соль, не подвергающуюся гидролизу.
А)KNO3;
В)K2S;
С)MgSO4;
D)AlCl3;
Е)Na2CO3.
$$$ 48
В результате гидролиза какой соли образуется основная соль?
А)CsCl;
В)Ba(NO3)2;
С)FeCl3;
D)K2S;
Е)Na2CO3.
$$$ 49
Определите титр 0,25Н раствора NaOH
1). 0.01
$$$ 50
Укажите слабый электролит.
А)HNO3;
В)NaOH;
С)Al(OH)3;
D)Na2SO4;
Е)KCl.
$$$ 51
Раствор, содержащий 8 г некоторого вещества в 100 г диэтилового эфира, кипит при 36,860С, тогда как чистый эфир кипит при 35,600С. Определить молекулярную массу растворенного вещества. Е(эфира)=2,020С.
1)20.5
$$$ 52
При полной диссоциации Na3PO4 образуется ионов:
1)4
$$$ 53
В результате гидролиза какой соли образуется кислая соль?
А)KNO3;
В)CuSO4;
С)NiCl2;
D)K2S;
Е)Na2SO4.
$$$ 54
Вычислите массовую долю (%) соли в растворе, содержащем 50 г соли и 200 г воды.
1)20
$$$ 55
Какую массу NaNO3 нужно растворить в 400 г воды, чтобы приготовить 20%-ный раствор?
1)100
$$$ 56
Укажите раствор какой соли при гидролизе имеет щелочную среду рН>7
А)CuSO4+HOH®¼
В)MgCl2+HOH®¼
С)KNO3+HOH®¼
D)CH3COONa+HOH®¼
Е)Na2SO4+HOH®¼
$$$ 57
В 100 мл раствора содержится 49 г H2SO4. Какова нормальность раствора (моль/л)?
1)10
$$$ 58
Гидролиз какой соли идет в три ступени?
А)CrCl3;
В)(NH4)2SO4;
С)NaCN;
D)K2S;
Е)Zn(NO3)2.
$$$ 59
Укажите раствор какой соли при гидролизе имеет кислую среду (рН<7).
А)Na2CO3;
В)K2SO4;
С)CuCl2;
D)NaCl;
Е)FeS.
$$$ 60
Если рОН раствора равен 3, то чему равна концентрация ионов водорода?
1) 10-11
$$$ 61
Определить температуру кипения раствора (0С), содержащего 3,46 г мочевины CO(NH2)2 ( = 60г/моль) в 100 г воды. Эбулиоскопическая константа воды равна 0,520.
= 60г/моль) в 100 г воды. Эбулиоскопическая константа воды равна 0,520.
1) 55.5
$$$ 62
В 100 мл раствора содержится 3,4 г AgNO3. M(AgNO3)=170 г/моль. Какова нормальность раствора (моль/л)?
1) 0.2
$$$ 63
Какой газ выделяется при совместном конечном гидролизе солей в реакции: AlCl3+Na2CO3+HOH®…
3) CO2
$$$ 64
В растворе какой соли рН будет наибольшим?
А)K2CO3;
В)Al(NO3)3;
С)FeCl3;
D)Cu(CH3COO)2;
Е)ZnSO4.
$$$ 65
Рассчитать, при какой температуре должен кристаллизоваться раствор, содержащий в 250 г воды 54 г глюкозы С6Н12О6. Криоскопическая константа воды равна 1,860.
$$$ 66
Азот объемом 11,2 л имеет массу (н.у.):
1) 14 г
$$$ 67
Каково математическое выражение ПР сульфата кальция?
1) 6,10*10-5
$$$ 68
Раствор массой 120 г содержит 24 г гидроксида калия (КОН). Какова массовая доля вещества в растворе (w, %)?
1) 20%
$$$ 69
Нормальная концентрация раствора (моль/л), содержащего 10,5 г фтористого натрия (M(NaF)=42г/моль) в 250 мл водного раствора равна:
1) 1 нормальный
$$$ 70
Укажите сильный электролит.
А)H2CO3;
В)H3PO4;
С)NaNO3;
D)Cu(OH)2;
Е)H2S.
$$$ 71
Из 400 г 50%-ного (по массе) раствора H2SO4 выпариванием удалили 100 г воды. Чему равна массовая доля (%) H2SO4 в оставшемся растворе?
1)66.7
$$$ 72
При какой температуре должен кипеть раствор, содержащий растворенный неэлектролит количеством вещества 0,062 моль в воде объёмом 200 мл? Эбулиоскопическая константа воды равна 0,520.
$$$ 73
Раствор массой 125 г содержит 25 г гидроксида натрия (NaOH). Какова массовая доля вещества в растворе (w, %)?
1) 20%
$$$ 74
Если рН раствора равен 6, то чему равна концентрация ионов водорода в этом растворе?
1) [H+]=10-6
$$$ 75
Вычислить осмотическое давление раствора, содержащего 16 г сахарозы (С12Н22О11) в 350 г Н2О при 293 К. Плотность раствора считать равной единице.
КПА
$$$ 76
Какой массы сахароза (С12Н22О11) находится в растворе объёмом 200 мл, если осмотическое давление этого раствора при 00С равно 6,61×105 Па?
$$$ 77
В 1 л раствора содержится 5,85 г NaCI (М(NaCI)=58,5 г/моль). Чему равна молярная концентрация раствора?
1)0.1
$$$ 78
При растворении 5,0 г вещества в 200 г воды получается не проводящий тока раствор, кристаллизующийся при –1,450С. Определить молекулярную массу растворенного вещества (г/моль). Криоскопическая константа воды равна 1,860.
1)32
$$$ 79
Отношение количества растворенного вещества к массе растворителя называется …концентрация;
1) Моляльная концентрация
$$$ 80
Отношение числа эквивалентов растворенного вещества к объему раствора называется …концентрация.
Нормальной
$$$ 81
Как надо изменить концентрацию ионов водорода в растворе, чтобы рН раствора увеличился на единицу?
1) Уменьшить в 10 раз
$$$ 82
В растворе какого электролита можно обнаружить хлорид ион?
А)NaClO;
В)NaCl;
С)NaClO3;
D)NaClO2;
Е)NaClO4.
$$$ 83
При диссоциации какого электролита образуется гидроксокатион?
А)CuSO4;
В)NaHCO3;
С)Al(Ac)3;
D)CuOHCl;
Е)NaH2PO4.
$$$ 84
При диссоциации какого электролита образуется гидроанион?
А)AlOHCl2;
В)Na2SO4;
С)NH4OH;
D)(CuOH)2SO4;
Е)Na2HPO4.
$$$ 85
На сколько градусов повысится температура кипения раствора сахара, если в 200 г Н2О растворить 40 г сахара (С12Н22О11). (М(С12H22O11)=342 г/моль). Е(Н2О)=0,520.
$$$ 86
На сколько градусов понизится температура замерзания раствора глицерина, если в 100 г Н2О растворить 10 г глицерина (С3Н8О3). (М(С3Н8O3)=92 г/моль). К(Н2О)=1,860С.
1) 2,02 0C
$$$ 87
Какая из солей не подвергается гидролизу?
А)K2CO3;
В)NH4Cl;
С)Na2SO4;
D)(NH4)2S;
Е)FeCl3.
$$$ 88
Укажите раствор какой соли при гидролизе имеет нейтральную реакцию среды, т.е. рН=7?
А)NaHCO3;
В)NH4CN;
С)Cu(NO3)2;
D)K2S;
Е)AlCl3.
$$$ 89
Укажите вещество электролит.
А)Cu;
В)CuO;
С)O2;
D)CuSO4;
Е)NO.
$$$ 90
Укажите вещество неэлектролит.
А)ZnCl2;
В)Na2SO4;
С)CrCl3;
D)MnO;
Е)Cu(NO3)2.
$$$ 91
Какая из указанных кислот в равных условиях, дает наименьшую концентрацию ионов водорода Н+.
А) HClO2 Kд=1×10-2;
В) HClO Kд=2,95×10-8;
С) HClO3 Kд=1×103;
D) HClO4 Kд=1×108;
Е) HCl Kд=1×108,9.
$$$ 92
Укажите сильный электролит.
А)HNO3 a=94 %;
В)СН3СОOH a= 2 %;
С)НCN a=0,15 %;
D)NH4OH a=1,35 %;
Е)H2CO3 a=0,17 %.
$$$ 93
Какой электролит диссоциирует ступенчато? H2SO4
А)KCN;
В)H2SO3;
С)NaOH;
D)KNO3;
Е)HCl.
$$$ 94
Какая реакция идет с образованием нерастворимого соединения?
А)Ni(OH)2+HNO3®…
В)CaCO3+HCl®…
С)Zn(OH)2+NaOH®…
D)FeCl3+NaOH®…
Е)H2SO4+KOH®…
$$$ 95
Какая реакция имеет краткое ионное уравнение Н++ОН-=Н2О?
А)CH3COOH+Ca(OH)2®…
В)H2CO3+KOH®…
С)HNO3+NaOH®…
D)H2SO4+Cu(OH)2®…
Е)HCl+NH4OH®…
$$$ 96
Какая реакция идет с образованием газообразного вещества?
А)CaCO3+HCl®…
В)Na2SiO3+HCl®…
С)Na2SO4+BaCl2®…
D)NH4Cl+AgNO3®…
Е)H2CO3+Ca(OH)2®…
$$$ 98
Какое вещество проявляет только окислительные свойства?
А)MnO;
В)MnO2;
С)K2MnO4;
D)KMnO4;
Е)MnCl2.
$$$ 99
Какое вещество проявляет только восстановительные свойства?
А)S;
В)H2SO3;
С)H2S;
D)H2SO4;
Е)Na2SO3.
$$$ 100
Укажите соединение, содержащее ион в степени окисления “+4”.
А)Zn(OH)2;
В)HClO3;
С)KNO2;
D)Na2SO3;
Е)PbS.
$$$ 101
Вычислите массовую долю (%) соли в растворе, содержащем 50 г соли и 200 г воды.
1)20
$$$ 102
Какую массу NaNO3 нужно растворить в 400 г воды, чтобы приготовить 20%-ный раствор?
1)100
$$$ 103
Определите, раствор какой соли при гидролизе имеет щелочную среду (рН>7).
А)CuSO4+HOH®¼
В)MgCl2+HOH®¼
С)KNO3+HOH®¼
D)CH3COONa+HOH®¼
Е)Na2SO4+HOH®¼
$$$ 104
В 100 мл раствора содержится 49 г H2SO4. Какова нормальность раствора (моль/л)?
1)10
$$$ 105
Гидролиз какой соли идет в три ступени?
А)CrCl3
В)(NH4)2SO4
С)NaCN
D)K2S
Е)Zn(NO3)2
$$$ 106
Определите, раствор какой соли при гидролизе имеет кислую среду (рН<7).
А)Na2CO3
В)K2SO4
С)CuCl2
D)NaCl
Е)FeS
$$$ 107
Если рОН раствора равен 3, то чему равна концентрация ионов водорода?
1) 10-11
$$$ 108
Определите температуру кипения раствора (0С), содержащего 3,46 г мочевины ( = 60г/моль) в 100 г воды. Эбулиоскопическая константа воды равна 0,520.
= 60г/моль) в 100 г воды. Эбулиоскопическая константа воды равна 0,520.
1) 55.5
$$$ 109
В 100 мл раствора содержится 3,4 г AgNO3. M(AgNO3)=170 г/моль. Какова нормальность раствора (моль/л)?
1)0.2
$$$ 110
Какой газ выделяется при совместном конечном гидролизе солей в реакции: AlCl3+Na2CO3+HOH®…
1) CO2
$$$ 111
В растворе какой соли рН будет наибольшим?
А)K2CO3
В)Al(NO3)3
С)FeCl3
D)Cu(CH3COO)2
Е)ZnSO4
$$$ 112
Рассчитать, при какой температуре должен кристаллизоваться раствор, содержащий в 250 г воды 54 г глюкозы С6Н12О6. Криоскопическая константа воды равна 1,860.
$$$ 113
Азот объемом 11,2 л имеет массу (н.у.):
1) 14 г
$$$ 114
Каково математическое выражение ПР хлорида свинца?
$$$ 115
Раствор массой 120 г содержит 24 г гидроксида калия. Какова массовая доля вещества в растворе (w, %)?
1) 20 %
$$$ 116
Нормальная концентрация раствора (моль/л), содержащего 10,5 г фтористого натрия (M(NaF)=42г/моль) в 250 мл водного раствора равна:
1) 1 нормальный
$$$ 117
Укажите сильный электролит.
А)H2CO3
В)H3PO4
С)NaNO3
D)Cu(OH)2
Е)H2S.
$$$ 118
Из 400 г 50%-ного (по массе) раствора H2SO4 выпариванием удалили 100 г воды. Чему равна массовая доля (%) H2SO4 в оставшемся растворе?
1) 66.7
$$$ 119
При какой температуре должен кипеть раствор, содержащий растворенный неэлектролит количеством вещества 0,062 моль в воде объёмом 200 мл? Эбулиоскопическая константа воды равна 0,520.
$$$ 120
Раствор массой 125 г содержит 25 г гидроксида натрия. Какова массовая доля вещества в растворе (w, %)?
1) 20%
$$$ 121
Если рН раствора равен 6, то чему равна концентрация ионов водорода в этом растворе?
1) [H+]=10-6
$$$ 122
Вычислить осмотическое давление раствора, содержащего 16 г сахарозы (С12Н22О11) в 350 г Н2О при 293 К. Плотность раствора считать равной единице.
$$$ 123
Какой массы сахароза (С12Н22О11) находится в растворе объёмом 200 мл, если осмотическое давление этого раствора при 00С равно 6,61×105 Па?
$$$ 124
В 1 л раствора содержится 5,85 г NaCI (М(NaCI)=58,5 г/моль). Чему равна молярная концентрация раствора?
1) 0.1 м
$$$ 125
При растворении 5,0 г вещества в 200 г воды получается не проводящий тока раствор, кристаллизующийся при  . Определить молекулярную массу растворенного вещества (г/моль). Криоскопическая константа воды равна 1,860.
. Определить молекулярную массу растворенного вещества (г/моль). Криоскопическая константа воды равна 1,860.
$$$ 126
Отношение количества растворенного вещества к массе растворителя называется:
1) Моляльная концентрация
$$$ 127
Отношение количества эквивалентов растворенного вещества к объему раствора называется:
$$$ 128
Как надо изменить концентрацию ионов водорода в растворе, чтобы рН раствора увеличился на единицу?
1) Уменьшить в 10 раз
$$$ 129
В растворе какого электролита можно обнаружить хлорид ион?
А)NaClO
В)NaCl
С)NaClO3
D)NaClO2
Е)NaClO4
$$$ 130
При диссоциации какого электролита образуется гидроксокатион?
А)CuSO4
В)NaHCO3
С)Al(Ac)3
D)CuOHCl
Е)NaH2PO4
$$$ 131
При диссоциации какого электролита образуется гидроанион?
А)AlOHCl2
В)Na2SO4
С)NH4OH
D)(CuOH)2SO4
Е)Na2HPO4
$$$ 132
На сколько градусов повысится температура кипения раствора сахара, если в 200 г Н2О растворить 40 г сахара (С12Н22О11). М(С12H22O11)=342 г/моль, Е(Н2О)=0,520.
1)5
$$$ 133
На сколько градусов понизится температура замерзания раствора глицерина, если в 100 г Н2О растворить 10 г глицерина (С3Н8О3). М(С3Н8O3)=92 г/моль, К(Н2О)=1,860.
1)7
$$$ 134
Какая из солей не подвергается гидролизу?
А)K2CO3
В)NH4Cl
С)Na2SO4
D)(NH4)2S
Е)FeCl3
$$$ 135
Определите, раствор какой соли при гидролизе имеет нейтральную реакцию среды, т.е. рН=7?
А)NaHCO3
В)NH4CN
С)Cu(NO3)2
D)K2S
Е)AlCl3
$$$ 136
Укажите вещество электролит.
А)Cu
В)CuO
С)O2
D)CuSO4
Е)NO
$$$ 137
Укажите вещество неэлектролит.
А)ZnCl2
В)Na2SO4
С)CrCl3
D)MnO
Е)Cu(NO3)2
$$$ 138
Какая из указанных кислот в равных условиях, дает наименьшую концентрацию ионов водорода (Н+)?
А)HClO2 Kд=1×10-2
В)HClO Kд=2,95×10-8
С)HClO3 Kд=1×103
D)HClO4 Kд=1×108
Е)HCl Kд=1×108,9
$$$ 139
Укажите сильный электролит.
А)HNO3 a=94 %
В)СН3СОOH a= 2 %
С)НCN a=0,15 %
D)NH4OH a=1,35 %
Е)H2CO3 a=0,17 %
$$$ 140
Какой электролит диссоциирует ступенчато? H2SO4
А)KCN
В)H2SO3
С)NaOH
D)KNO3
Е)HCl
$$$ 141
Какая реакция идет с образованием нерастворимого соединения?
А)Ni(OH)2+HNO3®…
В)CaCO3+HCl®…
С)Zn(OH)2+NaOH®…
D)FeCl3+NaOH®…
Е)H2SO4+KOH®…
$$$ 142
Какая реакция имеет краткое ионное уравнение Н++ОН-=Н2О?
А)CH3COOH+Ca(OH)2®…
В)H2CO3+KOH®…
С)HNO3+NaOH®…
D)H2SO4+Cu(OH)2®…
Е)HCl+NH4OH®…
$$$ 143
Какая реакция идет с образованием газообразного вещества?
А)CaCO3+HCl®…
В)Na2SiO3+HCl®…
С)Na2SO4+BaCl2®…
D)NH4Cl+AgNO3®…
Е)H2CO3+Ca(OH)2®…
$$$ 144
Какое вещество проявляет только окислительные свойства?
А)MnO
В)MnO2
С)K2MnO4
D)KMnO4
Е)MnCl2
$$$ 145
Какое вещество проявляет только восстановительные свойства?
А)S
В)H2SO3
С)H2S
D)H2SO4
Е)Na2SO3
$$$ 146
Определите соединение, содержащее ион в степени окисления “+4”.
А)Zn(OH)2
В)HClO3
С)KNO2
D)Na2SO3
Е)PbS
$$$ 147
Рассчитайте массу 3,01×1023 молекул сульфата меди(II).
$$$ 148
У какого элемента металлические свойства выражены сильнее?
1) Na E0=-2,71
$$$ 149
В результате окисления ОН- гидроксид-ионов, какой газ выделяется на аноде?
1) O2
$$$ 150
У какого из металлов образуется на поверхности плотная оксидная защитная пленка?
Al
$$$ 151
В каких массовых отношениях надо смешать два раствора с массовой долей растворенного вещества 10 и 40%, чтобы получить 20% раствор?
$$$ 152
Ток силой 6 А пропускали через водный раствор серной кислоты в течение 1,5ч. Вычислить массу разложившейся воды.
$$$ 153
В кристаллическом состоянии атомы металлов связаны…связью
1) металлической связью
$$$ 154
В каком ряду записаны только амфотерные гидроксиды?
А)Mn(OH)2, Cu(OH)2, Mg(OH)2
В)Be(OH)2, Zn(OH)2, Cr(OH)3
С)Co(OH)3, Fe(OH)3, Al(OH)3
D)KOH, NH4OH, LiOH
Е)NaOH, AgOH, AuOH
$$$ 155
Какое уравнение соответствует образованию основной соли?
А)Zn(OH)2+HNO3®¼
В)KOH+H2SO4®¼
С)NH4OH+H2S®¼
D)NaOH+HCN®¼
Е)LiOH+H3PO4®¼
$$$ 156
Какое уравнение соответствует образованию кислой соли
А)KOH+HNO3®¼
В)HCl+Fe(OH)3®¼
С)Cr(OH)3+CH3COOH®¼
D)NaOH+H2SO3®¼
Е)Ca(OH)2+HCl®¼
$$$ 157
Укажите вещество, взаимодействующее с NaOH с образованием воды:
А)K2SO4
В)HCl
С)Ba(OH)2
D)KNO3
Е)KOH
$$$ 158
Укажите вещество, с которым будет взаимодействовать гидроксид натрия:
А)K2O
В)SO3
С)CaO
D)BaO
Е)Li2O
$$$ 159
Укажите реакцию образования гидроксида бериллия:
А)BeCl2+AgNO3®¼
В)BeO+H2SO4®¼
С)Be(NO3)2+Ca(OH)2®¼
D)BeSO4+BaCl2®¼
Е)BeCO3+HCl®¼
$$$ 160
Какая из перечисленных солей основная?
А)K2SO4
В)BaCl2
С)NaHCO3
D)Al2(SO4)3
Е)MgOHCl
$$$ 161
В каком ряду увеличивается основной характер оксидов:
А)As2O3®BiO3®Sb2O3
В)CaO®CrO®CuO
С)CaO®SrO®BaO
D)Cs2O®BaO®CdO
Е)MnO®MnO3®Mn2O7
$$$ 162
Какой оксид при взаимодействии с водой образует кислоту?
А)SO2
В)FeO
С)MnO
D)K2O
Е)Co2O3
$$$ 163
Какой оксид растворяется в воде с образованием основания?
А)SiO2
В)Na2O
С)MoO3
D)Cl2O3
Е)P2O5
$$$ 164
Какая из перечисленных солей называется дигидроортофосфат калия?
1) KH2PO4
$$$ 165
Как называется соль (MnOH)2SO3?
1) Гидроксосульфит марганца
$$$ 166
Какую плотность по воздуху имеет газовая смесь, состоящая из азота, водорода и аммиака, если объёмные доли этих газов соответственно равны 30, 10, и 60%?
$$$ 167
Какое взаимодействие приведет к получению нормальной соли магния из гидроксохлорида магния?
А)MgOHNO3+HCl®¼
В)MgOHCl+HCl®¼
С)(MgOH)2SO4+HNO3®¼
D)MgOHCl+NaOH®¼
Е)MgCl2+KOH®¼
$$$ 168
Докажите амфотерность свинца, дописав уравнение реакции:
Pb(OH)2+2KOH=…+2H2O
1) K2PbO2
$$$ 169
Укажите основной оксид.
А)BaO
В)Cr2O3
С)SO2
D)Mn2O7
Е)SiO2
$$$ 170
Укажите кислотный оксид.
А)Cr2O3
В)CO2
С)Fe2O3
D)K2O
Е)PbO2
$$$ 171
Укажите амфотерный оксид.
А)CaO
В)Al2O3
С)SiO2
D)B2O3
Е)SO2
$$$ 172
Определите реакцию образования силиката кальция.
А)Ca(OH)2+HNO3®…
В)Ca(OH)2+SiO2®…
С)CaO+P2O5®…
D)Ca(OH)2+H2SO4®…
Е)Ca(OH)2+CO2®…
$$$ 173
Определите реакцию образования угольной кислоты.
А)CuSO4+Ca(OH)2®…
В)CaCl2+AgNO3®…
С)CaO+H2SO4®…
D)CaCO3+HCl®…
Е)Na2CO3+CaCl2®…
$$$ 174
Определите реакцию образования оксида железа(III).
А)FeCl3+NaOH®…
В)Fe(OH)3+H2SO4®…
С)Fe(OH)3  …
…
D)Fe(OH)3+NaOH®…
Е)Fe2(SO4)3+CaCl2®…
$$$ 175
Определите ряд веществ, с которыми реагируют основания.
А)SO3, H2SO4, Zn(OH)2
В)Ba(OH)2, КNO3, Cl2O7
С)H3BO3, HCl, KOH
D)Be(OH)2, HCl, Na2O
Е)N2O5, NH4OH, Cs2O
$$$ 176
В результате какой из реакций нельзя получить соль?
А)соль+основание®…
В)основной оксид+кислота®…
С)кислотный оксид+основание®…
D)кислотный оксид+вода®…
Е)щелочной металл+кислота®…
$$$ 177
Укажите формулу, с помощью которой можно привести объем газа к нормальным условиям.
1) PV/T=P0V0/T0
$$$ 178
Объем (л), занимаемый 0,5 моль водорода при н.у.:
1) 11,2
$$$ 179
Какая формула выражает закон эквивалентов?
1) m1/m2=Mэ1/Mэ2
$$$ 180
Какое количество вещества (моль) находится в 11,2 л оксида углерода(IV) CO2 при нормальных условиях?
1)0.5
$$$ 181
Укажите формулу, с помощью которой можно определить молярный объем:
1) V=v*Vm
$$$ 182
Для обнаружения ионов Fe2+ и Fe3+ используют:
А)раствор перманганата калия
В)соляную кислоту
С)гидроксид калия
D)лакмус
Е)карбонат натрия
$$$ 183
Какова молярная масса газа, если его относительная плотность по воздуху равна 1,5. Мвозд.=29 г/моль.
1) 43,5
$$$ 184
Какое выражение, соответствующее уравнению скорости для гомогенной реакции 2NO(г)+O2(г) ® 2NO2(г) является правильным?
$$$ 185
Какое выражение, соответствующее уравнению скорости для гетерогенной реакции S(к)+O2(г)® SO2(г) является верным?
$$$ 186
Чему равна молярная масса эквивалента (г/моль) фосфорной кислоты (М(Н3РО4)=98г/моль) в реакции: Н3РО4+Са(ОН)2=СаНРО4+2Н2О?
$$$ 187
Плотность газа по воздуху равна 2,2. Какова относительная молекулярная масса газа? Мвозд=29 г/моль.
1)64
$$$ 188
Что принимается за единицу количества вещества в системе СИ?
Моль
$$$ 189
Как правильно сказать: “1 моль вещества содержит”:
А)6,02×1023 молекул
В)6,02×1023 структурных единиц
С)6,02×1023 ионов
D)6,02×1023 электронов
Е)6,02×1023 атомов
$$$ 190
Какова размерность молярной массы эквивалента вещества Х (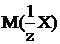 ).
).
1) Г/моль
$$$ 191
Определите значения эквивалентных объемов водорода и кислорода при н.у.
$$$ 192
Определите количество молей в 56 г N2 при н.у.
1) 2,0
$$$ 193
Определите, в каком случае содержится больше молекул при н.у.
А)10 г N2
В)10 г O2
С)10 г SO3
D)10 г NH3
Е)10 г SO2
$$$ 194
Укажите значение универсальной газовой постоянной.
1) R=8.314 дж/моль*К
$$$ 195
Укажите молярный объем газа при нормальных условиях.
Л/моль
$$$ 196
Определите значение молярной массы эквивалента гидроксида кальция.
$$$ 197
Определите, какое вещество имеет наименьшее значение молярной массы эквивалента.
А)H3PO4
В)CaCl2
С)O2
D)HCl
Е)KOH
$$$ 198
Определите, какое вещество имеет наибольшее значение молярной массы эквивалента.
А)H2SO4
В)НCl
С)Н3РО4
D)NaОН
Е)Fe(OH)3
$$$ 199
Определите массу (г) серной кислоты количеством 0,5 моль. М(H2SO4)=98г/моль.
$$$ 200
Какой объем (л) при нормальных условиях займет аммиак массой 34 г.
$$$ 201
Укажите формулу, выражающую закон эквивалентов.
$$$ 202
Определите число молекул в 3,4 г сероводорода.
$$$ 203
Определите молярную массу газа (г/моль), если 11 г этого газа занимает объем 5,6л при н.у.
$$$ 204
Определите массу (г) и число молекул, содержащихся в 2 молях фтороводорода.
$$$ 205
Укажите значение постоянной Авогадро.
1) 6,02*1023 моль-1
$$$ 206
Чему равен температурный коэффициент скорости реакции, если при увеличении температуры на 400С скорость возрастает в 81 раз?
1) 3
$$$ 207
Для какой из обратимых реакций повышение давления сместит равновесие в направлении прямой реакции:
А)H2+I2 Û 2HI
В)C+СO2 Û 2CO
С)N2+O2 Û 2NO
D)N2+3H2 Û 2NH3
Е)2HBr Û H2+Br2
$$$ 208
Как изменится скорость реакции 2NO(г)+O2(г) = 2NO2(г), если уменьшить объем реакционного сосуда в 3 раза?
1) возрастает в 27 раз
$$$ 209
Как изменится скорость реакции N2(г)+3Н2(г) Û 2NН3(г), если увеличить давление в системе в 3 раза?
1) 27
$$$ 210
В каком направлении сместится равновесие реакции А2(г)+В2(г) Û 2АВ(г), если давление увеличить в 2 раза и одновременно повысить температуру на 10 градусов? Температурные коэффициенты скоростей прямой и обратной реакций равны соответственно 2 и 3.
1) вправо, если темп. коэф.=2
$$$ 211
Значение константы скорости реакции зависит:
А)от объема и температуры
В)от природы реагирующих веществ
С)от давления в системе
D)от концентрации реагирующих веществ
Е)от давления и температуры
$$$ 212
Во сколько раз изменится скорость реакции 2А+В®А2В, если концентрацию вещества А увеличить в 2 раза, а концентрацию вещества В уменьшить в 2 раза?
1) возрастает в 2 раза
$$$ 213
Температурный коэффициент скорости реакции равен 2. Во сколько раз возрастет скорость реакции при повышении температуры от 200 до 700С?
$$$ 214
Математическое выражение скорости прямой реакции N2+3Н2®2NН3 соответствует уравнению:
1) V=k1*CN2*C3H2
$$$ 215
Катализатор ускоряет химическую реакцию благодаря …:
1) снижению энергии активации
$$$ 216
При увеличении концентрации реагирующих веществ, скорость химической реакции …:
1) увеличивается
$$$ 217
Как сместить равновесие реакции 2NO+O2®2NO2+Q влево?
1) повысить температуру
$$$ 218
Согласно правилу Вант-Гоффа как изменится скорость реакции при повышении температуры на 100С …?
1) растет в 2-4 раза
$$$ 219
Укажите гомогенную реакцию.
А)С(тв)+О2(г)=СО2(г)
В)4Al(тв)+3О2(г)=2Al2О3(тв)
С)CaСO3(тв) ®CaО(тв)+СО2(г)
D)N2(г)+3Н2(г) ®2NН3(г)
Е)2KClO3(тв)  2KCl(тв)+3О2(г)
2KCl(тв)+3О2(г)
$$$ 220
Во сколько раз увеличится скорость химической реакции: 4HCl(г)+O2(г)®2H2O(г)+2Cl2(г) при увеличении концентрации HCl в 2 раза?
1) 16
$$$ 221
Во сколько раз увеличится скорость химической реакции, протекающей в газовой фазе, при повышении температуры от 320 до 340 К, если g=3?
1) 9
$$$ 222
Как надо изменить давление, чтобы скорость реакции СО(г)+Н2О(г)=СО2(г)+Н2(г) увеличить соответственно в 36 раз?
$$$ 223
На сколько градусов надо понизить температуру, чтобы уменьшить скорость реакции в 81 раз, если g=3?
1) 400
$$$ 224
При повышении давления равновесие реакции: Fe3O4(тв)+4CO(г) Û 3Fe(тв)+4CO2(г)
1) не сместится
$$$ 225
Для смещения равновесия системы вправо, т.е. в сторону образования аммиака в реакции: N2(г)+3H2(г) Û 2NH3(г), необходимо:
1) увеличить давление
$$$ 226
Чтобы сместить равновесие системы 2CO(г)+O2(г) Û 2CO2(г)+Q влево (в сторону исходных веществ) необходимо:
 2018-01-21
2018-01-21 412
412







