Химическая кинетика
126. Учитывая, что при разложении 2 моль аммиака на простые вещества поглощается 92 кДж теплоты, укажите величину теплоты образования 1 моль аммиака. 46 кДж
127. Что такое энергия активации? Минимальное количество энергии,которое требуеться сообщить системе чтобы произошла реакция
128. На основании термохимического уравнения  кДж укажите величину теплового эффекта реакции образования 1 моль оксида Аl. 1600 кДж
кДж укажите величину теплового эффекта реакции образования 1 моль оксида Аl. 1600 кДж
129. Как меняется энтальпия в экзотермической реакции? - ∆H
130. Чему равны стандартные энтальпии образования простых веществ? 0
131. Какая из приведенных реакций является экзотермической? ∆H < 0
132. Экспериментально теплоты сгорания (а также энтальпии образования) определяют в специальном приборе, называемом калориметр
133. На основании термохимического уравнения  кДж, определите, какая масса углерода сожжена, если выделилось 206 кДж теплоты? 6г
кДж, определите, какая масса углерода сожжена, если выделилось 206 кДж теплоты? 6г
134. Учитывая термохимическое уравнение  укажите величину теплового эффекта реакции разложения 8 г оксида серы (ҮІ). 9,9
укажите величину теплового эффекта реакции разложения 8 г оксида серы (ҮІ). 9,9
135. На основании термохимического уравнения  определите, какой объем при н.у. займет молекула азота, если поглотится 45 кДж теплоты? 5,6л
определите, какой объем при н.у. займет молекула азота, если поглотится 45 кДж теплоты? 5,6л
136. На основании термохимического уравнения  определите, какой объем при н.у. займет водород, если выделилось 450 кДж теплоты. 336л
определите, какой объем при н.у. займет водород, если выделилось 450 кДж теплоты. 336л
137. Как обозначают стандартные тепловые эффекты? ∆Н0298
138. В каких единицах может выражаться скорость химической реакции? Моль л-1с-1
139. Какова размерность константы скорости для реакции первого порядка? с-1
140. Работы каких ученых в наибольшей степени способствовали выявлению
зависимости константы скорости химической реакции от температуры? Аррениус и Вант - Гоффа
141. Во сколько раз надо увеличить давление, чтобы скорость реакции

возросла в 1000 раз? 10
142. Как называются вещества, ускоряющие скорость химической реакции? катализаторы
143. какие вещества называют катализаторам? Изменяющие скорость химической реакции, но сами не изменяються в конце реакции
144. Как называется раздел химии, изучающий скорости и механизмы химических реакций? Химическая кинетика
145. Во сколько раз увеличится скорость реакции  при увеличении концентрации вещества
при увеличении концентрации вещества  в 3 раза? 3раза
в 3 раза? 3раза
146. Как изменится скорость реакции  при уменьшении концентрации вещества
при уменьшении концентрации вещества  в 2 раза? Уменьшиться в 4раза
в 2 раза? Уменьшиться в 4раза
147. Какое уравнение описывает зависимость скорости реакции V от температуры Т(g - температурный коэффициент реакции)? Ʋ2=Ʋ1 γt2-t1/10
148. Во сколько раз надо увеличить внешнее давление в системе, чтобы скорость реакции А(г)+2В(г)=С(г) увеличилась в 125 раз? 5 раз
149. Как изменится скорость реакции, протекающей по уравнению 
при увеличении концентрации водорода в 3 раза? Увеличиваеться в 9раз
150. Напишите математическое выражение для скорости реакции, протекающей по уравнению  . Ʋ= к [NH3]4[O2]5
. Ʋ= к [NH3]4[O2]5
151. Какой формулой запишется закон действия масс для реакции, протекающей по уравнению 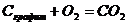 ? Ʋ= к[O2]
? Ʋ= к[O2]
152. Во сколько раз возрастет скорость химической реакции при увеличении температуры на 20˚С, если температурный коэффициент равен 2? 4раза
153. Во сколько раз увеличится скорость реакции при повышении температуры от  до
до 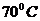 , если температурный коэффициент реакции равен 3? 27раз
, если температурный коэффициент реакции равен 3? 27раз
154. Во сколько раз увеличится скорость реакции при повышении температуры от  до
до  , если температурный коэффициент реакции равен 2? 16раз
, если температурный коэффициент реакции равен 2? 16раз
155. Во сколько раз возрастет скорость химической реакции при увеличении температуры на 40˚С, если температурный коэффициент равен 2? 16раз
156. Чему равен температурный коэффициент, если при увеличении температуры на 30˚С скорость химической реакции возрастет в 27 раз? 3
157. Какой формулой определяется скорость прямой химической реакции Sтв.+O2®SO2? Ʋ= к[O2]
158. Во сколько раз увеличится скорость реакции 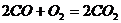 , если увеличить концентрацию реагирующих веществ в 2 раза? 8раз
, если увеличить концентрацию реагирующих веществ в 2 раза? 8раз
159. Для реакции  укажите кинетическое уравнение для прямого процесса.
укажите кинетическое уравнение для прямого процесса.
Ʋ= к [А2][В2]
 2018-01-21
2018-01-21 1319
1319








