Уравнение Гендерсона-Гассельбаха - математическое выражение, характеризующее возможности буферной системы. Уравнение показывает, как зависит кислотно-основное равновесие буферного раствора от свойств компонентов кислотно-основной буферной системы и от количественного соотношения этих компонентов в растворе. Показателем кислотно-основного равновесия в растворе является водородный показатель, pH. Свойство кислоты (её способность распадаться на ионы), как составляющей буферной системы, характеризуется значением константы равновесия, константы диссоциации кислоты, Kа. pK= – lgKД
Количественная структура (состав) буферной системы может быть оценена в виде отношения соль/кислота. Учитывая сказанное, уравнение Гендерсона-Гассельбаха выглядит следующим образом:
pH = pK+ lg 
На величину рН и рОН влияют константа диссоциации и соотношения концентраций компонентов.
12. Буферная ѐмкость. Зона буферного действия. Количественное определение буферной ёмкости.
Интервал рН=рКа±1 называется зоной буферного действия.
Буферная ёмкость(В) выражается количеством моль-эквивалентов сильной кислоты или щелочи, которое следует добавить к одному литру буфера, чтобы сместить рН на единицу.
В = 
В – буферная ёмкость,
nЭ– количество моль-эквивалента сильной кислоты или щелочи,
ΔрН – изменение рН.
На практике буферная ёмкость рассчитывается по формуле:
В = 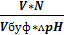
V – объём кислоты или щелочи,
N – эквивалентная концентрация кислоты или щелочи,
Vбуф - объём буферного раствора,
Δ рН – изменение рН.
Буферная ёмкость зависит от концентрации электролитов и соотношения компонентов буфера.
Количество кислоты или щелочи, которое нужно добавить к 1 л буферного раствора, чтобы значение его pH изменилось на единицу, называют буферной емкостью
Чем выше исходная концентрация буферной смеси, тем выше ее буферная емкость.
 2018-01-21
2018-01-21 2708
2708
