ПЕРВОЕ ВЫСШЕЕ ТЕХНИЧЕСКОЕ УЧЕБНОЕ ЗАВЕДЕНИЕ РОССИИ

МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ РОССИЙСКОЙ ФЕДЕРАЦИИ
Федеральное государственное бюджетное образовательное учреждение высшего образования
«САНКТ-ПЕТЕРБУРГСКИЙ ГОРНЫЙ УНИВЕРСИТЕТ»
Кафедра минералогии кристаллографии и петрографии
Реферат
По дисциплине: Геохимия а
(наименование учебной дисциплины согласно учебному плану)
Изучение геохимических свойств редкоземельных элементов
Автор: студент гр. РГИ-14 _________________ / Дорожкин Р. В./
(подпись) (Ф.И.О.)
Дата: ____________
Оценка: __________
ПРОВЕРИЛ: ассистент _________________ / Мельник А.Е. /
(должность) (подпись) (Ф.И.О.)
Санкт-Петербург
Содержание
Введение. 3
1. Общие сведения об РЗЭ.. 4
1.1. История открытия. 4
1.2. Область применения. 5
1.3. Положение в периодической системе и свойства РЗЭ.. 8
2. Распространенность РЗЭ.. 12
3. Основные типы месторождений РЗЭ.. 15
Заключение. 18
Список литературы.. 19
Введение
Редкоземельные элементы (РЗЭ) представлены группой из 15 весьма близких по свойствам элементов (№ 57–71 в системе Д. И. Менделеева). Название группы происходит от лат. «terrararae» – «редкая земля», поэтому их обозначают общим символом TR. К редкоземельным металлам относятся: лантан (La), церий (Се), празеодим (Рr), неодим (Nd), прометий (Рm), самарий (Sm), европий (Eu), гадолиний (Gd), тербий (Тb), диспрозий (Dy), гольмий (Но), эрбий (Еr), тулий (Тm), иттербий (Yb), лютеций (Lu).
В эту группу включен близкий к TR по свойствам иттрий (Y). Редкоземельные элементы широко используются в высокотехнологичных производствах. Ежегодно спрос на них возрастает на 10–15 %.
Общие сведения об РЗЭ
История открытия
В 1787 г. лейтенант шведской армии минералог-любитель Карл Аррениус нашел в заброшенном карьере поблизости от шведской деревни Иттерби неизвестный прежде черный блестящий минерал и назвал его в честь местонахождения – иттербит. Это событие положило начало эры открытий редкоземельных элементов (РЗЭ, R) и их последующих практических применений. Через семь лет, в 1794 г., финский профессор Ю. Гадолин исследовал иттербит и обнаружил в нем среди соединений магния, железа и кремния неизвестную ранее примесь, похожую одновременно и на оксид кальция, и на оксид алюминия. Гадолин назвал эту примесь иттриевой землей. В то время землями называли тугоплавкие плотные оксиды металлов. Отсюда и термин «редкие земли».
Уже в начале XX в. почти все члены редкоземельной семьи были обнаружены и описаны. Оставалась пустой только клетка периодической таблицы под № 61. Этот элемент открывали, закрывали и вновь открывали много раз. Но в 1947 г. была поставлена точка: американские исследователи Дж. Маринский, Л. Гленденин и Ч. Кориелл действительно нашли его среди продуктов, образующихся в ядерном реакторе. Последний лантаноид и последний редкоземельный элемент получил свое название в честь подарившего людям огонь Прометея – прометий (Pm). Открытием прометия завершилась удивительная история длиной в 160 лет (табл. 1) [3].
Таблица 1. Даты открытия РЗЭ и фамилии исследователей, которые это сделали

Область применения
Применение редкоземельных элементов можно разделить на следующие области:
· сферы, где используются неразделенные элементы (металлургия, производство катализаторов для нефтеперерабатывающей промышленности, выпуск перезаряжаемых аккумуляторных батарей, стекла и полировальных порошков);
· сферы, требующие использования разделенных элементов (производство каталитических фильтров-нейтрализаторов выхлопных газов автомобилей – церий; магнитов – самарий, неодим, тербий, диспрозий; люминофоров – иттрий, европий и тербий; конденсаторов – лантан; оптического стекла – лантан, церий; керамики – иттрий; высокотехнологичных абразивных материалов – церий; рентгеновских пленок – гадолиний, лантан, диспрозий; пигментов на основе сульфида и оксида церия).
В табл. 2 в лаконичном виде представлены сведения о базовых областях использования конкретных РЗЭ и их стоимости на мировом рынке до «редкоземельного кризиса» 2010–2011 гг.
Таблица 2. Основные области применения и стоимость РЗЭ.

В 70-е гг. ХХ в. использовались в основном неразделенные РЗЭ. Спрос на разделенные РЗЭ начал расти в 1980-е гг. по мере появления таких новых областей потребления, как производство люминофоров (иттрий и европий), магнитов (самарий и позднее неодим и диспрозий). Рынок сбыта разделенных редких земель в конце 1990-х гг. расширялся в среднем примерно на 8 % в год, однако спрос на редкоземельные металлы неоднороден. В настоящее время наиболее востребованными являются неодим, самарий и ставший весьма дефицитным диспрозий благодаря их использованию при производстве постоянных магнитов.
Катализаторы. На сегодня примерно треть всех потребляемых в мире РЗЭ используется в производстве катализаторов. Этот рынок подразделяется на два крупных сегмента: производство промышленных катализаторов и каталитических фильтров- нейтрализаторов выхлопных газов автомобилей. Первая группа товаров включает катализаторы, используемые в крекинге нефти и при синтезе каучука и полимеров. Для производства таких катализаторов применяются неразделенные элементы. Крупной составляющей мирового рынка каталитических фильтров-нейтрализаторов выхлопных газов автомобилей является производство катализаторов на основе церия (соединения этого металла способствуют удалению диоксида серы).
Постоянные магниты. Коммерческое производство редкоземельных магнитов началось в 1970 г. Появление самарий- кобальтовых сплавов для постоянных магнитов вызвало революционные преобразования во многих отраслях промышленности вследствие внедрения в технологические процессы мощных, обладающих высокой стабильностью малогабаритных магнитов с высокими характеристиками, что стимулировало расширение работ по разработке новых редкоземельных магнитных материалов. В результате был получен магнитный сплав неодим – железо – бор на основе фазы Nd2Fe14В, который в коммерческих масштабах начал производиться в середине 1980-х гг. Постоянные магниты на основе этого материала являются более энергоемкими, чем самарий-кобальтовые, и их производство требовало до последнего времени меньших затрат. В целом спрос на редкоземельные магниты в 1997– 2010 гг. рос в среднем на 15–21% в год даже в условиях финансового кризиса первой декады XXI в. В настоящее время на рынке редкоземельных магнитов доминирует Китай. На втором месте находится, хотя и не имеет собственного сырья, – Япония. Мировое производство редкоземельных магнитов на сегодня оценивается в 50–60 тыс. т в год. Россия вносит пока в этот объем весьма скромный вклад (порядка 1 %). Большую часть потребностей в магнитах промышленность России удовлетворяет за счет импорта магнитов из Китая.
Люминофоры и стекло. Производство люминофоров (включая пигменты) в стоимостном выражении является крупнейшей в мире сферой потребления РЗЭ. В 2000 г. продажи на этом рынке оценивались в $300 млн. Указанная сфера остается крупнейшим рынком сбыта иттрия, европия и тербия. Добавки РЗЭ позволяют увеличить коэффициент преломления и уменьшить степень рассеивания высокочистого стекла. Лантансодержащее стекло имеет высокое преломление и низкое рассеивание, поэтому его используют для изготовления линз теле-, фото- и кинокамер. Эрбийсодержащее оптическое волокно применяется в ретрансляционных станциях телекоммуникационных линий. Церий входит в состав добавок к экранному стеклу электронно-лучевых трубок и обеспечивает поглощение ультрафиолетовых лучей. Стекло, содержащее неодим, является отличным материалом для изготовления лазеров. Крупнейшим мировым центром производства редкоземельных люминофоров стал опять же Китай, чему способствовала передача в эту страну соответствующих технологий японских продуцентов, которые для снижения затрат перебазировали свои предприятия за рубеж.
Керамика. Важным рынком сбыта редких земель в индустриально развитых странах является производство промышленной электротехнической и электронной керамики. Поскольку телекоммуникации являются одной из быстроразвивающихся отраслей, то такие компоненты, как диэлектрические резонаторы, керамические фильтры, многослойные конденсаторы, будут изготовлять все в более значительном количестве. РЗЭ являются ключевой составляющей многих разрабатываемых твердых оксидных топливных элементов.
Металлургия. Редкоземельные элементы применяют в металлургии для устранения включений азота, кислорода и серы в стали. Например, в качестве сильных диоксидантов широко используются такие сплавы редкоземельных металлов, как Sc – Al, Sc – Mg, Y – Al, Y – Mg и Nd – Mn.
Аккумуляторные батареи. Перезаряжаемые аккумуляторные батареи подразделяются на три вида: NiCd, NiMH и Li-ионные. Батареи, содержащие РЗЭ – NiMH (никель-мишметалл-гидридные), примерно 10 лет тому назад стали новыми важными продуктами. Мишметалл (М) представляет собой сплав церия (45–70 %), лантана (22–35 %), неодима (15–17 %) и других редкоземельных элементов (8–10 %) с железом (до 10 %) и кремнием (0,1–0,3 %). В последние пять лет, ввиду развития рынков компьютеров и сотовых телефонов, наблюдался бурный рост спроса на Li-ионные батареи, которые доминируют на рынке портативных персональных компьютеров и высококачественных сотовых телефонов[4].
Положение в периодической системе и свойства РЗЭ
Под названием редкоземельные элементы (РЗЭ) объединяются лантан (порядковый номер 57) и следующие за ним в периодической системе химические элементы с порядковым номером 58-71, так называемые лантаниды. К ним относятся также иттрий и реже скандий (Табл. 3).
Таблица 3. Электронная структура, валентность и ионные радиусы РЗЭ и иттрия
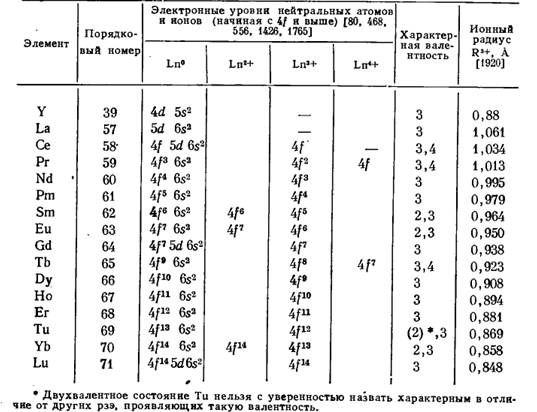
Указанные элементы принадлежат к III группе периодической системы элементов Д. И. Менделеева и имеют близкие химические свойства. Это зависит от того, что в двух внешних электронных оболочках их атомов, определяющих химические свойства, имеется одинаковое количество электронов. Лишь в третьей снаружи оболочке 4f имеется различное количество электронов. Различие в структуре глубинных оболочек атомов обусловливает различия физических свойств элементов и их соединений-растворимости, температуры кипения и др. По некоторым различиям в свойствах лантаниды делятся на две подгруппы – цериевую и иттриевую; последняя подразделяется еще на три подгруппы – тербия, эрбия и иттербия (табл. 4).
Таблица 4. Некоторые свойства редкоземельных элементов.
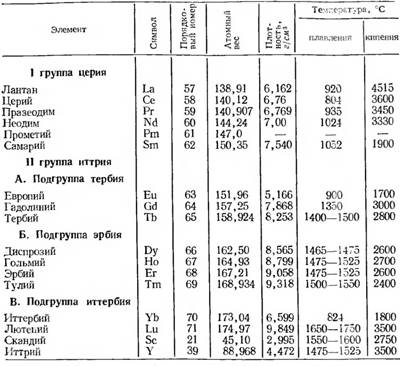
Элементы цериевой группы называют также легкими, и элементы иттриевой – тяжелыми. Помимо естественных известны искусственные радиоактивные изотопы редкоземельных элементов. Их получение и изучение началось относительно недавно, после создания первых ускорителей элементарных частиц.
Современные таблицы изотопов насчитывают около 150 радиоактивных изотопов редкоземельных элементов. Возможности получения новых искусственных изотопов также не исчерпаны.
Следует отметить, что РЗЭ имеют несколько природных изотопов. У лантана известно два изотопа: лантан-139 (99,9%) и лантан-138. За последние годы стало ясно, что изотоп лантана-138 не является стабильным, а распадается, испуская электроны с периодом полураспада Т =3.2*10-4 лет.
Среди 55 естественных изотопов РЗЭ имеется несколько радиоактивных: неоднм-150, самарий-147, лютеций-176. При этом самарий-147 является α-излучателем, неодин-150 β-излучателем; лютеций-176, испуская β-частицы, является также и слабым γ-излучателем. Имеются теоретические предсказания о β-активности для природных изотопов тулия-168.
Близость химических свойств отдельных РЗЭ, а также многих сопутствующих примесей требует очень сложных и трудоемких методов отделения и разделения редкоземельных элементов, что имеет важное санитарно-гигиеническое значение и может в значительной степени определять радиационную обстановку при выполнении тех или иных технологических операций.
слайд
Редкоземельным элементам свойствен металлический блеск, серый или желтоватый оттенок. Все РЗЭ – энергичные раскислители и дегазаторы. На воздухе они быстро покрываются пленкой окислов типа R2O3; активно взаимодействуют c водородом, азотом, галоидами, кислотами, водой. При прокаливании окислы образуют тугоплавкие белые порошки [1].
Церий, празеодим, тербий, кроме того, образуют высшие окислы типаRO2. Окислы европия, тербия, эрбия имеют розовую окраску; самария, диспрозия и гольмия – желтую; празеодима и тулия – зеленую; неодима голубую.
Окислы РЗЭ энергично присоединяют воду, образуя гидраты окислов R(OH)3. При нейтрализации солей редкоземельных элементов аммиаком или щелочью также образуются гидраты R(OH)3, нерастворимые в воде, но растворимые в кислых средах. Все полуторные окислы типа R2O3 редкоземельных элементов растворимы в кислотах, легко образуют нормальные соли даже со слабыми кислотами. Хлориды, нитраты и ацетаты лантана хорошо растворимы в воде. Карбонаты, фосфаты, напротив, трудно растворимы в воде, фториды нерастворимы даже в концентрированныхкислотах[2].
Относительно высокая химическая активность РЗЭ доказывается их способностью к образованию карбонатов. Растворимость карбонатов в углекислом аммонии увеличивается параллельно с ростом порядкового номера элемента.
При добавлении щавелевой кислоты к раствору, содержащему соли редкоземельных элементов и свободную минеральную кислоту, осаждаются оксалаты РЗЭ. Это дает возможность отделять их от других металлов при технологических операциях.
Наиболее распространены трехвалентные соединения РЗЭ, но встречаются и другие валентности. Благодаря тому, что четырехвалентные соединения церия обладают высокой окислительной способностью, он широко используется в аналитической химии.
РЗЭ склонны к образованию двойных солей с натрием, калием, аммонием и комплексов с органическими оксикислотами.
Редкоземельные элементы легко сплавляются со многими металлами, образуя интерметаллические соединения. Нитриды РЗЭ типа RN получают прямым соединением металлов с азотом при высоких температурах (около 1000° С). Сера при температуре ее кипения соединяется непосредственно с металлами, образуя сульфиды типа R2S3.
Прямым соединением получают также карбиды RC2, силициды, фосфиды. В результате действия фтора на карбиды соответствующих металлов образуются их фториды[1].
Галлоидные соединения РЗЭ гигроскопичны, хорошо растворимы в воде за исключением фторидов. В литературе имеются сведения о распределении галлоидов между водой и спиртами, кетонамии эфирами. Это свойство используется в химическом анализе для разделения некоторых редкоземельных элементов.
Для получения отдельных редкоземельных элементов широко используется комплексообразование с применением экстракции, а также ионного обмена на синтетических смолах. Для разделения РЗЭ довольно давно применяется фракционная кристаллизация[2].
 2018-01-21
2018-01-21 1108
1108