Для более точных расчѐтов используют метод последовательных приближений по известной зависимости теплосодержания(энтальпии)продуктов горения от температуры.
Если теплосодержание продуктов горения при Т=273 К принять равным нулю, то полное теплосодержание продуктов горения при Т Г будет равно количеству теплоты, выделившейся в результате химической реакции.
С учѐтом теплопотерь:
| Q н(1η) Н ПГ i V ПГ i , | (38) |


где Н ПГ i - теплосодержание (энтальпия) i -го продукта горения.
Задача состоит в том, чтобы найти температуру, при которой будет справедливо это равенство.
ПРИМЕР: Найти адиабатную температуру горения этилового спирта в воздухе, если теплота его образования равна - 278,2 кДж/моль.
Решение.
Адиабатную температуру горения вещества находят при условии отсутствия теплопотерь ( = 0), для стехиометрической смеси горючего с воздухом, т. е. при = 1.
= 0), для стехиометрической смеси горючего с воздухом, т. е. при = 1.
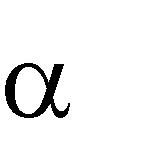
1. Для определения состава и объѐма продуктов горения запишем уравнение химической реакции горения этилового спирта:
С2Н6О + 3(О2 + 3,76 N2) = 2 CО2 + 3 Н2О + 3 3,76 N2.

2. Объѐм продуктов горения составляет: V CO2 2 моль/моль; V Н2O3моль/моль; V N 23  3,76 11,28 моль/моль; объѐм продуктов
3,76 11,28 моль/моль; объѐм продуктов

горения V ПГ 16,28 моль/моль.
3. Рассчитаем низшую теплоту сгорания этилового спирта по следствию из закона Гесса:



Q н  (Н СО2
(Н СО2  n CO2
n CO2  Н Н2О
Н Н2О  n Н2О
n Н2О  Н С2Н6О
Н С2Н6О  n C2Н6О)
n C2Н6О) 






 (2
(2  (396,9) 3
(396,9) 3  (242,2) (278,2)) 1242,2 (кДж/моль)
(242,2) (278,2)) 1242,2 (кДж/моль)
4. Так как теплопотери отсутствуют, то всѐ выделившееся тепло идѐт на нагрев продуктов горения. Среднее теплосодержание 1 моля продуктов горения будет составлять:
| Н ср | Q н | 1242,2 | 76,3 | (кДж/моль). | |
| V ПГ i | 16,28 | ||||



5. Воспользовавшись зависимостью теплосодержания газов от температуры (приложения 10 и 11), можно установить, какой температуре соответствует такое теплосодержание. Лучше всего это сделать, ориентируясь на азот, так как его больше всего в продуктах горения. Из приложения 10 видно, что при

температуре 2200 С теплосодержание азота 74,1 кДж/моль. Уточним, сколько потребовалось бы тепла, чтобы нагреть продукты горения до такой температуры. При t 1 = 2200 С

Q н1 Н СО2  V СО2 Н Н2О
V СО2 Н Н2О  V Н2О Н N2
V Н2О Н N2  V N2 120,8
V N2 120,8  2 98,8
2 98,8  3 74,1 11,28 1373,5
3 74,1 11,28 1373,5





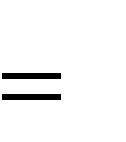
(кДж/моль).
Но это больше, чем выделилось тепла в результате реакции горения Q н1 Q н,поэтому можно сказать,что температура горения меньше,чем


2200 С. Определим, сколько потребуется тепла для нагревания продуктов горения до 2100 С.

| Q н 2 | 114,7 2 | 93,4 3 | 70,4 13,16 | 1303,7 | (кДж/моль). |
| Но и Q н2 | Q н,значит t Г | 2100 С | |||
| При температуре 2000 С | |||||
| Q н3 | 180,6 2 | 88,1 3 | 66,8 11,28 1217 | (кДж/моль). | |

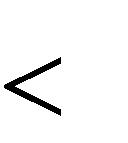


| Q н3 | уже меньше, чем | Q н,из этого можно сделать вывод,что температура | ||||||||||
| горения этанола имеет значение между 2000 и 2100 С. | ||||||||||||
| Уточним искомую температуру линейной интерполяцией между двумя | ||||||||||||
| этими ближайшими значениями: | ||||||||||||
| t Г | t 3 | t 2 | t 3 | (Q н | Q 3) 2000 | (1242 1217) 2029 | ºС или | |||||
| Q 2 | Q 3 | 1303,7 | ||||||||||


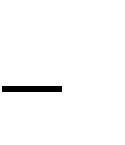




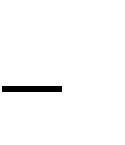



2302 (К).
Ответ: адиабатическая температура горения этанола составила2302К.
 2017-10-25
2017-10-25 1717
1717
