По заданным начальным значениям количества вещества (моль): n1, n2 и т.д. и общему давлению р′общ рассчитаем начальные парциальные давления участвующих в реакции газов: p′k = хk р′ общ, где хk - мольная доля компонента газовой смеси.
 ; Σ nk = 8,7, тогда
; Σ nk = 8,7, тогда
xC3H8 =  = 0,114942529
= 0,114942529
xC3H6 =  = 0,195402299
= 0,195402299
xH2 =  = 0,689655172
= 0,689655172
Рассчитаем парциальное давление компонентов по формуле:
pk = xk×робщ
p′k(C3H8) = 0,114942529×0,3 = 0,034482759
p′k(C3H6) = 0,195402299×0,3 = 0,05862069
p′k(H2) = 0,689655172×0,3 = 0,206896552
Далее, используя значения мольных долей компонентов, рассчитываем парциальные давления p′′k участников реакции при измененном в М = 20 раз общем давлении. Полученные данные внесём в Таблицу №3.
Таблица №3
| Вещество |  моль моль | 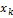 |  атм атм |  атм атм |  = =  атм атм |  атм атм |
 | 0,114942529 | 0,3 | 0,034482759 | 0,68965517 | ||
 | 1,7 | 0,195402299 | 0,3 | 0,05862069 | 1,17241379 | |
 | 0,689655172 | 0,3 | 0,206896552 | 4,13793103 |
Определение направления процесса при заданных условиях
Расчет ∆GT проводится по уравнению изотермы химической реакции. Одна из форм записи этого уравнения для нашей реакции имеет вид:
∆G975 = - RT lnKP,975 + RT ln 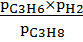
Рассчитаем ∆G975 при р′общ = 0,3атм и Т = 975К. Полученное значение ∆G′975 = -14384,90945 Дж/моль указывает на то, что при выбранных условиях реакция может идти самопроизвольно в сторону образования продуктов.
 2017-11-01
2017-11-01 901
901








