Термодинамика процесса
NaCN - комплексообразователь;
O2 - окислитель.
j0Au/Au+ = +1.88;
j0 O2/OH- = 0,40 B.
j0 O2/OH+H2O2 =-0,15B
E = jок - jвос >0, тогда процесс возможен.
jAu/Au(CN)2- - по уравнению Нернста = f(aAu+ ).
[Au(CN)2]- : KH = 1.1*10-41
aAu+ ¯¯, jAu/Au(CN)2- = -0.54 B.
Процесс становится также возможен.
Аналогично для [Ag(CN)2]-: KH = 1.8*10-19 ; jAg/Ag(CN)2- = -0.31 B.
Лимитирующую стадию процесса устанавливают экспериментально по следующим факторам:
- По интенсивности перемешивания;
- По влиянию температуры на процесс;
- По уравнению Аррениуса рассчитывают энергию активации
K=K0exp(-E/RT);
-По энергии активации (до20 КДж/моль- дифференциальные,
-50 КДж/моль- кинетические);
- влияние концентрации реагирующих веществ;
- влияние крупности материала.
Цианирование является типичным гетерогенным процессом, где твердая
фаза Au/Ag, жидкая фаза - цианистый раствор, газообразная фаза - О2.
Процесс цианирования можно представить состоящим из нескольких
элементарных стадий:
1. адсорбция O2 воздуха раствором;
2. диффузия ионов циана и молекул О2 к поверхности частицы;
3. химическая реакция;
4. отвод, диффузия продуктов реакции oт поверхности в объем раствора.
Если медленной является (1) или (2) стадия, процесс лимитируется дифузией. Если медленной является (3) стадия, то процесс лимитируется химической кинетикой. Эксперименты, проведенные Каковским и сотрудниками показали следующее рисунок 10.
ЕAgакт = 3,8 - 14,97 КДж/моль;
ЕAuакт = 6 - 15 КДж/моль.
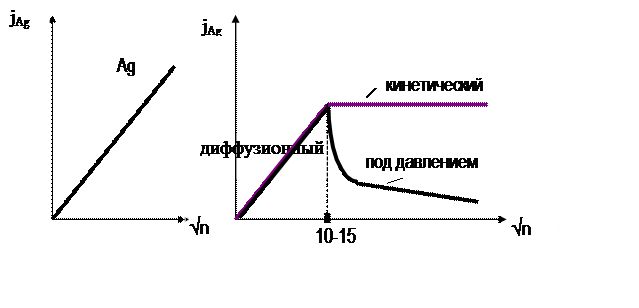 |
Рис. 10.
Таким образом, процесс протекает в диффузионном режиме. Лимитирующей является диффузия либо циан - иона, либо О2. Для Au характерен переход при интенсивном перемешивании из диффузионного режима в кинетический. Считают, что при интенсивном перемешивании происходит адсорбция О2 на поверхности Au, что затрудняет доступ цианида. Рисунок 11.
 |
.
В реальных условиях, как правило, лимитирует диффузия О2. Оптимальную скорость процесса можно достичь путем подбора соответствующих концентраций цианида и О2. Рисунок 12.
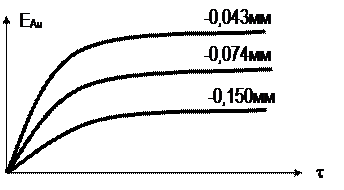 |
Рис. 12.
Чем больше поверхность реагирования, тем больше Е и скорость процесса.
!!! Все факторы, ускоряющие диффузию следует рассматривать как возможные пути интенсификации процесса цианирования.
 2014-01-25
2014-01-25 807
807








