Получение.
Кислые соли, помимо ионов металла и кислотного остатка, содержат ионы водорода.
Кислые соли
Кислые соли - представляют собой продукты неполного замещения атомов водорода атомами металла. Кислые соли - продукт неполной нейтрализации многоосновных кислот основаниями.
От двухосновных кислот (H2 SO4, H2 CO3, H2 S и т.д.) производится только один тип кислых солей - однозамещенные (атом металла замещает только один атом водорода кислоты).
Например:
H2 SO4 при неполной нейтрализации едким натром образует только одну кислую соль - NaHSO4.
От трехосновных кислот можно получить уже два типа кислых солей: однозамещенные и двухзамещенные.
Например:
при нейтрализации H3PO4 едким натром можно получить однозамещенную соль NaH2PO4:
H3PO4 + NaOH = NaH2PO4 + H2O
и двухзамещенную соль Na2HPO4:
H3PO4 + 2NaOH = Na2HPO4 + 2 H2O
Названия кислых солей содержат приставку "гидро" (от слова hydrogenium - водород). Например:
NaHCO3 - гидрокарбонат натрия,
K2HPO4 - гидрофосфат калия,
KH2PO4 - дигидрофосфат калия.
Диссоциация:
При диссоциации соли дают катионы металла (NH4+), ионы водорода и анионы кислотного остатка.
NaHCO3 «Na+ + HCO3- «Na+ + H+ + CO32-
Кислые соли получаются при взаимодействии кислот с металлами, оксидами металлов, гидроксидами металлов, солями, аммиаком, если кислота в избытке.
Например:
Zn + 2H2SO4 = H2 + Zn(HSO4)2,
CaO + H3PO4 = CaHPO4 + H2O,
NaOH + H2SO4 = H2O + NaHSO4,
Na2S + HCl = NaHS + NaCl,
NH3 + H3PO4 = NH4H2PO4,
2NH3 + H3PO4 = (NH4)2HPO4.
Также кислые соли получаются при взаимодействии кислотных оксидов со щелочами, если оксид в избытке. Например:
CO2 + NaOH = NaHCO3,
2SO2 + Ca(OH)2 = Ca(HSO3)2.
Средняя соль 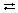 кислая соль; например:
кислая соль; например:
K2СО3 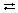 KНСО3.
KНСО3.
Чтобы из средней соли получить кислую, нужно добавить избыток кислоты или соответствующего оксида и воды:
K2СО3 + Н2О + СО2 = 2KНСО3.
Чтобы из кислой соли получить среднюю, нужно добавить избыток щелочи:
KНСО3 + KОН = K2СО3 + Н2О.
Гидрокарбонаты разлагаются с образованием карбонатов при кипячении:
2KНСО3 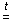 K2СО3 + Н2О + СО2.
K2СО3 + Н2О + СО2.
 2014-01-27
2014-01-27 761
761








