Возможны два типа гибридизации: d2sр3 и sр3d2, в зависимости от того, какие d-орбитали комплексообразователя доступны для лиганд. Гибридизация d2sр3 осуществляется в том случае, если в образовании σ связей участвуют s и рорбитали внешнего уровня и две d-орбитали предпоследнего уровня. Этот вид гибридизации называется внутренней гибридизацией, а образующиеся комплексы внутриорбитальными.
Например: [Cr(NH3)6]3+
Cr3+ 
 гибридизирующиесяорбитали
гибридизирующиесяорбитали
[Cr(NH3)6]3+ 
 электронные пары от лигандов
электронные пары от лигандов
При внутренней гибридизации лиганды прочно связаны с комплексообразователем, поэтому внутриорбитальные комплексы отличаются высокой устойчивостью.
Если на образование σ-связей комплексообразователь поставляет только орбитали внешнего уровня, то осуществляется sр3d2 гибридизация. Её называют внешней, а образующиеся комплексы внешнеорбитальными. Такие комплексы образуют d- элементы с полностью заселёнными d подуровнями. Например: [Cd(Cl)6]4-
Cd2+ 
 гибридизирующиесяорбитали
гибридизирующиесяорбитали
[Cu(Cl)6]4-

 электронные пары от лигандов
электронные пары от лигандов
Устойчивость комплексных соединений в растворе. Константа нестойкости комплексных соединений, её связь с константой устойчивости.
Ионы внешней сферы соединены с комплексом ионной связью, поэтому в водных растворах они легко отщепляются: [Fe(Н2О)6]SO4 ↔ SO42- + [Fe(Н2О)6]2+.
Этот процесс называется первичной диссоциацией. Внутренняя сфера в зависимости от прочности также способна диссоциировать на комплексообразователь и лиганды:
[Fe(Н2О)6]2+ ↔ Fe2+ + 6 Н2О – это вторичная диссоциация. Она аналогична диссоциации слабых электролитов и характеризуется константой равновесия: Крав. = 
константа равновесия может служить мерой прочности комплекса: чем менее стоек комплекс, тем больше концентрация простых ионов или молекул Fe2+ и Н2О, тем больше численное значение константы. Поэтому константу равновесия,
называют константой нестойкости комплекса. Величина, обратная константе нестойкости, называется константой устойчивости:
Куст.= 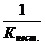 =
=  .
.
 2018-03-09
2018-03-09 99
99








