Термодинамический процесс – совокупность состояний системы, соответствующая некоторой непрерывной последовательности значений параметров состояния.
Равновесный термодинамический процесс – равновесный процесс представляет непрерывную последовательность равновесных состояний термодинамической системы когда все термодинамические параметры системы изменяются во времени одинаково и одновременно во всех точках её объёма.
Строго говоря, все реальные процессы неравновесны. Однако, при определённых условиях, реальные процессы очень близки к равновесным.
Равновесные процессы сравнительно просто описываются математически и графически. В самом деле, если известен конкретный вид уравнения состояния (2.3), пользуясь этим уравнением можно построить в координатах  некоторую поверхность, которая называется термодинамической поверхностью.
некоторую поверхность, которая называется термодинамической поверхностью.
Каждая точка этой поверхности соответствует вполне определённому равновесному состоянию системы, а любая линия, расположенная на этой поверхности, изображает равновесный процесс.
В равновесном процессе внешние условия изменяются настолько медленно, что термодинамическая система успевает прийти в равновесие с окружающей средой.
Обратимый термодинамический процесс. Всякий равновесный процесс является обратимым: термодинамическую систему можно вернуть из конечного состояния в начальное. и при этом, во внешней среде не произойдет никаких изменений. Это означает, что в обратном процессе система пройдет через те же состояния, через которые она проходила в прямом процессе.
Адиабатический процесс - процесс, происходящий без подвода и отвода тепла ( ). Из первого закона термодинамики следует, что при адиабатическом процессе
). Из первого закона термодинамики следует, что при адиабатическом процессе 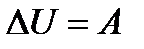 , т. е. внешняя работа совершается за счет внутренней энергии системы.
, т. е. внешняя работа совершается за счет внутренней энергии системы.
Изотермические процессы расширения и сжатия идеального газа,  .При расширении газа происходит его охлаждение. Для того чтобы процесс расширения был изотермическим необходимо компенсировать это охлаждение подводом тепла из окружающей среды. Этот процесс должен протекать достаточно медленно, чтобы температура газа все время успевала сравняться с температурой окружающей среды. Согласно первого закона термодинамики, количество теплоты, переданное газу, идёт на совершение газом работы против внешних сил.
.При расширении газа происходит его охлаждение. Для того чтобы процесс расширения был изотермическим необходимо компенсировать это охлаждение подводом тепла из окружающей среды. Этот процесс должен протекать достаточно медленно, чтобы температура газа все время успевала сравняться с температурой окружающей среды. Согласно первого закона термодинамики, количество теплоты, переданное газу, идёт на совершение газом работы против внешних сил.
При сжатии газа происходит его нагревание. Для того чтобы процесс нагревания был изотермическим необходимо компенсировать это нагревание отводом тепла в окружающую среду. Этот процесс должен протекать также достаточно медленно, чтобы температура газа все время успевала сравняться с температурой окружающей среды. Согласно первого закона термодинамики отвод теплоты от газа происходит за счет работы внешних сил.
В обоих процессах давление убывает с увеличением объёма, но в адиабатном процессе убывание идёт быстрее (рис.2.2).

Рис. 2.2. Сравнительный ход изотермы и адиабаты
Физически это объясняется тем, что при адиабатном расширении давление газа уменьшается не только за счет уменьшения объема, но и по причине происходящего при этом понижении температуры.
Наоборот, при адиабатном сжатии от объема до объема давление газа растет быстрее, чем при изотермическом процессе, так как при адиабатном процессе давление увеличивается не только за счет уменьшения объема, но и вследствие роста температуры газа.
Работа газа в произвольном термодинамическом процессе. Предположим, что газ расширяется при постоянном давлении  . Тогда сила элементарная сила
. Тогда сила элементарная сила 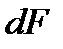 , с которой газ действует на поршень, с элементарной площадью
, с которой газ действует на поршень, с элементарной площадью  также постоянна. Пусть поршень переместился на расстояние х (рис. 2.3.а).
также постоянна. Пусть поршень переместился на расстояние х (рис. 2.3.а).
Работа газа равна: 
Рассмотрим работу газа в произвольном термодинамическом процессе, когда давление не постоянно (рис. 2.3.б).
Рис.2.3. Работа газа в произвольном термодинамическом процессе
Рассмотрим элементарное изменение  объёма газа при котором давление будет оставаться приблизительно постоянным
объёма газа при котором давление будет оставаться приблизительно постоянным  .
.
Газ совершит элементарную работу  . Тогда работа
. Тогда работа  газа во всём процессе найдётся суммированием этих элементарных работ:
газа во всём процессе найдётся суммированием этих элементарных работ:
 (2.6)
(2.6)
 2018-03-09
2018-03-09 101
101








