Данная программа предназначена для проведения лабораторных работ по термодинамике для студентов технических вузов. Она позволяет моделировать и получать количественные характеристики любого термодинамического (квазистатического) процесса. Также имеется возможность увидеть графики этих процессов при любой функциональной зависимости координатных осей.
Лабораторная установка представляет собой цилиндр с подвижным поршнем, заполненный двухатомным идеальным газом (молярную массу можно выбирать произвольно). Газ в установке можно нагревать (охлаждать). В программе предусмотрена возможность помещения установки в термостат. Для начала эксперимента необходимо ввести начальные значения необходимых вам параметров. Невведенные параметры вычисляются через известные или им присваиваются (в случае нехватки параметров для вычисления) значения параметров при нормальных условиях.
Изотермический процесс
1. Выберите в окне программы значение массы газа, степень свободы и молярную массу газа (рис.2). Занесите в табл.1 начальные параметры газа.
2. Для проведения с газом изотермического процесса необходимо рядом с буквой Т установить флажок.
3. Уменьшите объём газа перетаскиванием бегунка полосы прокрутки, расположенного справа от рисунка.
4. Занесите в табл. 1 конечные параметры газа, а также количество теплоты, сообщенное газу, изменение внутренней энергии и совершенную газом работу.
5. Рассчитайте теплоемкость газа в данном процессе.
6. Зарисуйте графики изотермического процесса в координатах рV, рТ, VT.
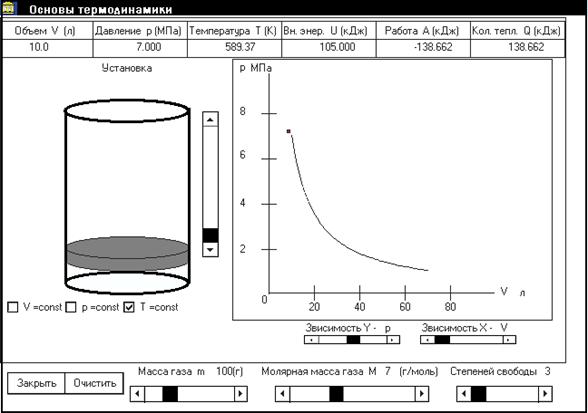
Рис.2. Рабочее окно программы
Таблица 1
Результаты измерений
| Параметры | V | p | T | A | ∆U | Q | C |
| В начале процесса | |||||||
| В конце процесса |
Изохорный процесс
1. Выберите в окне программы значение массы газа, степень свободы и молярную массу газа (рис. 3). Занесите в табл.2 начальные параметры газа. Для проведения с газом изохорного процесса необходимо рядом с буквой V установить флажок.
2. Для проведения с газом изохорного процесса необходимо выбрать мощность нагревателя нажатием клавиши «Обогреватель».
3. Нажатием клавиши «Начать эксп.» нагрейте газ примерно на 100 К. Выключите нагреватель, нажав клавишу «Остановить эксп.»
4. Занесите в табл. 2 конечные параметры газа, а также количество теплоты, сообщенное газу, изменение внутренней энергии и совершенную газом работу.
5. Рассчитайте теплоемкость газа в данном процессе.
6. Зарисуйте графики изохорного процесса в координатах pV, pT, VT.
Таблица 2
Результаты измерений
| Параметры | V | p | T | A | ∆U | Q | C |
| В начале процесса | |||||||
| В конце процесса |
Изобарный процесс
1. Для проведения с газом изобарного процесса необходимо рядом с буквой Р установить флажок. Выбор мощности нагревателя производится нажатием клавиши «Обогреватель».
2. Выберите в окне программы значение массы газа, степень свободы и молярную массу газа (см. рис. 3). Занесите в табл.3 начальные параметры газа.
3. Нажатием клавиши «Начать эксп.» нагрейте газ примерно на 100 К. Выключите нагреватель, нажав клавишу «Остановить эксп.»
4. Занесите в табл.3 конечные параметры газа, а также количество теплоты, сообщенное газу, изменение внутренней энергии и совершенную газом работу.
5. Рассчитайте теплоемкость газа в данном процессе.
6. Зарисуйте графики изобарного процесса в координатах pV, pT, VT.
Таблица 3
Результаты измерений
| Параметры | V | p | T | A | ∆U | Q | C |
| В начале процесса | |||||||
| В конце процесса |
Адиабатный процесс
1. Выберите в окне программы значение массы газа, степень свободы и молярную массу газа (см. рис. 3). Занесите в табл.4 начальные параметры газа.
2. Уменьшите объём газа перетаскиванием вниз бегунка полосы прокрутки, расположенного справа от рисунка.
3. Занесите в табл.4 конечные параметры газа, а также количество теплоты, сообщенной газу, изменение внутренней энергии и совершенную газом работу.
4. Рассчитайте теплоемкость газа в данном процессе.
5. Зарисуйте графики адиабатного процесса в координатах pV, pT, VT.
Таблица 4
Результаты измерений
| Параметры | V | p | T | A | ∆U | Q | C |
| В начале процесса | |||||||
| В конце процесса |
Проверка первого начала термодинамики
Вычислите работу, изменение внутренней энергии и количество теплоты с помощью теоретических формул и сравните с полученными значениями. Заполните табл. 5.
Найдите значение отношения Ср / CV.
Таблица 5
Результаты измерений
| Процесс | А | ∆U | Q | А | ∆U | Q |
| Теоретические | Экспериментальные | |||||
| Изохорный | ||||||
| Изобарный | ||||||
| Изотермический | ||||||
| Адиабатный | ||||||
Заключение
При защите Л.Р. вы должны уметь зарисовать график любого из процессов в любых координатах, знать и уметь показать по формулам особенности поведения Q, A, 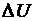 в любом из процессов, уметь подсчитать и сравнить теплоёмкости газов.
в любом из процессов, уметь подсчитать и сравнить теплоёмкости газов.
 2018-02-13
2018-02-13 325
325







