Галогенопроизводные углеводородов – это продукты замещения атомов водорода в молекулах углеводородов на атомы галагенов. Их общая формула R-X, где Х – может быть F, Cl, Br, J. В зависимости от характера радикала различают галогенопроизводные предельных и непредельных углеводородов: по числу галогена – моно-, ди – и полигалогенпроизводные.
Моногалогенопроизводные предельных углеводородов называются алкилгалогенидами. Названия их производят от названий соответствующих углеводородных радикалов (алкилов) с прибавлением слова – хлорид, бромид, иодид, фторид. Например:
СН3Cl CH3 – CH2 – Br
метилхлорид этилбромид
Некоторые галогенопроизводные имеют тривиальные названия, например, CHCl3 – хлороформ, CHJ3 – иодоформ. По М.Н. названия галогенопроизводных производят от названий углеводородов с добавлением названия галогена и цифры, обозначающей, при каком атоме углерода он находится. Углеродную цепь нумеруют с того конца, к которому ближе стоит галоген:
С(4)Н3 – С(3)Н2 – С(2)Н – С(1)Н3 С(1)Н3 – С(2)Н – С(3)Н – С(4)Н2 –СН3
| | |
Cl Br CH3
2-хлорбутан 2-бром-3метилпентан
Химические свойства
Галогенопроизводные углеводородов обладают высокой реакционной способностью. Это объясняется тем, что электронная пара – связи углерод – галоген смещена к более электроотрицательному атому галогена -> С(б+) → Х(б-), что приводит к появлению на нем частичного отрицательного заряда (б-). На атоме углерода появляется частичный положительный заряд (б+). Т.е. связь углерод – галоген сильно поляризована и возможен гетеролитический разрыв этой связи с отщеплением аниона галогена. Для галогенопроизводных характерны реакции нуклеофильного замещения атомов галогена.
1. Гидролиз. При действии на алкилгалогениды воды в присутствии щелочей происходит замещение атома галогена на гидроксильную группу с образованием спиртов:
б+ б- + –
|

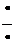 CH
CH 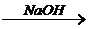 CH3 – CH2 – OH + HCl
CH3 – CH2 – OH + HCl
этилхлорид этанол
2. Аммонолиз. При действии аммиака на алкилгалогениды галоген замещается на аминогруппу – NH2. Образуются амины:
б+ б-
|
 –NH(· ·)2
–NH(· ·)2  CH3 – CH2 – NH2 + HJ
CH3 – CH2 – NH2 + HJ
этилиодид этиламин
3. Действие цианида калия. Образуются нитрилы, например:

СН3  J + K – CN
J + K – CN  CH3 – CN + KJ
CH3 – CN + KJ
метилиодит ацетонитрил
4. Отщепление галогеноводорода. При действии на алкилгалогениды спиртовых растворов щелочей происходит отщепление галогеноводорода и образуются алкены. Отщепление галогеновоорода происходит по правилу Зайцева: водород уходит от соседнего, наименее гидрированного атома углерода:
СН3–СН2–СHBr–CH3+KOH 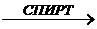 CH3–CH=CH–CH3+KBr+H2O
CH3–CH=CH–CH3+KBr+H2O
2-бромбутан -HBr бутен-2
Из дигалгенопроизводных образуются алкины:

H H
| |
НС – СН + КОН 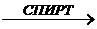 СН ≡ СН + 2KBr + 2H2О
СН ≡ СН + 2KBr + 2H2О
 | | -2HBr
| | -2HBr
Br Br
1,2 – дибромэтан этин
 2018-02-13
2018-02-13 422
422






