Расчётные характеристики для заданных видов топлива предоставлены в таблицах 2.1 и 2.2
Таблица 2.1 Характеристики твёрдого топлива.
| Ср % | Wp % | Ap % | Spk % | TSpop % | Hp % | Np % | Op % | Qрн КДж/кг | Vг | t1 0С | t2 0С | t3 0С |
| 84,8 | 3 | 0,1 | 1.4 | 11.2 | 0.5 | 0.5 | 9490 * 4.187 | 50 | 1450 | >1500 | - | |
Таблица 2.2 Характеристики газа.
| CH4 % | C2H6 % | C3H8 % | C4H10 % | C5H12 % | N2 % | CO2 % | H2S % | O2 % | CO% | H2 % | Qсн КДж/м3 | rсг кг/м3 |
| 93.9 | 3.1 | 1.1 | 0.3 | 0.1 | 1.3 | 0.2 | - | - | - | - | 8860*4.187 | 0.766 |
Теплота сгорания смеси топлив
При сжигании смеси жидкого и газообразного топлив расчёт с целью упрощения условно ведется на 1 кг жидкого топлива с учётом количества газа (м3), приходящегося на 1 кг жидкого топлива. Поскольку доля жидкого топлива в смеси задана по теплу, то теплота сгорания жидкого топлива и является этой долей.
Следовательно, удельная теплота сгорания смеси определиться как

где  – теплота сгорания твёрдого топлива, кДж/кг;
– теплота сгорания твёрдого топлива, кДж/кг;
 – доля твёрдого топлива по теплу, %;
– доля твёрдого топлива по теплу, %;
Количество теплоты, вносимое в топку с газом:

Тогда расход газа (в м3) на 1 кг твёрдого топлива будет равен:

где 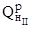 – теплота сгорания газа, кДж/м.
– теплота сгорания газа, кДж/м.
Проверка:

Объёмы воздуха и продуктов сгорания
Необходимое для полного сгорания топлива количество кислорода, объёмы и массовые количества продуктов сгорания определяются из нижеследующих стехиометрических уравнений:
· Для твёрдого топлива:




· Для газообразного топлива:
V°вII=0.0476∙[0.5∙СО+0.5∙Н2+1.5∙Н2S+∑(m+0.25∙n)∙СmНn–О2]=
=0.0476∙(0+(1+0,25*4)*93,9+(2+0,25*6)*3,1+(3+0,25*8)*1,1+(4+0,25*10)*0,3+(5+0,25*12)*0,1)=9,84844 м/м;
V°N2II=0.79∙V°вII+0.01∙N2=0.79∙9.84844+0.01∙1,3=7.8 мм;
V°RO2II=0.01∙(СО2+СО+Н2S+∑m∙СmНn)=0.01∙(0.2+1∙93.2+2∙3,1+3∙1.1+4∙0.3+5Ч0,1)=1.053 мм;
V°Н2OII=0.01∙(Н2S+Н2+∑0.5∙n∙СmНn+0.124∙dr)+0.0161∙V°в=0.01∙(0.5∙4∙93.9+6·3,1·0,5+0.5∙8∙1.1+0.5∙10∙0.3+0.5∙12·0,1+0,124·)+0.0161∙9.84844=2.2 мм;
· Для смеси топлив:
V°в=V°вI+Х∙V°вII=10,6+1,9∙9,84844=29,22 м/кг;
V°N2=V°N2I+Х∙V°N2II=8,378+1,9∙7.8=23,198 мкг;
VRO2=V°RO2I+Х∙V°RO2II=1,6+1,9∙1.053=3,6 мкг;
V°Н2O=V°Н2OI+Х∙V°Н2OII=1,45+1,9∙2,2=5,63м/кг;
Расчёт действительных объёмов.
VN2=V°N2+(a–1)∙V°в=23,198+(1.1–1)∙29,22=26,12 м/кг;
VН2O=V°Н2O+0.0161∙(a–1)∙V°в=5,63+0.0161∙(1.1–1)∙29,22=5,68м/кг;
Vr=VRO2+VN2+VН2O=3,6+26,12+5,68=35,4 м/кг;
Объёмные доли трёхатомных газов.
rRO2=VRO2/Vr=3,6/35,4=0.102
rН2O=VН2O/Vr=5,68/35,4=0.16
rn=rRO2+rН2O=0.102+0.16=0.3
 2020-01-14
2020-01-14 150
150








