| № | Химическая формула вещества | Название вещества |
| 1 | 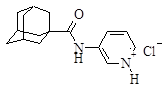
| N-(1-адамантил)-3-аминопиридина гидрохлорид |
| 2 | 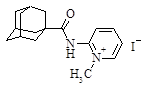
| 2-[N-(1-адамантоил)амино]-1-метилпиридиний иодид |
| 3 | 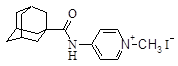
| 4-[N-(1-адамантоил)амино]-1-метилпиридиний иодид |
| 4 | 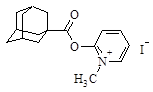
| N-(1-метилпиридиний-3-ил)-адамантил-1-карбоксамид иодид |
| 5 | 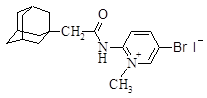
| 2-[N-(1-адамантоил)амино]-4-бром-1-метилпиридиний иодид |
| 6 | 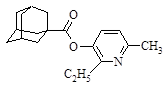
| 3‑(адамантил-1-карбонилокси)-2‑этил‑6-метилпиридин |
| 7 | 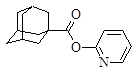
| 2‑(адамантил‑1‑карбонилокси)-пиридин |
Продолжение таблицы 1.
| № | Химическая формула вещества | Название вещества |
| 8 | 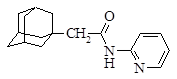
| N-(1-адамантилацетил)-2-аминопиридин |
| 9 | 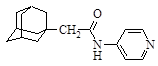
| N-(1-адамантилацетил)-4-аминопиридин |
| 10 | 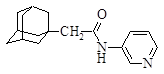
| N-(1-адамантилацетил)-3-аминопиридин |
| 11 | 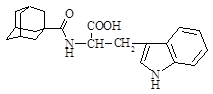
| N-(1-адамантоил)-D,L-триптофан |
| 12 | 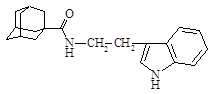
| 3-(1-адамантанкарбоксамидо-этил)индол |
| 13 | 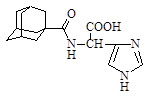
| N-(1-адамантоил)-D,L-гистидин |
| 14 | 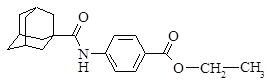
| 4-адамантанкарбоксамидо-этилбензоат |
| 15 | 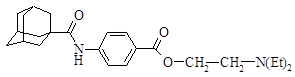
| 4-адамантанкарбоксамидо-N - [2-(диэтиламино)этил]-бензоат |
| 16 | 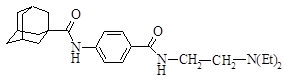
| 4-адамантанкарбоксамидо-N-[2-(диэтиламино)этил]-бензамид |
Продолжение таблицы 1.
| № | Химическая формула вещества | Название вещества |
| 17 | 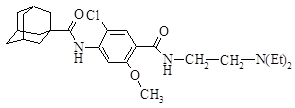
| 4-адамантанкарбоксамидо-5-хлор-N-[2-(диэтиламино)этил]-2-метоксибензамид |
| 18 | 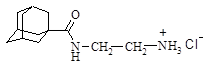
| N-(1-адамантоил)этилендиамина гидрохлорид |
| 19 | 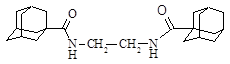
| N,N'-ди-(1-адамантоил)этилендиамин |
Эти вещества синтезированы в лаборатории кафедры органической химии СамГУ научным сотрудником кандидатом химических наук Ермохиным В. А. [13, 14, 15, 16]. Строение вновь синтезированных соединений доказано данными ЯМР 1Н и ИК спектроскопии (Приложение, табл. 1-4). ИК спектры соединений снимали на спектрофотометре ИКС-29 в таблетках из KBr. Спектры ЯМР получены на приборе Bruker WP-200 SY (рабочая частота 200,13 МГц). В качестве растворителя применяли ДМСО-d6, CD3CN, CDCl3. Отсчёт химических сдвигов проводили относительно сигнала ТМС. Для подтверждения индивидуальности всех полученных соединений проводили тонкослойную хроматографию на пластинках Silufol UV в этилацетате. Соединения № 18 и № 19 были синтезированы ранее [12].
Агрегация тромбоцитов исследована фотометрическим методом Борна [4]. Принцип метода основан на регистрации снижения оптической плотности исследуемой плазмы после введения в неё тромбоцитагрегирующего агента. Происходит «склеивание» тромбоцитов, образующиеся агрегаты постепенно оседают и проба плазмы становится более прозрачной.
Биологический материал предоставлен самарской областной станцией переливания крови. Кровь, взятую из локтевой вены, стабилизировали 3,8 % раствором цитрата натрия (9:1). Богатую тромбоцитами плазму получали центрифугированием цитратной крови при 1000 об/мин в течение 10 минут. Плазму разбавляли 0,154 М раствором хлорида натрия, рН 7,2 до достижения оптической плотности пробы 0,4-0,6 ед. (стандартизация плазмы). Плазму разливали в кюветы по 2 мл. Изучаемые соединения растворяли в 96 % этиловом спирте. В качестве агрегирующих агентов использовали растворённый в 0,154 М физ. растворе рН 7,2 5-гидрокситриптамин креатин сульфат (серотонин) и АДФ в конечной концентрации 1*10-5 М. В эксперименте в качестве агреганта использовался также адреналина гидрохлорид в концентрации 0,1 %. Конечные концентрации всех соединений составляли 0,099 мг/мл. Оптическую плотность измеряли против контроля на СФ-46 при длине волны 600 нм, кювета 10 мм (в контрольную пробу добавляли спирт вместо раствора вещества) в течение 30 минут. Об интенсивности агрегации судили по изменению оптической плотности относительно контроля, которое выражали в условных единицах: ∆ А30 (изменение оптической плотности за 30 минут)´1000=х у. е.
Полученные данные анализировали для установления значений их достоверности согласно критерию Стьюдента. Данные считали достоверными при уровне значимости р<0,05 [41].
 2020-01-14
2020-01-14 155
155








