Чтобы в этом убедиться, можно исследовать влияние на репродуктивную систему хронического, но небольшого стресса. Возьмем традиционное незападное земледельческое сообщество, в котором отмечаются высокий уровень заболеваний (скажем, сезонная малярия), высокий уровень зараженности паразитами и небольшое сезонное недоедание, — например, фермеров Кении. Прежде чем в моду вошло планирование семьи, кенийская женщина в среднем рожала восьмерых детей.
Сравним это сообщество с фермерской общиной гуттеритов, проживающей в США. Эти люди не используют механизированный труд, и их образ жизни напоминает традиции амишей. Гуттериты не испытывают ни одного из хронических стрессоров, которым подвергаются кенийские фермеры, не используют противозачаточных средств и имеют почти такой же уровень рождаемости: в среднем по девять детей на женщину. (Количественное сравнение этих двух популяций провести трудно. Гуттериты, например, вступают в брак довольно поздно, что снижает уровень рождаемости, а кенийские фермеры традиционно вступают в брак очень рано. И наоборот, кенийские женщины, как правило, кормят ребенка грудью в течение по крайней мере года, что снижает уровень рождаемости, а гуттериты отнимают детей от груди намного раньше. Но самое главное, что даже при такой разнице в образе жизни уровень рождаемости у этих двух сообществ почти одинаковый.)
Как же ведет себя репродуктивная система во время очень сильного стресса? Этот вопрос активно обсуждается в литературе и всегда ставит перед нами этическую проблему: как описать научное открытие, если его авторы были бессердечными монстрами? Например, есть известное исследование женщин — узниц концентрационных лагерей Третьего рейха, проведенное нацистскими врачами. (Существует специальная конвенция, запрещающая называть имена этих врачей и предписывающая всегда отмечать преступность их экспериментов.) Исследование узниц концлагеря Терезиенштадт показало, что у 54% женщин репродуктивного возраста прекратились менструации. Это едва ли удивительно; голод, рабский труд и ужасающее психологическое насилие нарушают функционирование репродуктивной системы.
Среди тех женщин, у которых прекратились менструации, у большинства это случилось в первый месяц нахождения в концлагере, еще до того, как голод и тяжелый труд снизили количество жира в организме до критического уровня. Многие исследователи считают, что это подтверждает, насколько разрушительным для репродуктивной системы может быть один лишь психологический стресс.
А я думаю, что удивительно как раз обратное. Несмотря на голод, изнурительный труд и ежедневный ужас от осознания того, что этот день может оказаться последним, менструации прекратились только у 54% женщин. Почти у половины из них репродуктивные механизмы продолжали действовать (хотя, возможно, овуляция происходила не у всех). И я готов поспорить, что, несмотря на ужас ситуации, у многих мужчин — узников концлагерей репродуктивная система тоже работала нормально. Мне кажется невероятным тот факт, что в таких условиях репродуктивная система продолжала действовать, пусть даже только у некоторых людей.
Репродуктивная система представляет собой обширную иерархию поведенческих и физиологических феноменов, которые значительно отличаются между собой по уровню тонкости. Некоторые ее аспекты являются базовыми и наиболее важными — овуляция, перенаправление кровотока к пенису. Другие очень деликатны, такие как строка стихотворения, волнующая душу, или легкий аромат, исходящий от любимого человека и вызывающий прилив желания. Не все эти феномены одинаково чувствительны к стрессу. У многих людей базовый репродуктивный механизм может быть удивительно устойчив к стрессу, как показывает опыт холокоста. Размножение — один из самых сильных биологических рефлексов. Об этом знают любой лосось, выпрыгивающий из воды, поднимаясь против течения, чтобы отложить икру, самцы самых разных видов животных, рискующие жизнью и здоровьем, чтобы получить доступ к самкам, и подросток с безумным взглядом, затуманенным стероидами.
Но когда дело доходит до пируэтов и изысканных па сексуальности, стресс может все разрушить. Возможно, для голодающих беженцев или для животных в разгар засухи это не так уж важно. Но очень важно для нас, с нашей культурой множественного оргазма, коротких периодов воздержания и океанов либидо. Над нашей одержимостью сексом можно смеяться, но тонкие нюансы сексуальности, глянцевые журналы и прочие приметы нашего избалованного века имеют смысл. Они дарят нам такие прекрасные, но такие хрупкие и мимолетные радости бытия.
8. Иммунитет, стресс и болезни
Конференц-залы научных институтов сегодня полны ученых новой породы — психонейроиммунологов. Эти люди зарабатывают на жизнь исследованиями, основанными на том невероятном факте, что происходящее в нашей голове может влиять на работу нашей иммунной системы. Когда-то считалось, что две эти сферы никак между собой не связаны — иммунная система уничтожает бактерии, продуцирует антитела, охотится на опухоли; мозг помогает нам танцевать, изобретать колесо и смотреть любимые телесериалы. Но идея о независимости иммунной и нервной систем оказалась ошибочной. Автономная нервная система пронизывает нервами ткани организма, которые формируют или хранят клетки иммунной системы. Затем эти клетки поступают в кровь. Кроме того, ткани иммунной системы, оказывается, чувствительны (то есть обладают рецепторами) ко всем тем интересным гормонам, которые вырабатываются гипофизом по команде мозга. Поэтому, как оказалось, мозг постоянно сует свой нос в дела иммунной системы.
Доказательства влияния мозга на иммунную систему начали появляться как минимум 100 лет назад начиная с первой демонстрации: если перед носом человека, страдающего аллергией на розы, помахать искусственной розой (при условии, что он не знает, что роза фальшивая), у него случится аллергическая реакция. А вот очаровательная и более свежая демонстрация того, что мозг влияет на иммунную систему: возьмем две группы профессиональных актеров. Попросим первую группу целый день репетировать мрачную, депрессивную сцену, а вторую — оптимистичный, радостный этюд. У актеров из первой группы ослабеет реакция иммунной системы, а у актеров второй группы она усилится. (Как вы думаете, где было проведено это исследование? Конечно же, в Калифорнийском университете в Лос-Анджелесе.) Но наиболее явно на связь между мозгом и иммунной системой указало исследование, основанное на парадигме, получившей название «условное подавление иммунитета».
Введите животному препарат, подавляющий иммунную систему. После этого проведите эксперименты в стиле Павлова с «условными стимулами», например давайте животному ароматизированный напиток, который оно может связать с подавляющим иммунитет препаратом. Несколько дней спустя дайте животному только условный стимул, вызывающий реакцию, — и иммунитет упадет. В 1982 году был опубликован отчет об эксперименте, основанном на одном из вариантов этой парадигмы и проведенном двумя новаторами в этой области, Робертом Адером и Николасом Коэном из Рочестерского университета. Результаты ошеломили ученых. В экспериментах на мышах животные неожиданно начали болеть из-за избыточной активности иммунной системы. Обычно болезнь контролируют, давая мышам иммунодепрессанты. Адер и Коэн показали, что при использовании техники обусловливания препарат можно заменить условным стимулом — и это оказывает влияние на иммунитет животных в такой степени, что может продлить им жизнь.
Подобные исследования убедили ученых, что существует прочная связь между нервной и иммунной системами. Вполне очевидно, что раз искусственная роза или вкус ароматизированного напитка могут изменить иммунную функцию, то стресс тоже может это делать. В первой части этой главы мы обсудим влияние стресса на иммунитет и чем оно может быть полезно в стрессовых ситуациях. Во второй части главы мы поговорим о том, может ли длительный стресс из-за хронического подавления иммунитета ослаблять способность организма бороться с инфекционными заболеваниями. Это очень интересный вопрос, и ответить на него можно лишь с большой осмотрительностью и множеством оговорок. Появляются доказательства того, что стрессогенное подавление иммунитета действительно может увеличивать риск развития некоторых заболеваний и их серьезность. Но эта связь, похоже, не очень выражена и ее важность часто преувеличивают.
Чтобы оценить современные достижения в этой сложной, но важной области знаний, нужно начать с азов — с того, как вообще работает иммунная система.
Как действует иммунная система
Основная задача иммунной системы — защищать организм от возбудителей инфекций, например от вирусов, бактерий, грибков и паразитов. Этот процесс невероятно сложен. С одной стороны, иммунная система должна различать нормальные клетки и клетки-агрессоры — на жаргоне иммунологов, отличать «своих» от «чужих». Каким-то образом иммунная система помнит, как выглядит каждая клетка в нашем теле, и атакует любые клетки, где нет нашей индивидуальной «клеточной подписи» (например, бактерии). Кроме того, сталкиваясь с новым захватчиком, иммунная система способна даже создавать иммунологическую «запись» о том, на что похож этот возбудитель инфекции. Это позволяет ей подготовиться к его вторжениям в будущем. На этой способности основан принцип действия вакцинации: нам вводят небольшое количество ослабленного возбудителя инфекции, и это готовит иммунную систему к реальному нападению.
Иммунную защиту приводит в действие сложный комплекс клеток, циркулирующих в крови. Они называются лимфоцитами и моноцитами (все вместе иммунные клетки называются лейкоцитами; «циты» — это «клетки»). Есть два класса лимфоцитов: Т-клетки и В-клетки. Итеидругие формируются в костном мозге, но Т-клетки мигрируют в тимус (вилочковую железу) и достигают зрелости уже там (поэтому они и называются «Т-клетками»). В-клетки вызревают в костном мозге. В-клетки производят преимущественно антитела. Существует несколько видов Т-клеток (Т-хелперы, Т-супрессоры, цитотоксичные Т-киллеры и т. д.).
Т-клетки и В-клетки атакуют возбудителей инфекции по-разному. Т-клетки создают клеточный иммунитет (рис. 25). Когда возбудитель инфекции вторгается в организм, его распознает моноцит, который называют макрофагом. Он сообщает о чуждой частице клетке Т-хелперу. Включается тревожная сирена, и в ответ на вторжение «чужака» Т-клетки начинают рассредоточиваться по организму. Эта система сигнализации приводит к активации и быстрому распространению цитотоксичных Т-киллеров. В соответствии со своим названием они атакуют возбудителей инфекции и уничтожают их. Кстати, вирус СПИДа убивает как раз Т-клетки иммунной системы.
В-клетки действуют иначе. Они поддерживают иммунитет путем создания антител (рис. 26). Если макрофаги и Т-хелперы начали действовать, они стимулируют распространение В-клеток. Основная задача В-клеток—дифференцировать и производить антитела—большие белки, распознающие те или иные особенности вторгшегося возбудителя инфекции (как правило, его специфический белок) и присоединяющиеся к нему. Такая избирательность очень важна — форма образующегося антитела точно «подходит» к форме того или иного отличительного признака захватчика, как ключ к замку. Таким образом, антитела присоединяются к клеткам возбудителя инфекции, блокируют их и готовят к уничтожению.
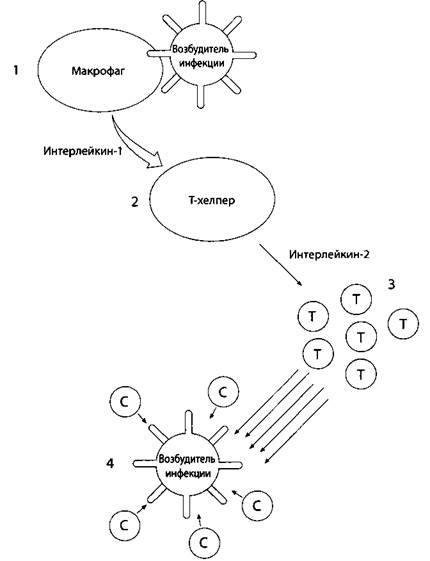
Рис. 25. Каскад клеточного иммунитета. (1) Возбудителя инфекции атакует моноцит особого типа, который называется макрофагом. (2) Макрофаг сообщает о возбудителе инфекции клетке Т-хелперу (тип лейкоцита) и вырабатывает интерлейкин-1 (IL-1), стимулирующий активность Т-хелпера. (3) ЗатемТ-хелпер вырабатывает интерлейкин-2 (IL-2), который запускает распространение!- клеток. (4) Это приводит к распространению лейкоцитов другого типа, цитотоксичных Т-киллеров, и они уничтожают возбудителя инфекции

Рис. 26. Иммунный каскад на основании антител. (1) Возбудитель инфекции сталкивается с макрофагом. (2) Макрофаг сообщает о возбудителе инфекции клеткам Т-хелперам, и они вырабатывают интерлейкин-1 (IL-1), стимулирующий активность Т-хелперов. (З)Т-хелперы вырабатывают фактор роста В-клеток, и это запускает дифференциацию и быстрое распространение лейкоцитов другого типа, В-клеток. (4) В-клетки вырабатывают специфические антитела, которые присоединяются к белкам возбудителя инфекции, подготавливая его к уничтожению многочисленной группой белков, циркулирующих в крови, которые называются комплементом
У иммунной системы есть еще один интересный аспект. Например, если разные части печени должны скоординировать ту или иную активность, у них есть преимущество соседства. Но клетки иммунной системы свободно циркулируют в крови. Чтобы тревожную иммунную сирену услышали во всех частях этой обширной системы, организм создал химические посредники (цитокины). Они также циркулируют в крови и переносят сообщения между иммунными клетками разных типов. Например, когда макрофаги впервые распознают возбудителя инфекции, они вырабатывают посредника, который называется интерлейкин-1. Он побуждает Т-хелперы вырабатывать интерлейкин-2, который стимулирует рост Т-клеток (чтобы еще больше усложнить эту схему, есть как минимум штук пять дополнительных интерлейкинов с более узкими функциями). На фронте антител Т-клетки также вырабатывают фактор роста В-клеток. Другие классы посредников, например интерфероны, активируют разные типы лимфоцитов.
Процесс сортировки, когда иммунная система проводит разграничение между «своими» и «чужими», обычно довольно эффективен (хотя некоторые коварные тропические паразиты, например возбудители шистосо- моза, научились обманывать иммунную систему, присваивая «подпись» собственных клеток организма). Иммунная система постоянно занята отделением «своих» от «чужих»: эритроциты — это мое. Брови — мои. Вирус — гадость, атакуем. Мышечные клетки — наши ребята... (рис. 27).

Но что, если в процессе иммунной сортировки случится сбой? Один очевидный тип ошибки — когда иммунная система не может распознать инфекцию-захватчика; конечно, это очень плохо. Не менее опасно, если иммунная система по ошибке признает вредным захватчиком того, кто на самом деле им не является. Например, какое-то совершенно безвредное вещество вызывает реакцию аварийного сигнала. Это может быть что-то съедобное, скажем арахис или моллюски, или что-то распыленное в воздухе и безвредное, вроде цветочной пыльцы. Но иммунная система по ошибке решила, что это не только «чужое», но и опасное, и начала активно с этим бороться. В таком случае возникает аллергия.
При втором типе гиперреакции иммунной системы за возбудителя инфекции принимается нормальная часть нашего собственного тела, и в результате она подвергается атаке. Когда иммунная система по ошибке нападает на нормальную часть тела, это может привести к самым разным и очень неприятным «аутоиммунным» заболеваниям. Например, при рассеянном склерозе нападению подвергается нервная система; при ювенильном диабете — клетки поджелудочной железы, обычно вырабатывающие инсулин. Как мы скоро увидим, стресс, как ни странно, влияет на течение аутоиммунных заболеваний.
До сих пор в этом кратком обзоре иммунной системы мы говорили о приобретенном иммунитете. Предположим, что вы в первый раз подвергаетесь действию некоего нового, опасного болезнетворного микроорганизма, назовем его патогеном X. У приобретенного иммунитета есть три особенности. Во-первых, он позволяет «научиться» атаковать именно патоген X с помощью специфических антител и иммунных клеток, способных распознавать именно этот патоген. Это дает важное преимущество: у нас появляется «маркер», на котором написано название патогена X. Во-вторых, для создания такого иммунитета нужно время: когда мы впервые сталкиваемся с патогеном X, нужно выяснить, какие антитела лучше всего ему соответствуют, и создать миллионы его копий. После этого мы можем выявлять и уничтожать патоген X в течение многих лет, и если эта специфическая защита уже есть, повторное воздействие патогена X будет только укреплять эту защиту.
Такой приобретенный иммунитет — весьма необычное изобретение, и он есть только у позвоночных животных. Но у нас есть еще и более простой, более древний механизм иммунной системы, такой же, как у живых существ совсем другого вида — у насекомых. Он называется врожденным иммунитетом. Он не предусматривает средств защиты, предназначенных специально для патогена X и особых антител, которые отличаются от тех, которые предназначены, скажем, для патогена Y. Но когда какой-то патоген поражает нас во второй раз, эта неспецифическая иммунная реакция тоже вступает в действие.
Такая общая иммунная реакция чаще всего возникает на переднем крае, где патоген завоевывает первый плацдарм, например в коже либо в ткани слизистой оболочки во рту или в носу. Как только это произошло, антитела, содержащиеся в слюне, атакуют любые «чужие» микробы. Это неспецифическая реакция, не отличающая захватчиков друг от друга. Такие антитела вырабатываются в слизистой оболочке и покрывают ее антисептическим слоем. Кроме того, в месте инфекции расширяются капилляры и иммунные клетки могут свободно поступать сюда из крови, пропитывая область инфекции. Среди этих клеток—макрофаги, нейтрофилы и неспецифические клетки-киллеры, атакующие вредоносных микробов. Расширение капилляров также увеличивает приток жидкости, содержащей белки, препятствующие попаданию агрессивных микробов в кровь. Что происходит в результате? Белки борются с микробами, а жидкость вызывает отек. Так действует врожденная иммунная система: она вызывает воспаление[53].
Итак, теперь у нас есть общее представление о том, как функционирует иммунная система. Пришло время рассмотреть, как стресс влияет на иммунитет. Естественно, этот процесс намного сложнее, чем может показаться.
Как стресс угнетает иммунную функцию?
С тех пор как Селье обнаружил первые доказательства того, что стресс способен подавлять иммунитет, прошло почти 60 лет. Селье обнаружил, что у крыс, подвергавшихся воздействию различных неприятных факторов, могут атрофироваться иммунные ткани, например тимус. С тех пор ученые намного больше узнали об иммунной системе, и оказалось, что стресс нарушает очень многие иммунные функции.
Стресс подавляет формирование лимфоцитов, замедляет их циркуляцию в крови и сокращает время, в течение которого лимфоциты, уже находящиеся в крови, в ней остаются. Это угнетает производство новых антител в ответ на возбудителя инфекции и нарушает коммуникацию между лимфоцитами, уменьшая выработку соответствующих посредников. А это подавляет врожденную иммунную реакцию, поэтому воспаления не возникает. Так действуют самые разные стрессоры — физические и психологические, у приматов, крыс, птиц и даже рыб. И конечно, у человека.
Лучше всего такой процесс подавления иммунитета виден на примере глю- кокортикоидов. Например, глюкокортикоиды могут вызывать уменьшение размеров тимуса; этот факт установлен вполне надежно. В былые времена (около 1960 года), когда мы еще не умели напрямую измерять количество глюкокортикоидов в крови, для этого использовали один косвенный способ: диагностику размеров тимуса. Чем меньше тимус, тем больше в крови глюкокортикоидов. Глюкокортикоиды угнетают формирование в тимусе новых лимфоцитов, а ведь ткань тимуса состоит преимущественно из этих новых клеток, готовых выйти в кровь. Глюкокортикоиды подавляют выработку посредников — интерлейкинов и интерферонов — и поэтому снижают чувствительность лимфоцитов к сигналу тревоги при возникновении инфекции.
Глюкокортикоиды, кроме того, вымывают лимфоциты из крови и заставляют их возвращаться в «хранилища» в иммунных тканях. Такое действие глюкокортикоидов угнетает в первую очередь Т-клетки, а не В-клетки. Это значит, что оно больше вредит клеточному иммунитету, а не иммунитету антител. И что самое интересное, глюкокортикоиды могут уничтожать лимфоциты. Это одна из самых горячих тем в медицине, получившая название запрограммированной гибели клеток[54]. Клетки запрограммированы на то, чтобы иногда совершать самоубийство. Например, если клетка начинает превращаться в злокачественную, в ней активируется функция самоуничтожения, нейтрализующая ее до того, как она начнет процесс неконтролируемого деления; несколько типов раковых образований связаны с нарушением функции запрограммированной гибели клеток. Оказывается, что глюкокортикоиды с помощью нескольких механизмов способны запускать программу самоуничтожения у лимфоцитов.
Гормоны симпатической нервной системы, бета-эндорфин и КРГ в мозге также принимают участие в подавлении иммунитета во время стресса. В отличие от воздействия на иммунитет глюкокортикоидов механизмы такого влияния пока мало изучены. Эти гормоны традиционно считались менее важными, чем глюкокортикоиды. Однако множество экспериментов показывают, что стрессоры способны подавлять иммунитет независимо от секреции глюкокортикоидов с помощью других механизмов.
Почему иммунитет подавляется во время стресса?
Механизм, с помощью которого глюкокортикоиды и другие гормоны стресса подавляют иммунитет, — очень горячая тема современной цитобиологии и молекулярной биологии, особенно что касается уничтожения лимфоцитов. Но среди всех увлекательных открытий ультрасовременной науки было бы разумно задать вопрос о том, почему организм вообще допускает, чтобы его иммунная система была подавлена во время стресса. В первой главе я предложил одно объяснение; теперь, когда мы немного лучше представляем себе процесс стрессогенного подавления иммунитета, должно быть очевидно, что то мое объяснение не имеет никакого смысла. Я предположил, что во время стресса логично «закрыть» долгосрочные строительные проекты и направить энергию на более неотложные задачи — это касается и иммунной системы. Она прекрасно умеет находить опухоли, которые могли бы убить нас через шесть месяцев, или вырабатывать антитела, которые понадобятся нам через неделю, но не нужна в чрезвычайной ситуации, возникшей прямо сейчас.
Такое объяснение имеет смысл лишь в том случае, если стресс «заморозил» иммунную систему именно в том состоянии, в котором она находится сейчас, — больше никаких расходов на иммунитет, до тех пор пока чрезвычайная ситуация не закончится. Но на самом деле происходит иначе. Стресс приводит к большому расходу энергии, необходимой для демонтажа тканей иммунной системы — эти ткани съеживаются, их клетки разрушаются. Это нельзя объяснить простой «экономией» — ведь мы платим своей энергией за разрушение иммунной системы. И это приводит нас к теории, указывающей на более долгосрочные последствия этого процесса.
Почему эволюция позволила нам заниматься такими вопиющими глупостями? Уничтожать иммунную систему во время стресса! Возможно, для этого нет никаких серьезных причин. Но это не так глупо, как кажется. Не все функции организма можно объяснить с точки зрения эволюционной адаптивности. Возможно, стрессогенное подавление иммунитета — просто побочный продукт другой, вполне адаптивной функции; оно просто идет «в нагрузку».
Но вряд ли это так. Когда возникает инфекция, иммунная система вырабатывает химический посредник интерлейкин-1. Наряду с другими функциями он стимулирует гипоталамус к выработке КРГ. Как мы говорили в главе 2, КРГ стимулирует гипофиз, заставляя его вырабатывать АКТГ, который затем вызывает выработку глюкокортикоидов надпочечниками. Они, в свою очередь, подавляют иммунную систему. Другими словами, при некоторых обстоятельствах иммунная система побуждает организм вырабатывать гормоны, которые в итоге подавляют иммунную систему. Независимо от причин этого явления иммунная система иногда поощряет подавление иммунитета. Вероятно, это не случайно[55].
В последние годы возникло множество гипотез в попытках объяснить, почему же во время стресса мы активно разрушаем собственный иммунитет при добровольном содействии самой иммунной системы. Некоторые из этих гипотез казались довольно вероятными, пока мы не узнали немного больше об иммунитете и не смогли их исключить. Другие были просто безумными, и даже я сам опрометчиво продвигал некоторые из них в первом издании этой книги. Но в последние 10 лет ответ был найден, и он перевернул все представления об этой сфере.
Сюрприз, сюрприз
Оказывается, что в первые несколько минут (скажем, около получаса) после начала действия стрессора мы не подавляем иммунитет как таковой — наоборот, мы улучшаем множество его аспектов (фаза А на приведенном ниже графике) (рис. 28). Это касается всех аспектов иммунитета, но прежде всего врожденного иммунитета. Это вполне логично — полезно активировать те аспекты иммунной системы, которые будут создавать для нас антитела в следующие несколько недель. Но еще полезнее немедленно активировать те элементы иммунной системы, которые могут выручить нас прямо сейчас. Чем больше иммунных клеток срочно отправляются в кровь, когда нервная система переживает травму, тем более сильное воспаление возникает в поврежденной ткани. Кроме того, циркулирующие в крови лимфоциты лучше вырабатывают иммунные посредники и лучше на них реагируют. И в слюну выделяется еще больше неспецифических антител врожденной иммунной системы. Такое повышение иммунитета происходит не только в ответ на инфекцию. Физические и психологические стрессоры, по-видимому, также запускают раннюю стадию активации иммунитета. Что еще интереснее, главные злодеи, подавляющие иммунитет, — глюкокортикоиды — играют в этом процессе важнейшую роль (вместе с симпатической нервной системой).
Итак, с началом действия любого стрессора наша иммунная защита усиливается. Но если стресс продолжается долго, ситуация меняется на прямо противоположную. Примерно через час продолжающаяся активация глюкокортикоидов и симпатической системы начинает подавлять иммунитет. Если действие стрессора в это время заканчивается, что нам даст подавление иммунитета? Иммунная функции вернется в то состояние, с которого началась реакция, — назад к базовой линии (фаза В). Если
сильные стрессоры действуют дольше или уровень глюкокортикоидов очень высокий, иммунная система не просто возвращается к базовой линии, а резко падает к тому уровню, где начинается подавление иммунитета (фаза С). Для большинства аспектов иммунной системы, которые можно измерить, длительное действие сильных стрессоров снижает показатели на 40-70% ниже базовой линии.

Рис. 28. Стресс ненадолго стимулирует иммунную систему
стресса длительность стресс стресса
Гипотеза о временной активации иммунной системы в начале действия стрессора вполне логична (по крайней мере не меньше, чем некоторые замысловатые теории о том, почему имеет смысл подавление иммунитета). Как и идея о том, что все, что повышается, должно в итоге снизиться. И, как мы часто видим на страницах этой книги, если у нас есть стрессор, который действует слишком долго, адаптивное снижение к базовой линии может зайти слишком далеко. И тогда мы попадаем в беду.
Почему нам потребовалось так много времени, чтобы это выяснить? Вероятно, по двум причинам. Во-первых, потому что многие методы измерения различных показателей иммунной системы только недавно стали достаточно чувствительными, чтобы отмечать небольшие, быстрые различия. Раньше ученым не удавалось «поймать» фазу А, эту быструю вспышку стимуляции иммунной системы в начале действия стрессора. Поэтому в течение многих десятилетий мы думали, что изучаем иммунную реакцию на стресс, а на самом деле изучали восстановление иммунной реакции на стресс. Во-вторых, в этой области ученые обычно исследуют действие сильных, длительных стрессоров или влияние большого количества глюкокортикоидов в течение
длительных периодов. Это создает определенный перекос в планировании и проведении экспериментов — они обычно предполагают сильное воздействие. Если при этом ничего не происходит, выбирается новая область исследований. А если что-то происходит, повторяется достаточно много раз и вы уверены, что это происходит, только после этого можно начинать думать о более тонких нюансах. Поэтому в начале исследований в этой сфере ученые изучали только те стрессоры или паттерны воздействия глюкокортикоидов, которые переводят организм в фазу С, и только позже пришло время для изучения более тонких аспектов, возникающих на фазе В.
Это произошло благодаря экспериментам Аллана Мунка из Дартмутского университета, одного из крестных отцов данной области, еще в середине 1980-х предсказавшего почти все недавние открытия. Он также предсказал ответ на другой важный вопрос. Зачем возвращать иммунную функцию к дострессовому уровню (фаза В на диаграмме)? Почему просто не оставить ее на более активированном, более высоком уровне, достигнутом в первые 30 минут, и не воспользоваться этой активацией на следующих фазах? Выражаясь метафорически, почему бы и дальше не держать армию в состоянии максимальной мобилизации? Прежде всего, это очень дорого. Что еще важнее, система, постоянно находящаяся в состоянии максимальной готовности, в какой-то момент не выдержит, и в результате «дружественного огня» может пострадать кто-то из «своих». Так может случиться и с иммунной системой, если она хронически активирована: она начинает путать с агрессором части собственного организма. Так возникают аутоиммунные заболевания.
Такие рассуждения привели Мунка к гипотезе о том, что если вы не прошли фазу В и не вернули активированную иммунную систему к базовой линии, то у вас растет риск аутоиммунных заболеваний. Эта идея была подтверждена по крайней мере в трех областях. Во-первых, можно искусственно заблокировать у крыс уровень глюкокортикоидов в низком базовом диапазоне, а затем подвергнуть их стрессу. При этом у животных возникнет фаза А (по большей части под воздействием адреналина), но не будет расти уровень глюкокортикоидов, и это не позволит им полностью перейти в фазу В. При этом у крыс возрастет риск аутоиммунных заболеваний. Во-вторых, врачам иногда приходится удалять пациенту один из двух надпочечников (источник глюкокортикоидов), как правило, из-за опухоли.
 2020-04-07
2020-04-07 107
107








