22. Поступление ксенобиотиков в организм. Поступление через органы дыхания, через кожу и через желудочно-кишечный тракт
Основные пути поступления токсических ксенобиотиков (промышленных ядов, пестицидов) в организм человека это пищеварительный тракт (около 70 %), дыхание (около 20 %) и через кожу.
Через слизистую оболочку дыхательных путей поступают ксенобиотики, находящиеся в газо- и парообразном состоянии, в виде аэрозолей и пыли.
Через кожу проникают липофильные вещества, находящиеся в жидком или газообразном состоянии при непосредственном контакте.
Проникновение ксенобиотиков через слизистую оболочку пищеварительного тракта наблюдается при аварийных ситуациях в результате заглатывания распыленных в воздухе токсических аэрозолей, при применении отравляющих веществ, при поступлении отравленных пищи и воды.
.
23. Экскреция ксенобиотиков и их метаболитов через лёгкие и почки. Экскреция ксенобиотиков печенью.
Экскреция ксенобиотиков и их метаболитов через различные выделительные системы – заключительный этап в процессе поступления и трансформации. Экскреция осуществляется через почки, легкие, кожу, кишечник, слюнные, потовые, слезные, сальные, молочные железы.
В основе почечной экскреции: клубочковая фильтрация, канальцевая секреция, канальцевая реабсорбция.
экскреция ксенобиотиков легкими. Удаляются в основном летучие и газообразные вещества (ингаляционные наркотики и их метаболиты), промышленные газы, продукты печеночной биотрансформации многих токсических веществ, в т.ч. хлорированных углеводородов, этанол.
экскреция ксенобиотиков печень осуществляется путем выделения метаболитов или конъюгатов из гепатоцитов через систему желчных ходов или обратного всасывания в синусоиды и через почки. Интенсивность желчной экскреции зависит также от соотношений между константами связывания ксенобиотиков с белками гепатоцитов и плазмой крови.
24. Пути поступления и выведения ксенобиотиков у растений.
Растения способны к метаболическому превращению ксенобиотиков, хотя, в отличие от животных, не имеют органа или специальной ткани, ответственных за их метаболизм.
Различные части растений содержат ферменты, катализирующие превращение ксенобиотиков. Так как один и тот же организм имеет участки различного возраста, то их активность неодинакова.
Микросомальная система, участвующая в процессах биотрансформации, распространена в разных растительных органах и тканях: корнях, корнеплодах, корневищах, листьях и зрелых плодах.
Растения могут запасать токсины в своих клетках в нетоксичной связанной форме (например, HCN связывается в виде цианистого гликозида).
Наиболее изучена у растений, как и у других организмов, трансформация органических ксенобиотиков, происходящая, как и у животных, за счет реакций окисления, восстановления, гидролиза и последующей конъюгации.
Цель у растений, как и у животных, одна – инактивировать ксенобиотик и довести его до растворимого состояния с тем, чтобы в дальнейшем либо изолировать в клеточных вакуолях, либо вывести через корневую систему и листья (редко).
Летальная доза синильной кислоты составляет 3,7 мг/кг (порядка 0,3 г для взрослого человека). Такое количество может содержаться меньше, чем в 100 г миндаля. Всего 10 орешков горького миндаля могут быть смертельными для ребенка.
25. Пути поступления наночастиц в организм.
Наночастицы могут проникать через органы дыхания, которые являются весьма распространенным каналом.
Частицы аэрозолей могут быть ингалированы, если их аэродинамический диаметр меньше 10 микрон.
Частицы, размером 1 нм, не могут достигнуть легочных альвеол; они депонируются в верхних областях легких.
Частицы, размером 5 нм, депонируются относительно равномерно в носу и зеве, трахее и бронхиолах и, наконец, в альвеолах.
Более 50 % наночастиц, имеющих размеры 20 нм, скапливается в альвеолах.
Наноматериалы, поступающие в почву, грунтовые воды и воды открытых водоемов в результате антропогенной деятельности, могут попадать в ткани несовершенных грибов и водорослей.
Находящиеся внутри клеток наночастицы способны оказывать влияние на метаболические процессы грибов и водорослей.
Поскольку степень токсического воздействия (угнетение фотосинтетических процессов и газообмена, образование свободных радикалов) наночастиц на эти организмы определяется в основном химическим составом и поверхностной реакционной способностью наноматериалов, при контроле их содержания в этих объектах окружающей среды необходимо учитывать, прежде всего, эти параметры.
26. Одно- и многокомпартментные системы в поступлении ксенобиотиков.
При описании закономерностей накопления и выведения ксенобиотика в организме можно рассматривать как отдельные органы или ткани (однокомпартментная система), так как организм в целом (многопартментая система), причем ксенобиотик может поступать одноразово и многоразово.
Однокомпартментная система. Разовая доза. Попадание в организм разовой дозы вещества приводит к появлению определенного количества этого вещества в тканях. В процессах метаболизма и экскреции это вещество выводится из организма с определенной скоростью. Например, была изучена скорость выведения ДДТ из организма человека. Добровольцы проглатывали определенное количество ДДТ, после чего это вещество появлялось в тканях. Концентрационная зависимость ДДТ в жировой ткани, представленная в виде функции от времени, имела экспоненциальный характер.
В этом случае зависимость, представленная в полулогарифмических координатах, выражается прямой линией, наклон которой определяет константу скорости реакции (б). Период полувыведения составил 3,7 года.
Многократное дозирование. В природной среде воздействие вещества на организм редко ограничивается разовой дозой. Если в окружающей среде вещество распределено повсеместно, организм подвергается его воздействию непрерывно. Рассмотрим, что произойдет, если организм ежедневно получает дозу в 1 г вещества, период полувыведения которого в этом организме составляет 24 ч.
27. Процессы метаболического превращения ксенобиотиков. Роль цитохрома Р-450 в метаболизме ксенобиотиков.
В качестве основного компонента монооксигеназные системы содержат терминальную оксидазу – цитохром Р-450, относящийся к гемопротеидам.
Цитохром Р-450 впервые найден в микросомах печени крыс, затем в различных органах (легкие, почки и др.) животных. Позже было установлено, что цитохром Р-450 широко распространен в живой природе не только в эукариотных, но и в прокариотных организмах.
Кроме млекопитающих и человека, эти цитохромы выделены из тканей беспозвоночных (насекомых, членистоногих и др.), птиц, микроорганизмов, растений.
Основная функция цитохрома Р-450 в организме – обезвреживание эндогенных субстратов в результате монооксигеназной реакции. В каталитических реакциях монооксигеназ цитохром Р-450 выполняет роль активного центра.
Основная функция цитохрома Р-450 в организме – обезвреживание эндогенных субстратов в результате монооксигеназной реакции. В каталитических реакциях монооксигеназ цитохром Р-450 выполняет роль активного центра. Он взаимодействует с субстратом и молекулярным кислородом, а также принимает электроны от соответствующих доноров.
Различают микросомальную, митохондриальную и бактериальную монооксигеназные системы цитохрома Р-450.
Микросомальная широко встречается у животных, растений, эукариотических микроорганизмов, включая дрожжи и плесени. Больше всего она изучена для микросом печени млекопитающих, в которых монооксигеназная система состоит из двух флавопротеинов, цитохрома b и множества других форм цитохрома Р-450. Реакция протекает на поверхности ЭР.
Митохондриальная монооксигеназа – менее изучена. Она принадлежит к числу мембрансвязанных и была обнаружена в организмах различных животных, в растениях и у эукариотических микроорганизмов. Митохондриальная система Р-450 в основном предназначена для регуляции эндогенных субстратов (стероидов), а не ксенобиотиков.
Впервые наличие цитохрома Р-450 бактериальной монооксигеназной системы установлено в бактериях Rhizobium bacteroids. В наибольшей степени она изучена на бактериях Pseudomonas putida.
28. Реакции окисления. Окисление спиртов и альдегидов. Окисление аминов. Окисление ароматических аминов.
1) Окисление спиртов и альдегидов осуществляется сравнительно малоспецифической алкогольдегидрогеназой, более специфичными альдегндоксидазами и др. ферментами:
Окисление спиртов в альдегиды или кетоны:
RCH2OH -> RCHO + Н20,
R,CHOHR2 -► R,COOR2 +Н20.
Окисление альдегидов в карбоновые кислоты:
[О]
RCHO -► RCOOH.
Ферменты дегидрогеназы удаляют водород, что приводит к образуются все более полярные вещества, которые способно диссоциировать с образованием отрицательно заряженных ионов.
2) Окисление аминов: окисления диэтиламина с нитритом в кислой среде желудка, в результате которой получается канцероген - диэтилнитрозамин.
3) Гидроксилирование кольцевых систем: алициклические кольцевые структуры гидроксилируются легче, чем ароматические.
4) Ароматизация алициклических соединений: происходит в случае окисления некоторых циклогексанкарбоновых кислот с четным числом СН2-групп в боковой цепи с участием митохондрий до бензойной кислоты. При реакциях окисления с участием фермента эпоксидазы образуется эпоксидное кольцо (реакция эпоксидации).
29. Окисление ароматических алкил-замещенных соединений. Гидроксилирование кольцевых систем. Ароматизация алициклических соединений.
Окисление ароматических алкил-замещенных соединений. Они обычно расщепляются между атомами С1 и С2 боковой цепи с образованием соответствующей ароматической кислоты:
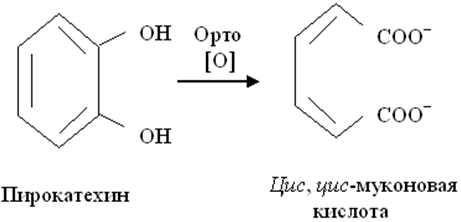
Гидроксилирование кольцевых систем. Алициклические кольцевые структуры гидроксилируются легче, чем ароматические. Это одна из причин высокой токсичности бензола, поскольку он тяжело окисляется до фенола. Если в ароматическом кольце есть неуглеродный заместитель, то гидроксилирование обычно происходит в пара-положении. Однако если последнее занято, то гидроксилирование может идти и в ортоположении с образованием в некоторых случаях канцерогенных метаболитов (например, при окислении некоторых ароматических аминов). В реакциях гидроксилирования могут участвовать ферменты микросом. Катализируют реакции оксигеназы.
Ароматизация алициклических соединений. Происходит в случае окисления некоторых циклогексанкарбоновых кислот (с четным числом СН2-групп в боковой цепи) с участием митохондрий. Конечный продукт – бензойная кислота.
30. Окисление, или окислительное замещение органической серы. Окислительное дезалкилирование О- и N-атомов. Биологическое окисление, катализируемое системами микросомальных ферментов.
) Окисление или окислительное замещение органической серы. Гетероциклическая сера обычно окисляется в сульфоксиды или ди- су льфоны. Сера в алифатических комбинациях или ароматических боковых цепях иногда замещается кислородом.
(RO)3P = S -> (RO)3P = О
Паратион параоксон
6) Окислительное дезалкилирование О- и N-атомов: реакции требуют молекулярного кислорода и осуществляются монооксигеназами (динитроанилины, фенилмочевины, симметричные триазины, фосфорорганические соединения, алкил амины и др. ксенобиотики.
а) О-дезалкилирование аромат. эфиров
б) N-дезалкилирование вторичных аминов
При окислительной биотрансформации ксенобиотиков нередко получаются более токсичные или канцерогенные соединения. Биологическое окисление, катализируемое системами микросомаль- ных ферментов, включает широкий круг реакций, но все они могут быть сведены к одному общему механизму, а именно к гидроксилированию.
31. Процессы метаболического превращения ксенобиотиков. Реакции восстановления (восстановление альдегидов и кетонов, восстановление нитро- и азогрупп, немикросомное метаболическое восстановление).
Они менее обычны, чем реакции окисления. Однако если восстановленная форма соединения лучше экскретируется из организма, то закон действия масс может сдвигать редокс-реакции в сторону восстановления. Наряду с окислительными ферментативными системами в ЭР содержатся ферменты, которые восстанавливают ксенобиотики.
1. Некоторые из альдегидов и кетонов могут восстанавливаться в спирты под действием алкогольдегидрогеназ. Однако ацетон может прямо входить в цикл аэробного метаболизма через ацетоацетат и ацетил-КоА. Реакция восстановления кетонов до спиртов имеет вид

2. Восстановление нитро- и азогрупп. Целый ряд ароматических нитросоединений, например нитробензол, паранитробензойная кислота и хлорамфеникол, восстанавливаются в соответствующие амины нитроредуктазой (нитроредуктазами), находящейся в микросомальной и растворимой фракциях печени и почек:

Немикросомное метаболическое восстановление:
а) восстановление дисульфидов (R – S – S – R). Они расщепляются с образованием тиолов;
б) восстановление двойных связей. Двойные связи некоторых алифатических или алициклических соединений могут становиться насыщенными (например, у циклогексена). Простейшие алкены и алкины часто экскретируются без изменений их структуры;
в) дегидроксилирование. Реакция гидроксилирования может обращаться. Пример – восстановление замещенных катехолов с двумя ОН-группами до соответствующих замещенных монофенолов под действием гидроксилаз печени или бактерий;
г) ароматические циклы могут восстанавливаться анаэробными микроорганизмами.
32. Процессы метаболического превращения ксенобиотиков. Гидролиз эфиров карбоновых кислот. Гидролиз амидов, гидразидов и нитрилов. Гидролиз фосфорорганических веществ.
Гидролиз. Сложные чужеродные вещества могут гидролизоваться рядом гидролитических ферментов (гидролаз), находящихся в печени и плазме крови. Установлено, что некоторые из них находятся в микросомальной фракции печени.
В зависимости от субстратной специфичности ферменты, катализирующие данные процессы, относятся к различным группам.
1. Гидролиз эфиров карбоновых кислот. Наиболее распространены в живых организмах ферменты, катализирующие гидролиз эфиров карбоновых кислот (эстеразы). Их классифицируют по группам веществ, на которые они воздействуют, и по их отношению к ингибиторам:
а) арилэстеразы гидролизуют ароматические эфиры;
б) карбоксилэстеразы гидролизуют преимущественно алифатические эфиры; участвуют в метаболизме многочисленных фосфорорганических инсектицидов;
в) холинэстергидролазы действуют наиболее эффективно на эфиры холина;
г) ацетилэстеразы подобны ферментам, указанным в первой группе, однако они по-другому реагируют на воздействие ингибиторов.
Гидролиз амидов, гидразидов и нитрилов. Эти реакции происходят в дополнение к другим реакциям биотрансформации.
Гидролиз амидной связи описан при изучении микробиологической деградации фениламидных пестицидов и происходит с участием амидаз. Многие из изученных амидаз являются внеклеточными гидролазами.
Гидролиз амидов происходит с меньшей скоростью, чем эфиров карбоновых кислот. Иногда на этом эффекте основано действие лекарственных препаратов, имеющих большой период разложения.
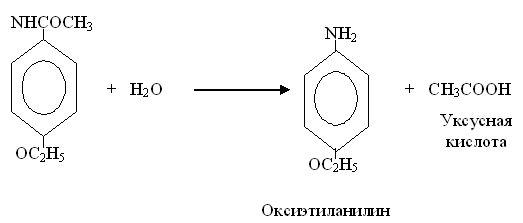
Фосфорорганические вещества гидролизуются с помощью ферментов, атакующих эфирные связи или действующих на ангидриды кислот. К первым из изученных ферментов, расщепляющих связь с фтором, относятся фторгидролаза (обнаружена в различных органах и тканях высших животных).
33. Процессы метаболического превращения ксенобиотиков. Общие сведения о конъюгации. Конъюгация с уксусной кислотой
Реакции конъюгации. К конъюгационным относятся процессы биосинтеза, в результате которых из ксенобиотиков или их метаболитов и эндогенных продуктов (глюкуроновой кислоты, ацетилсульфата, глицина и др.) образуются сложные вещества.
Схематически реакцию конъюгации можно представить в следующем виде:

Как и большинство биосинтетических реакций, это энергозависимые процессы, подразделяющиеся на две группы. В основу классификации положена природа активных промежуточных продуктов реакций.

К первому типу относятся реакции метелирования, ацетилирования, образования глюкуронидов, гликозидов и сульфатов, к второму – аминокислотная конъюгация.
В определенных ситуациях реакции конъюгации считаются высокоэффективными путями снижения токсичности некоторых ксенобиотиков. Наиболее изучены реакции конъюгации, в которых участвуют следующие молекулы.
1. Ацетат конъюгируется при участии ацетил-КоА с некоторыми ароматическими аминами и сульфонилмидами. Ацетилирование катализируется соответствующими ацетил-трансферазами.
.
34. Конъюгация с глицином, глутатионовая конъюгация, конъюгация с глюкозой, сульфатная конъюгация.
Глицин. Его конъюгация с бензойной кислотой, описанная Т. Келлером в 1842 г. – одна из первых изученных реакций биотрансформации. Глицин служит также конъюгирующим агентом при метаболизме бензойной кислоты

и при метаболизме никотиновой кислоты:
3. Глутатионовая конъюгация. Глутатион принимает участие в реакциях биотрансформации таких устойчивых ксенобиотиков, как нафталин.
Наиболее изучены реакции конъюгации, в которых участвуют следующие молекулы:
Глюкоза. Оба соединения часто используются для конъюгации; конъюгаты глюкозы особенно широко представлены в растениях, у моллюсков и насекомых. Гликозирование является основным путем детоксикации растениями чужеродных фенолов, при этом образуются довольно сложные соединения. Примером может служить продукт конъюгации пентахлорфенола с глюкозой.
Сульфатная конъюгация (сульфатирование) – один из древних видов биотрансформации. В нее вступают фенолы, спирты, ароматические амины, гидроксиламины, некоторые стероиды. Происходит с участием сульфат-аденилтрансферазы, аденил-сульфаткиназы, возможно, и других ферментов группы сульфотрансфераз, локализованных в цитоплазме гепатоцитов и других клеток.
35. Факторы, влияющие на биотрансформацию ксенобиотиков.
Видовые различия и различия внутри одного вида. Различия процессов биотрансформации между видами могут быть количественными (идентичные реакции протекают с неодинаковой скоростью) и качественными (различные метаболические реакции).
Возраст. Процесс развитияхарактеризуется резким увеличением активности ферментов, в том числе и отвечающих за метаболизм ксенобиотиков. Это является фактором адаптации новорожденных к новым условиям существования. У новорожденных отсутствуют микросомальные ферменты, в том числе и цитохром Р-450.
Их появление происходит в течение первых дней после рождения и достигает максимума примерно через 30 дней (4 недели) у крыс, через 8 недель у человека.
Таким образом, эмбрионы и новорожденные особенно чувствительны к токсикантам. Способность новорожденных синтезировать конъюгаты также заметно снижена, например глюкурониды у них синтезируются достаточно медленно вследствие дефицита фермента глюкурония трансферазы.
Микросомальные энзиматические системы плода и новорожденных можно стимулировать введением химических активаторов. Например, введение новорожденным крысам 3,4-бензопирена усиливает биосинтез глюкуронидов в печени.
Пол. У взрослых самцов чужеродные соединения метаболизируется быстрее, чем у взрослых самок. Это обусловлено действием половых гормонов на синтез ферментов микросомного окисления, так как эффект проявляется только при достижении половой зрелости и исчезает при кастрации животных.
Питание и диета. Активность энзимов метаболизма чужеродных соединений отчетливо зависит от питания животного. У мышей голодание приводит к уменьшению скорости гидроксилирования одних ксенобиотиков и увеличению других. У крыс, находящихся на диете с дефицитом белка, наблюдается уменьшение активности ферментов моноксигеназных систем.
Гормоны. Введение крысам тироксина вызывает уменьшение активности ферментов монооксигеназной системы. Напротив, стероидные гормоны стимулируют активность микросомных ферментов, в первую очередь благодаря индукции их синтеза.
Беременность. В конце беременности заметно уменьшается глюкуронидная конъюгация ксенобиотиков, вероятно, из-за наличия в тканях прогестерона – ингибитора глюкуронилтрансферазной активности в печени и других тканях.
36. Неорганические ксенобиотики. Металлы в живой клетке.

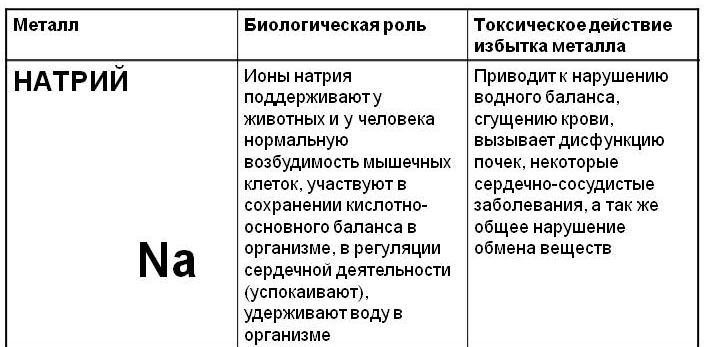
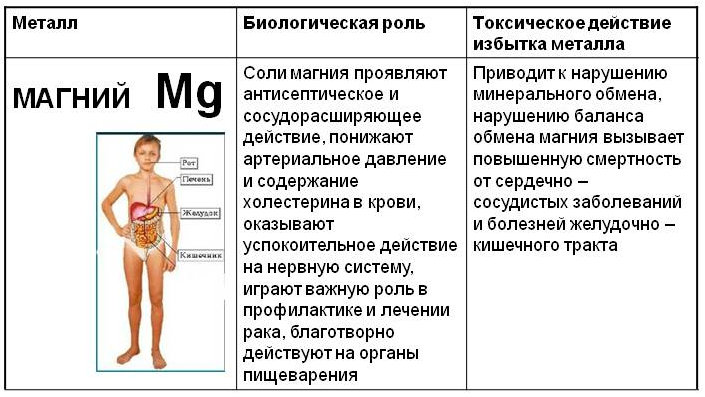
37. Механизмы биологического действия хелатирующих агентов.
Наличие двухфазной реакции организма на металлы свидетельствует о существовании двух разных механизмов действия хелатирующего агента в биологических системах:
I – удаление металлов из клетки или «маскировка» их в клетке (в виде комплексов);
 2020-04-07
2020-04-07 234
234








